Clear Sky Science · ar
الارتباط بالأحماض الأمينية والفيروس من قِبل ناقل الأحماض الأمينية الكاتيوني عالي الألفة 1 (CAT1) من Mus musculus
كيف تتحكم الخلايا في اللبنات الحيوية وتواجه الدخيل الفيروسي
تعتمد خلايانا على تدفق ثابت لبعض الأحماض الأمينية — جزيئات صغيرة تبني البروتينات وتغذي تفاعلات حيوية أساسية. في الوقت نفسه، طورت بعض الفيروسات آليات لاختطاف البوابات نفسها التي تسمح بدخول هذه المغذيات إلى الخلايا. تكشف هذه الدراسة، بتفصيل ذري، كيف أن بوابة مماثلة في الفئران تُدعى CAT1 تنقل الأحماض الأمينية موجبة الشحنة عبر غشاء الخلية وفي الوقت نفسه تعمل مقر دخول لفيروس يسبب اللوكيميا. يساعد فهم هذه الوظيفة المزدوجة في تفسير كيف تستشعر الخلايا المغذيات، وكيف تزدهر بعض الأورام، ولماذا تصيب فيروسات محددة بعض الأنواع ولا تصيب أخرى.
حارس البروتين على سطح الخلية
يستقر CAT1 في غشاء الخلية الخارجي ويتخصص في إدخال ثلاثة أحماض أمينية موجبة الشحنة: الأرجينين والليسين والأورنيثين. هذه الجزيئات حيوية لتشكيل البروتينات، وإزالة الأمونيا السامة عبر دورة اليوريا، وتشغيل مسارات النمو، وتوليد جزيئات إشارات مثل أكسيد النيتريك. عندما يعطل CAT1 عمله، تموت الفئران بعد الولادة مباشرة، وفي البشر يرتبط الناقل المماثل بسرطانات المبيض والقولون. ومن المثير للاهتمام أن البروتين نفسه يعمل أيضاً كمستقبل رئيسي لفيروس رترو يُعرف باسم فيروس صداقة الفئران المسبب للوكيميا، الذي يستخدم CAT1 للتعرف على الخلايا القارضة وإصابتها.
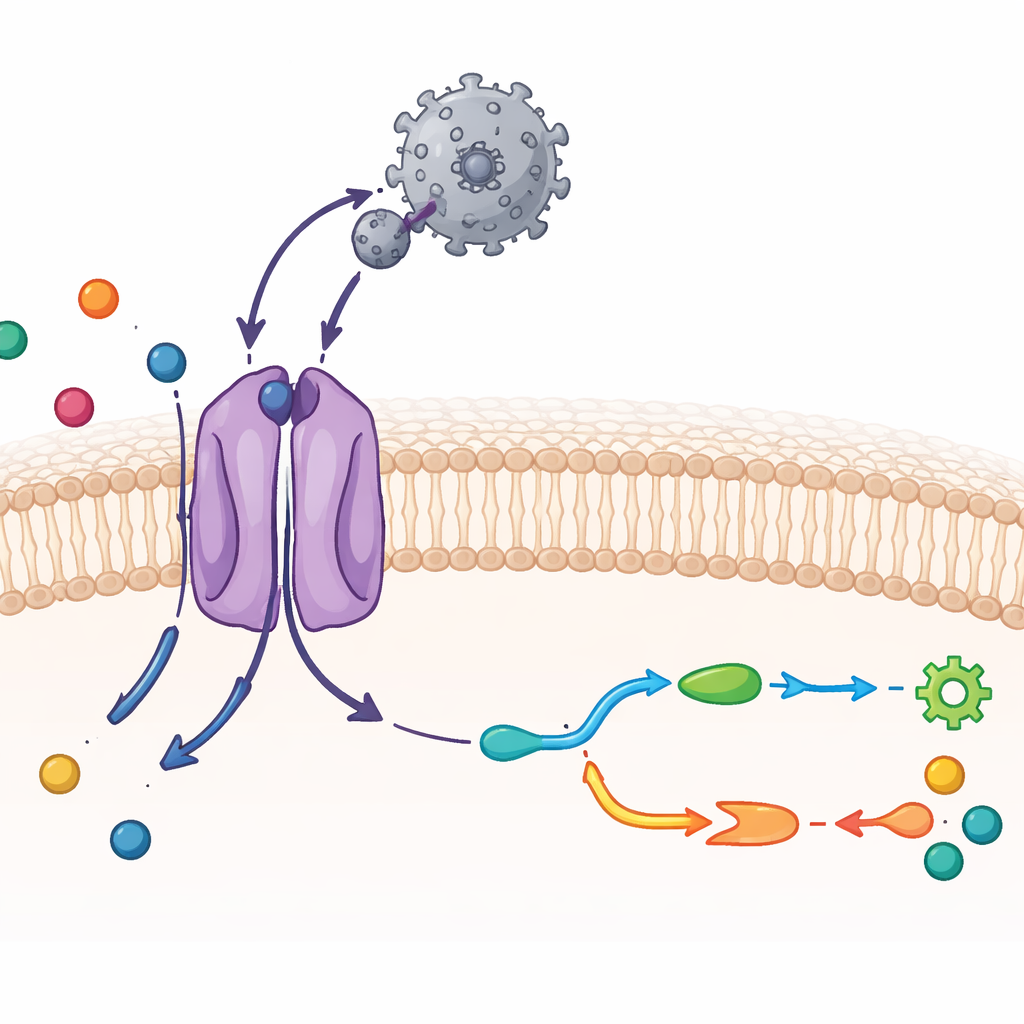
رؤية CAT1 وفيروس بتفصيل ذري
استخدم الباحثون المجهر الإلكتروني بالتبريد، تقنية تصور الجزيئات المجمدة بدقة تقارب الذرات، جنباً إلى جنب مع اختبارات بيوكيميائية. نظفوا CAT1 الفأري وخلطوه مع المنطقة الخارجية الرابطة للفيروس، قطعة بروتينية مدمجة تلتصق بالناقلة. تُظهر البنية الناتجة مركباً بنسبة واحد إلى واحد: نطاق ربط فيروسي واحد ملتصق بجزيء CAT1 واحد في الغشاء. أمكن تصور معظم مقاطع الناقل الأربعة عشرة العابرة للغشاء، بما في ذلك مقطعين إضافيين فريدين لهذه العائلة. يحتضن المقطع الفيروسي حلقة مكشوفة على الجانب الخارجي من CAT1 ويشكل شبكة كثيفة من روابط الهيدروجين، ما يفسر تمسكه الشديد. ومع ذلك، يكاد البروتين الفيروسي نفسه لا يغير شكله، ما يساعد في الحفاظ على هذا التفاعل القوي بتكلفة طاقية قليلة.
كيف يختار CAT1 حمولته ويحركها
داخل CAT1، حدد الفريق الجيب الدقيق حيث يرتبط الأرجينين والليسين والأورنيثين. يحتجز عمود كل حمض أميني في مكانه حلقة من ذرات البروتين تشكل روابط هيدروجينية متعددة، في حين تُستقر السلاسل الجانبية داخل تجويف مبطن بمجموعات جانبية موضوعة بعناية وبقاعدة سالبة الشحنة حرجة واحدة. عندما نُقلت هذه البقايا الحمضية أو نقاط التماس المجاورة بتغيرات طفرية، فقد CAT1 قدرته على الاستقرار عند إضافة الأحماض الأمينية، مما كشف عن أهميتها في التعرف. أظهر مقارنة البنى مع الأرجينين والليسين والأورنيثين المرتبطين أن CAT1 يمسك الثلاثة بطرق متقاربة جداً، متكيفاً فقط بشكل طفيف لاستيعاب اختلافات طول السلسلة الجانبية. تفسر هذه التفاصيل لماذا يفضل CAT1 الأحماض الأمينية موجبة الشحنة بقوة ويستبعد إلى حد كبير المحايدة منها.
بوابة متحركة لكنها تحتفظ بالفيروس
من خلال تصوير CAT1 بوجود الحمض الأميني وبدونه، التقط المؤلفون خطوتين رئيسيتين من دورة عمله. في أحدهما، يُغلق موقع الحمولة من الجانبين — حالة «مقطوعة» يُحبس فيها الحمض الأميني بالداخل. في الأخرى، يفتح الموقع نحو داخل الخلية، مما يسمح بإطلاق الحمولة. تنطوي هذه التغيرات على حركات تأرجحية لعدة مقاطع عابرة للغشاء وببتيد «قفل» مرن على السطح الداخلي يبدو أنه يتحكم في الفتح باتجاه الداخل. ومن الجدير بالملاحظة أن منطقة ربط الفيروس على الجانب الخارجي تتحرك فقط طفيفاً وتبقى ملتصقة بقوة أثناء هذه التحولات. يدعم هذا الأدلة السابقة أن ربط الفيروس ونقل الأحماض الأمينية مستقلان إلى حد كبير — فـ CAT1 يمكنه الاستمرار في تغذية الخلية حتى أثناء عمله كمستقبل فيروسي.
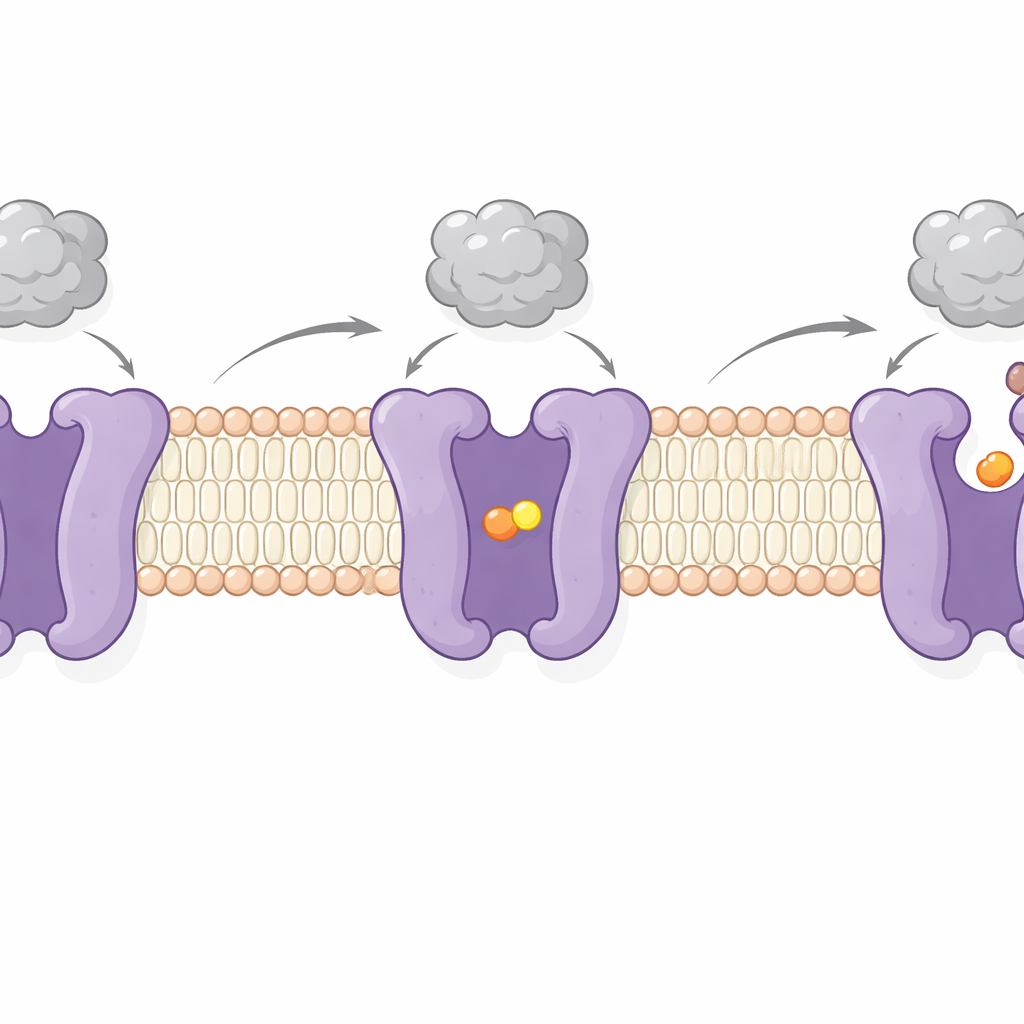
لماذا تهم هذه الوظيفة المزدوجة
من خلال رسم خريطة دقيقة لكيفية تعرف CAT1 على كل من المغذيات والفيروس، يوضح هذا العمل سبب إصابة فيروس لوكيميا الصداقة للقوارض وليس البشر: يتفاعل الفيروس مع حلقة خارجية قصيرة من CAT1 تختلف اختلافاً كبيراً بين الأنواع. إن استبدال هذا المقطع من الفأر إلى CAT1 البشري يكفي لاستعادة الربط الفيروسي في اختبارات الخلايا. كما تشير البنى إلى كيفية مساهمة CAT1 في إحساس الخلايا بمستويات الأرجينين ونقل تلك المعلومات إلى مسارات التحكم في النمو، وتحدد مواقع محددة حيث قد تعدل الأدوية أو المركبات الكيميائية النقل أو تمنع دخول الفيروس. في الجوهر، تُظهر الدراسة كيف يمكن لبروتين غشائي واحد أن يعمل كصمام مغذي وكمقبض فيروسي في آن واحد، مع وجوه مختلفة لنفس الجزيء تؤدي أدواراً تدعم الحياة وتسهِم في المرض.
الاستشهاد: Ye, M., Liang, Z., Zhou, D. et al. Amino acid and viral binding by the high-affinity Cationic Amino acid Transporter 1 (CAT1) from Mus musculus. Nat Commun 17, 2829 (2026). https://doi.org/10.1038/s41467-026-69421-0
الكلمات المفتاحية: نقل الأحماض الأمينية, بنية بروتين الغشاء, مستقبلات فيروسية, استقلاب الأرجينين, تخصص العائل