Clear Sky Science · it
Trasporto di amminoacidi e legame virale da parte del trasportatore cationico ad alta affinità 1 (CAT1) di Mus musculus
Come le cellule controllano i mattoni vitali e affrontano gli invasori virali
Le nostre cellule dipendono da un flusso costante di alcuni amminoacidi—piccole molecole che costruiscono le proteine e alimentano reazioni chiave. Allo stesso tempo, alcuni virus hanno evoluto meccanismi per dirottare le stesse porte che introducono questi nutrienti nelle cellule. Questo studio rivela, in dettaglio atomico, come una di queste porte nei topi, chiamata CAT1, trasporta amminoacidi carichi positivamente attraverso la membrana cellulare e funge anche da punto d'ingresso per un virus che causa leucemia. Capire questo duplice ruolo aiuta a spiegare come le cellule percepiscono i nutrienti, come alcuni tumori prosperano e perché specifici virus infettano alcune specie ma non altre.
La guardiana proteica sulla superficie cellulare
CAT1 è inserita nella membrana esterna della cellula e si specializza nell'importare tre amminoacidi carichi positivamente: arginina, lisina e ornitina. Queste molecole sono vitali per la conformazione delle proteine, per rimuovere l'ammoniaca tossica attraverso il ciclo dell'urea, per attivare vie di crescita e per generare messaggeri come l'ossido nitrico. Quando CAT1 non funziona correttamente, i topi muoiono poco dopo la nascita, e nell'uomo il trasportatore corrispondente è associato a tumori dell'ovaio e del colon. È interessante che la stessa proteina svolga anche il ruolo di recettore principale per un retrovirus murino noto come Friend murine leukemia virus, che usa CAT1 per riconoscere e infettare le cellule dei roditori.
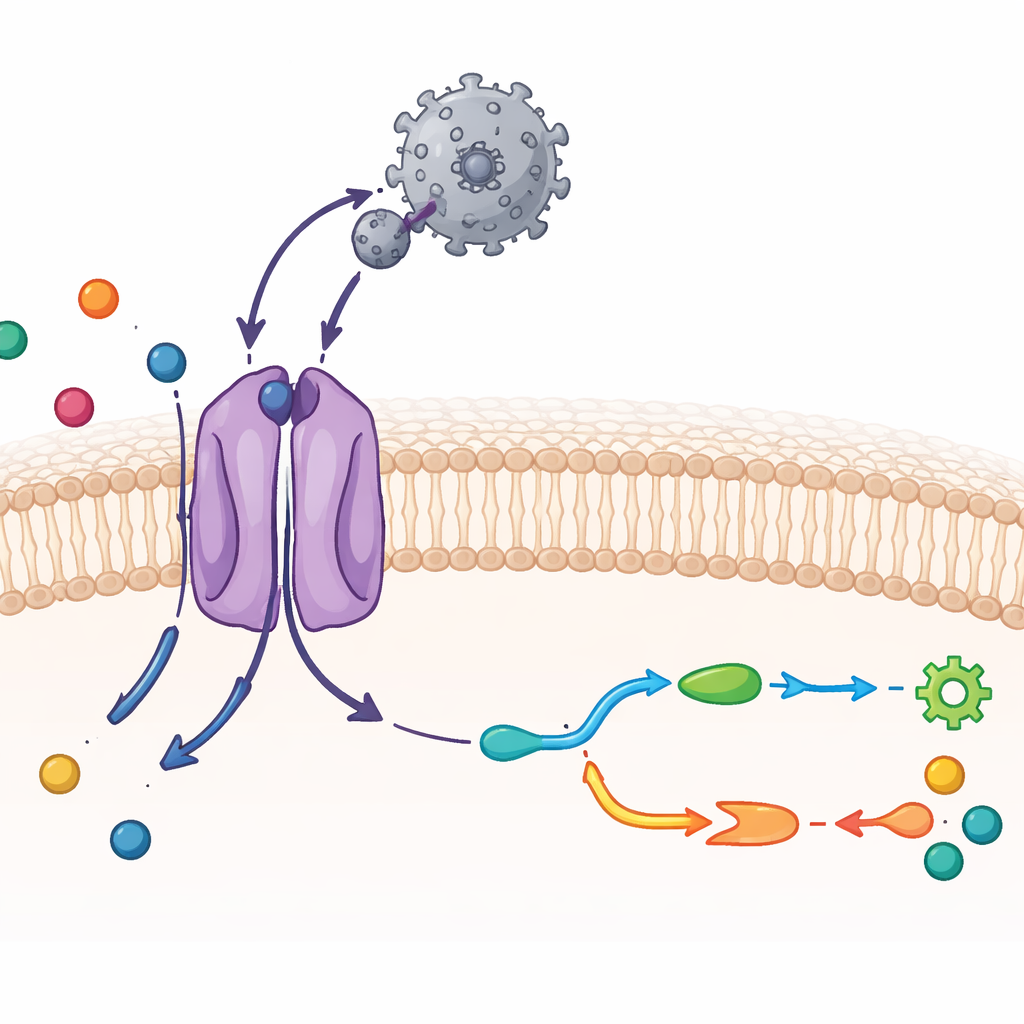
Osservare CAT1 e un virus in dettaglio atomico
I ricercatori hanno utilizzato la crio-microscopia elettronica, una tecnica che imageggia molecole congelate a risoluzione prossima all'atomica, insieme a test biochimici. Hanno purificato CAT1 murino e lo hanno mescolato con la regione esterna di legame del virus, un frammento proteico compatto che si attacca al trasportatore. La struttura risultante mostra un complesso uno-a-uno: un singolo dominio legante virale attaccato a una singola molecola di CAT1 nella membrana. La maggior parte dei 14 segmenti transmembrana del trasportatore è stata visualizzata, incluse due eliche addizionali caratteristiche di questa famiglia. Il frammento virale avvolge un'ansa esposta sul lato esterno di CAT1 e forma una fitta rete di legami a idrogeno, che spiega la sua presa straordinariamente salda. Eppure la proteina virale cambia poco la sua conformazione, il che favorisce il mantenimento di questa forte interazione con un basso costo energetico.
Come CAT1 sceglie e muove il suo carico
All'interno di CAT1, il gruppo ha identificato la tasca precisa in cui si legano arginina, lisina e ornitina. Lo scheletro di ciascun amminoacido è mantenuto in posizione da un anello di atomi proteici che forma molteplici legami a idrogeno, mentre le catene laterali sono alloggiate in una cavità rivestita da gruppi laterali posizionati con cura e da un unico residuo carico negativamente critico. Quando questo residuo acido o punti di contatto vicini sono stati alterati per mutazione, CAT1 ha perso la capacità di stabilizzare il legame con gli amminoacidi aggiunti, rivelandone l'importanza nel riconoscimento. Il confronto delle strutture con arginina, lisina e ornitina legate ha mostrato che CAT1 afferra tutti e tre quasi allo stesso modo, adattandosi solo leggermente per accomodare le differenze nella lunghezza della catena laterale. Questi dettagli spiegano perché CAT1 preferisce nettamente gli amminoacidi carichi positivamente ed esclude in gran parte quelli neutri.
Un cancello che si muove ma mantiene il virus
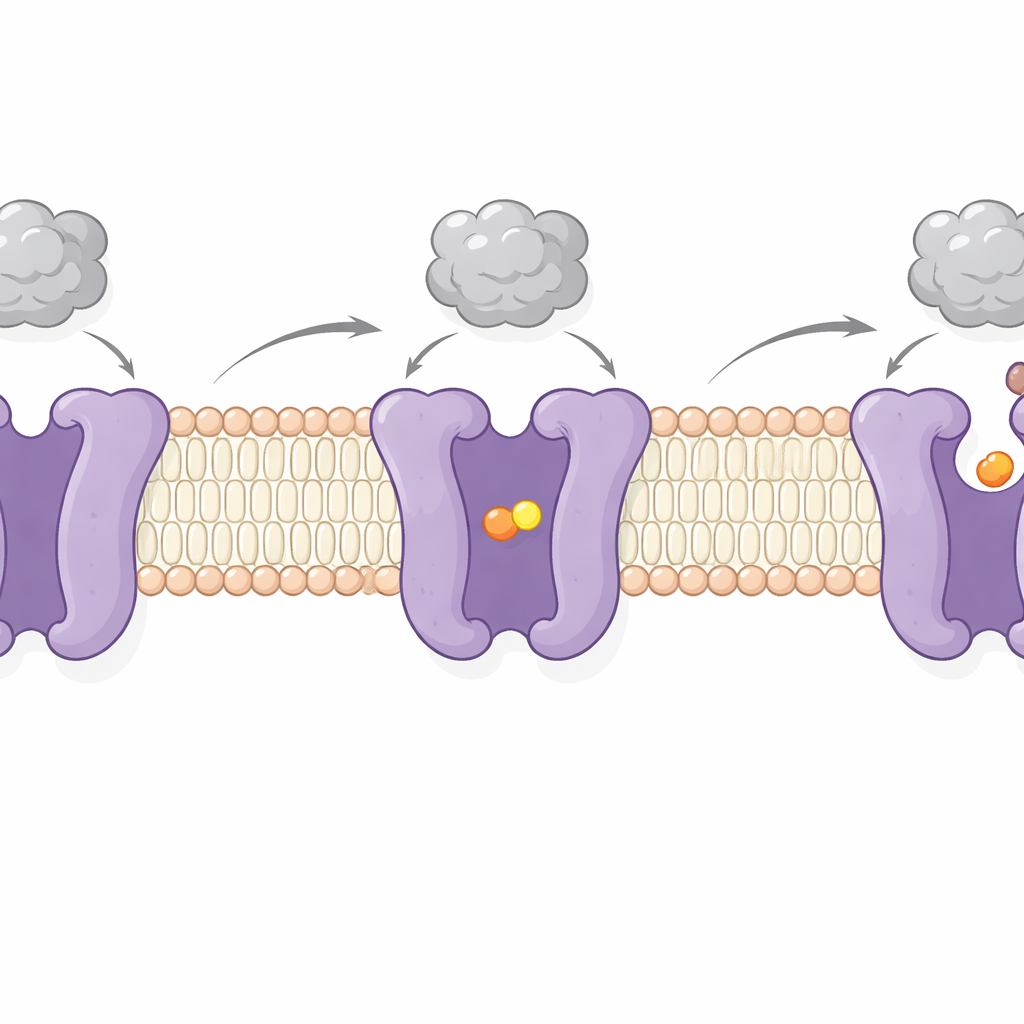
Immaginando CAT1 con e senza amminoacido legato, gli autori hanno catturato due fasi chiave del suo ciclo di funzionamento. In una, il sito del carico è isolato da entrambi i lati della membrana—uno stato “occluso” in cui l'amminoacido è bloccato all'interno. Nell'altra, il sito si apre verso l'interno della cellula, consentendo il rilascio del carico. Questi cambiamenti comportano movimenti oscillatori di diversi segmenti transmembrana e di un peptide "chiavistello" flessibile sulla superficie interna che sembra controllare l'apertura verso l'interno. È notevole che la regione di legame virale sul lato esterno si muova solo leggermente e rimanga saldamente attaccata durante questi spostamenti. Ciò supporta evidenze precedenti secondo cui l'aggancio virale e il trasporto degli amminoacidi sono in gran parte indipendenti—CAT1 può continuare a nutrire la cellula anche mentre funge da recettore virale.
Perché questo doppio ruolo è importante
Mappando esattamente come CAT1 riconosce sia i nutrienti sia un virus, questo lavoro chiarisce perché il virus della leucemia Friend infetta i roditori ma non gli umani: il virus interagisce con una breve ansa esterna di CAT1 che differisce marcantemente tra le specie. Sostituire questo segmento del topo in CAT1 umano è sufficiente a ripristinare il legame virale nei test cellulari. Le strutture suggeriscono anche come CAT1 aiuti le cellule a percepire i livelli di arginina e a trasmettere quell'informazione alle vie di controllo della crescita, e indicano siti specifici dove farmaci o modificatori chimici potrebbero modulare il trasporto o bloccare l'ingresso virale. In sostanza, lo studio mostra come una singola proteina di membrana possa funzionare sia da valvola nutritiva sia da maniglia per il virus, con facce diverse della stessa molecola che svolgono ruoli essenziali per la vita e per la promozione della malattia.
Citazione: Ye, M., Liang, Z., Zhou, D. et al. Amino acid and viral binding by the high-affinity Cationic Amino acid Transporter 1 (CAT1) from Mus musculus. Nat Commun 17, 2829 (2026). https://doi.org/10.1038/s41467-026-69421-0
Parole chiave: trasporto di amminoacidi, struttura delle proteine di membrana, recettori virali, metabolismo dell'arginina