Clear Sky Science · ja
マウスの高親和性陽イオン性アミノ酸トランスポーター1(CAT1)によるアミノ酸およびウイルス結合
細胞が必須の構成要素を制御し、ウイルスに直面する仕組み
細胞はタンパク質を構築し重要な反応を駆動するために、特定のアミノ酸を安定的に取り込むことに依存しています。同時に、いくつかのウイルスはこれらの栄養素を細胞に導入する通路を乗っ取るよう進化してきました。本研究は、マウスにおける一つの通路であるCAT1が、陽イオン性アミノ酸を細胞膜を越えて運ぶと同時に、白血病を引き起こすウイルスの侵入ドックとしても機能する様子を原子レベルで明らかにします。この二重の役割を理解することで、細胞が栄養を感知する仕組み、一部のがんがどのように増殖するか、特定のウイルスがある種に感染し他の種には感染しない理由が説明されます。
細胞表面にあるタンパク質の門番
CAT1は細胞の外膜に位置し、アルギニン、リシン、オルニチンという三つの陽に帯電したアミノ酸の取り込みを専門としています。これらの分子はタンパク質の構築、尿素回路による有毒なアンモニアの除去、成長経路の活性化、そして一酸化窒素などのシグナル分子の生成に不可欠です。CAT1が正常に働かないとマウスは出生直後に致命的となり、人間では関連するトランスポーターが卵巣や結腸のがんと関連づけられています。興味深いことに、同じタンパク質がFriend murine leukemia virusとして知られるマウスのレトロウイルスの主要受容体としても働き、このウイルスはCAT1を用いて齧歯類の細胞を認識し感染します。
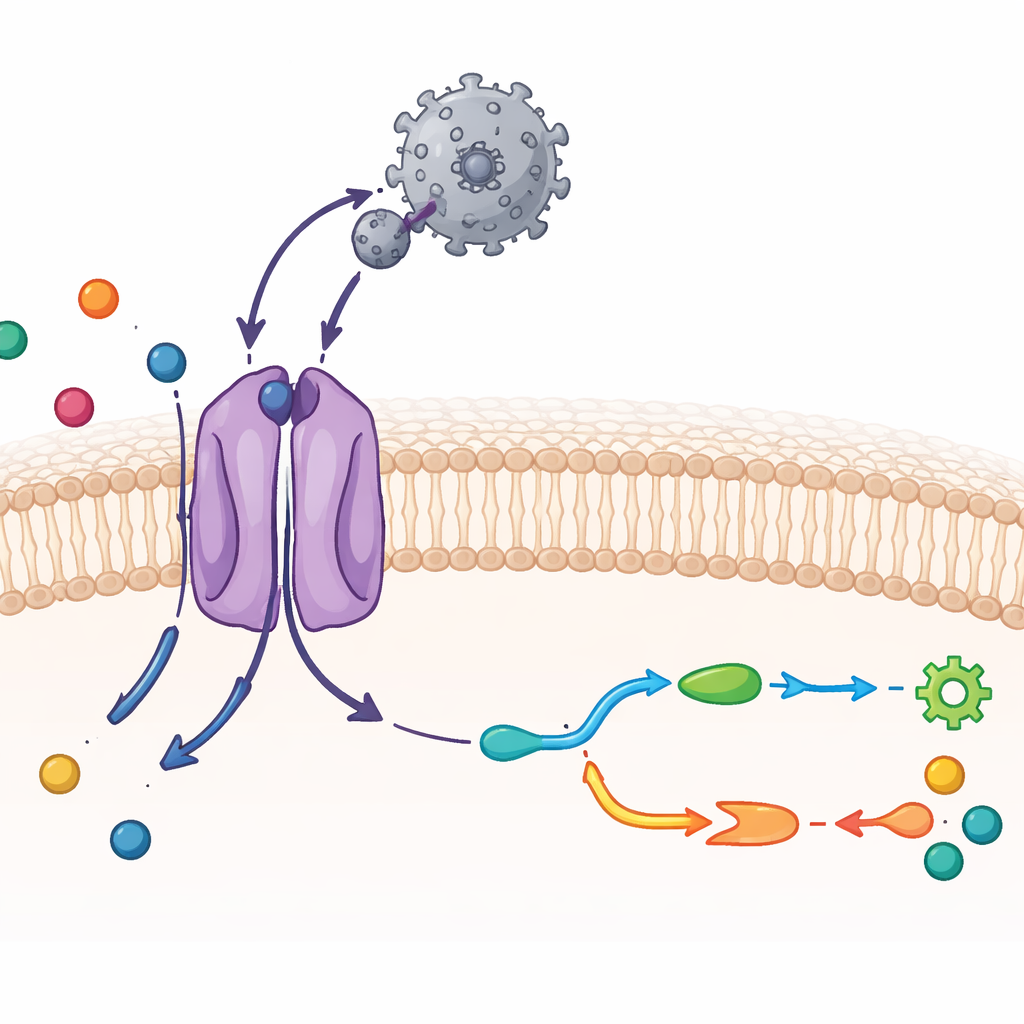
CAT1とウイルスを原子レベルで可視化する
研究者たちはクライオ電子顕微鏡法(冷凍分子をほぼ原子分解能で撮像する技術)と生化学的検査を組み合わせて解析しました。彼らはマウスCAT1を精製し、トランスポーターに結合するウイルスの外側結合領域というコンパクトなタンパク質断片と混合しました。得られた構造は1対1の複合体を示しており、単一のウイルス結合ドメインが膜中の単一CAT1分子に付着しています。トランスポーターの14本の膜貫通セグメントの大部分が可視化され、そのうちこのファミリーに特有の二つの追加セグメントも含まれていました。ウイルス断片はCAT1の外側に露出したループに密着し、水素結合の密な網を形成して非常に強い結合を説明します。一方でウイルス側のタンパク質自体はほとんど形を変えず、低いエネルギーコストで強固な相互作用を維持するのに寄与しています。
CAT1が荷を選び移動させる仕組み
CAT1の内部で、研究チームはアルギニン、リシン、オルニチンが結合する正確なポケットを同定しました。各アミノ酸の骨格は複数の水素結合を形成するタンパク質原子の輪によって固定され、側鎖は慎重に配置された官能基と単一の重要な負に帯電した残基で裏打ちされた空洞に収まっています。この酸性残基や近傍の接触点を変異させると、アミノ酸が添加された際にCAT1が安定化できなくなり、認識におけるこれらの部位の重要性が明らかになりました。アルギニン、リシン、オルニチンを結合した構造を比較すると、CAT1は側鎖の長さの違いにわずかに対応するだけで、ほぼ同じ方式で三者を把握していることが示されました。これらの詳細は、CAT1がなぜ正に帯電したアミノ酸を強く好み、ほとんど中性のアミノ酸を排除するのかを説明します。
動く門だがウイルスはつかんだまま
アミノ酸結合の有無でCAT1を撮像することで、著者らはその作動サイクルの二つの重要な段階を捉えました。一つは貨物部位が膜の両側から遮断される「遮蔽(occluded)」状態で、アミノ酸が内部に閉じ込められています。もう一つは細胞内側に向かって開き、貨物を放出する状態です。これらの変化には複数の膜貫通セグメントの揺動運動や、細胞内面の柔軟な「ラッチ」ペプチドの動きが関与し、内側への開口を制御しているように見えます。注目すべきは、外側のウイルス結合領域はわずかにしか動かず、これらの変化の間もしっかりと付着したままであることです。これはウイルスのドッキングとアミノ酸輸送が大部分で独立しているという以前の証拠を支持しており、CAT1はウイルス受容体として機能しながらも細胞への栄養供給を続けられることを示唆します。
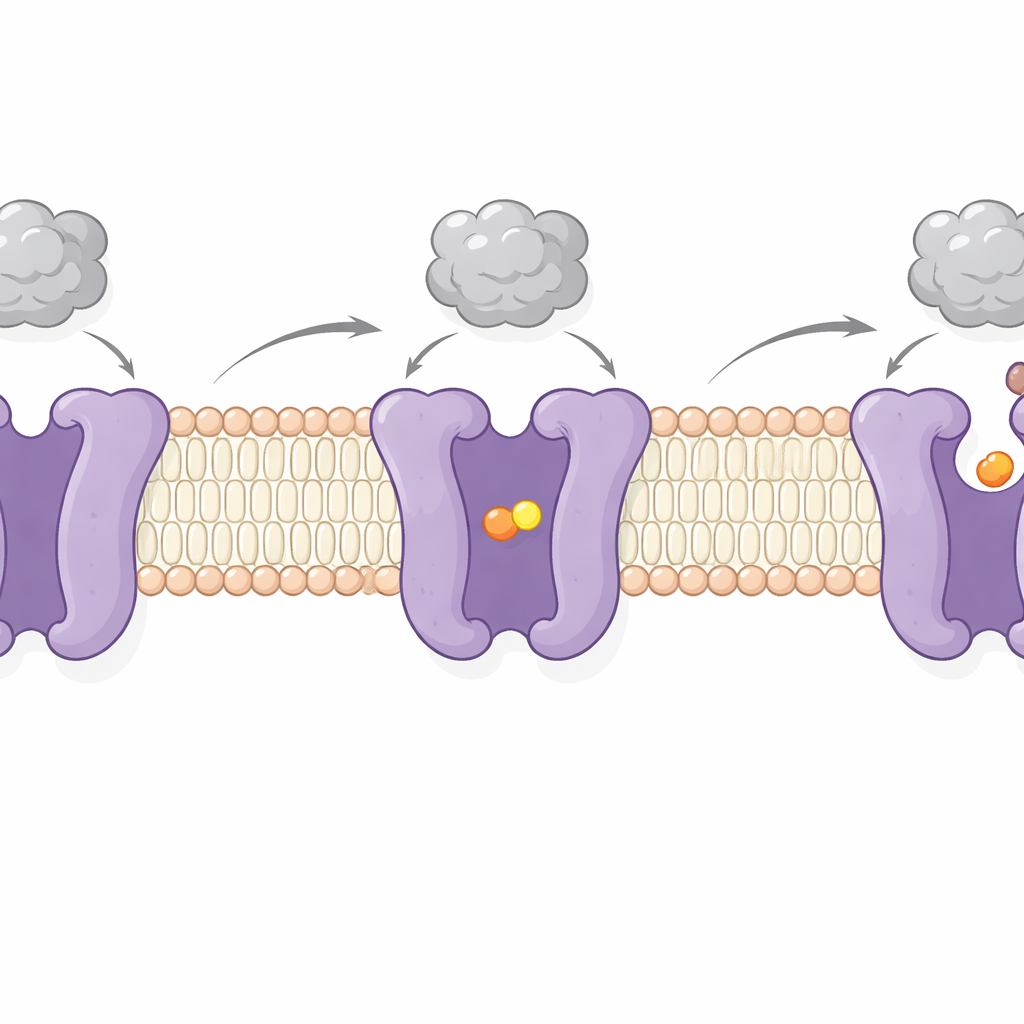
この二重の役割が重要である理由
CAT1が栄養とウイルスの両方をどのように認識するかを正確に写し出すことで、この研究はFriend白血病ウイルスがなぜ齧歯類に感染し人間には感染しないのかを明らかにします:ウイルスは種間で大きく異なるCAT1の短い外側ループに結合します。マウス由来のこの区間をヒトCAT1に置換すると、細胞試験でウイルス結合が回復するのに十分です。構造はまた、CAT1がアルギニン濃度を細胞が感知し成長制御経路へ伝える手助けをする仕組みの手がかりを与え、輸送を調節したりウイルスの侵入を阻止したりするための薬剤や化学的修飾が標的にできる特定部位を示しています。本質的に、本研究は単一の膜タンパク質が栄養の弁としてもウイルスの把手としても働きうることを示しており、同一分子の異なる面が生命維持と疾病促進の両役割を担うことを明らかにしています。
引用: Ye, M., Liang, Z., Zhou, D. et al. Amino acid and viral binding by the high-affinity Cationic Amino acid Transporter 1 (CAT1) from Mus musculus. Nat Commun 17, 2829 (2026). https://doi.org/10.1038/s41467-026-69421-0
キーワード: アミノ酸輸送, 膜タンパク質構造, ウイルス受容体, アルギニン代謝, 宿主トロピズム