Clear Sky Science · zh
EZH2 与 DNA 甲基化相互作用介导神经内分泌前列腺癌谱系可塑性
为何癌细胞身份很重要
前列腺肿瘤并非始终保持不变。有些肿瘤最初依赖男性激素并对常规治疗有反应,但随后会转变为一种更具侵袭性的形式——神经内分泌前列腺癌。这种形态可变性称为谱系可塑性,帮助肿瘤逃避免疫与治疗,是治疗失败的主要原因之一。本综述研究探讨了 DNA 及其包装上的两种化学“关闭开关”如何协同控制这一危险的身份转换,以及阻断其中一个开关如何导致另一个开关补偿性地发挥作用。
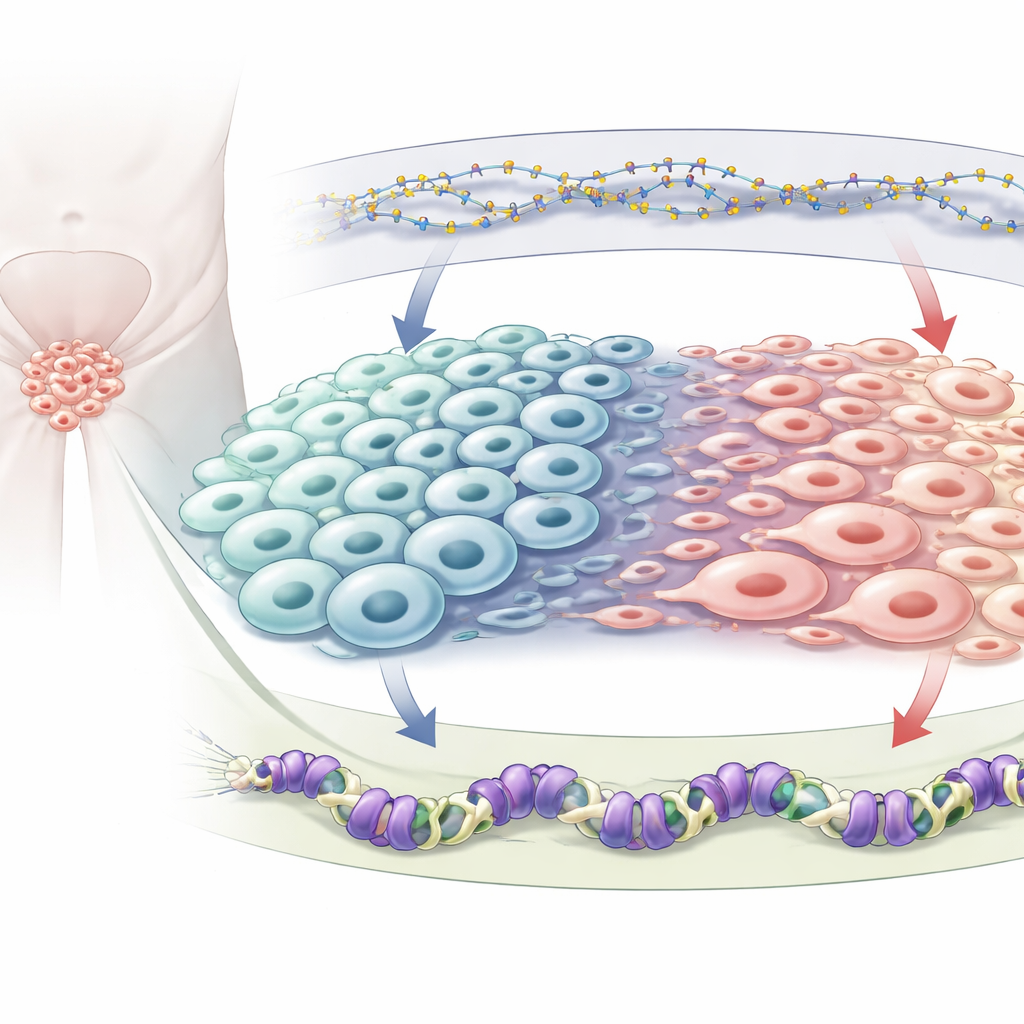
基因组上的两道化学刹车
每个细胞携带相同的基因,但化学标记决定哪些基因被开启或关闭。作者关注两类抑制性标记。一类是 DNA 甲基化,即小的化学基团直接附着在 DNA 上,通常沉默邻近基因;这一过程由名为 DNMT1 的酶维持。另一类是称为 H3K27me3 的标记,位于缠绕 DNA 的组蛋白上,由蛋白 EZH2(多梳抑制复合体 2 的一部分)添加。已知这两套系统在前列腺癌中会发生变化,尤其是在肿瘤变为神经内分泌型时,但它们如何相互影响并共同引导细胞身份尚未被清晰描绘。
标记侵袭性前列腺肿瘤的模式
研究者利用基因工程小鼠、患者肿瘤样本和体外培养的类器官,比对典型的去势耐受性前列腺腺癌与神经内分泌前列腺癌。他们发现两种状态之间 DNA 甲基化发生了一致性变化:数百个基因组区域丢失甲基化,而另一些区域则获得甲基化。引人注目的是,在神经内分泌肿瘤中变得去甲基化的区域常常积累更多与 EZH2 相关的 H3K27me3 标记,尽管这两种抑制系统通常被认为互相排斥。许多这些区域位于与神经样特征相关的基因附近,以及所谓的双价启动子处,这些启动子使发育基因保持一种可快速开启或关闭的待命状态。
当一只刹车被松开时会发生什么
为探明因果关系,团队在易于演化为神经内分泌肿瘤的小鼠模型中禁用 EZH2,并在患者来源的类器官中使用 EZH2 抑制药物。在两种情境下,全局 DNA 甲基化图谱都发生了大规模重编排。先前被 EZH2 靶向的区域常变得甲基化增加,而其他区段则失去甲基化并激活了与神经分化及已知神经内分泌特征相关的基因。换言之,去除基于 H3K27me3 的刹车允许 DNA 甲基化系统迁入并保持许多原本被沉默的基因处于关闭状态,同时在其他位点松动控制,从而强化神经内分泌状态。
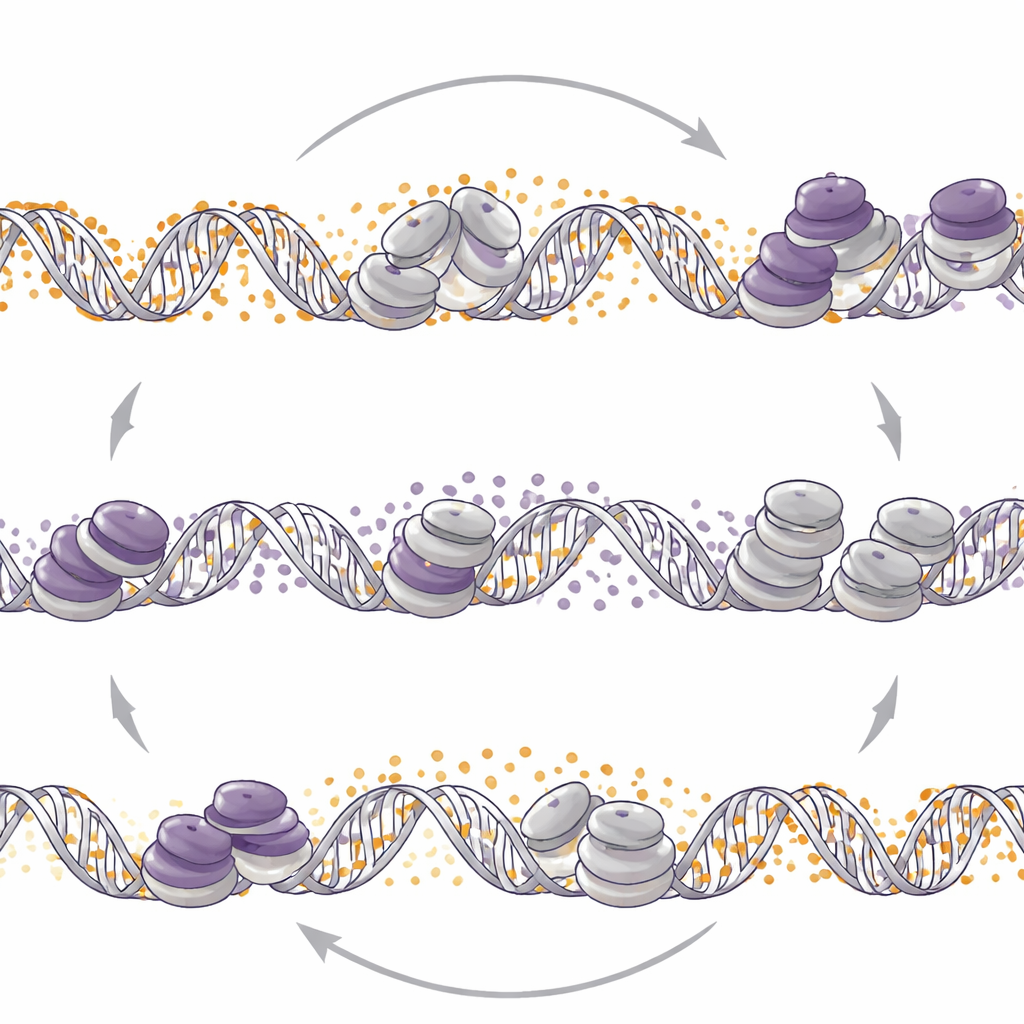
翻转另一只开关会如何重塑控制
科学家随后探询反向是否同样成立:改变 DNA 甲基化是否会重新定位 EZH2 标记?当他们在神经内分泌模型中删除 DNMT1 或使用降低 DNA 甲基化的药物地西他滨时,观察到 H3K27me3 在全基因组范围内的广泛再分布。在这些肿瘤中,降低 DNA 甲基化导致某些待命启动子处 H3K27me3 增加、激活性组蛋白标记丧失以及神经内分泌基因活性下降。相反,在一株前列腺腺癌细胞系中,DNMT1 的丧失在相似的待命区域导致 H3K27me3 减少并且激活性标记增加,从而释放出神经内分泌相关基因。因此,同样的分子推动——削弱 DNMT1——可能在不同肿瘤语境下要么抑制要么点燃神经内分泌程序。
这对未来治疗意味着什么
这些实验共同揭示,DNA 甲基化与 EZH2 驱动的组蛋白标记像两道协调的刹车,能够互相替代以保持关键基因沉默或处于待命状态,帮助前列腺肿瘤切换身份并抗拒治疗。单独干扰某一系统常会触发另一系统的补偿性变化,这可能限制单药靶向 EZH2 或 DNA 甲基化的持久疗效。研究提示,考虑到这种分子拉锯的精心设计策略——可能包括两类表观遗传药物的联合或时序使用——未来有望更好地预防或治疗最具侵袭性、对治疗耐受的前列腺癌形式。
引用: Singh, R., Venkadakrishnan, V.B., Imada, E. et al. Crosstalk between EZH2 and DNA methylation mediates neuroendocrine prostate cancer lineage plasticity. Nat Commun 17, 2992 (2026). https://doi.org/10.1038/s41467-026-69308-0
关键词: 前列腺癌, 神经内分泌肿瘤, 表观遗传学, DNA 甲基化, EZH2