Clear Sky Science · es
Interacción entre EZH2 y la metilación del ADN que media la plasticidad de linaje en el cáncer de próstata neuroendocrino
Por qué importa la identidad de las células cancerosas
Los tumores de próstata no permanecen siempre igual con el tiempo. Algunos dependen inicialmente de las hormonas masculinas y responden a los tratamientos estándar, pero después pueden transformarse en una forma mucho más agresiva llamada cáncer de próstata neuroendocrino. Esta capacidad de cambiar de forma, conocida como plasticidad de linaje, ayuda a los tumores a escapar de la terapia y es una causa importante del fracaso del tratamiento. El estudio resumido aquí explora cómo dos “interruptores” químicos sobre el ADN y su empaquetamiento trabajan conjuntamente para controlar este peligroso cambio de identidad, y cómo bloquear un interruptor puede hacer que el otro compense.
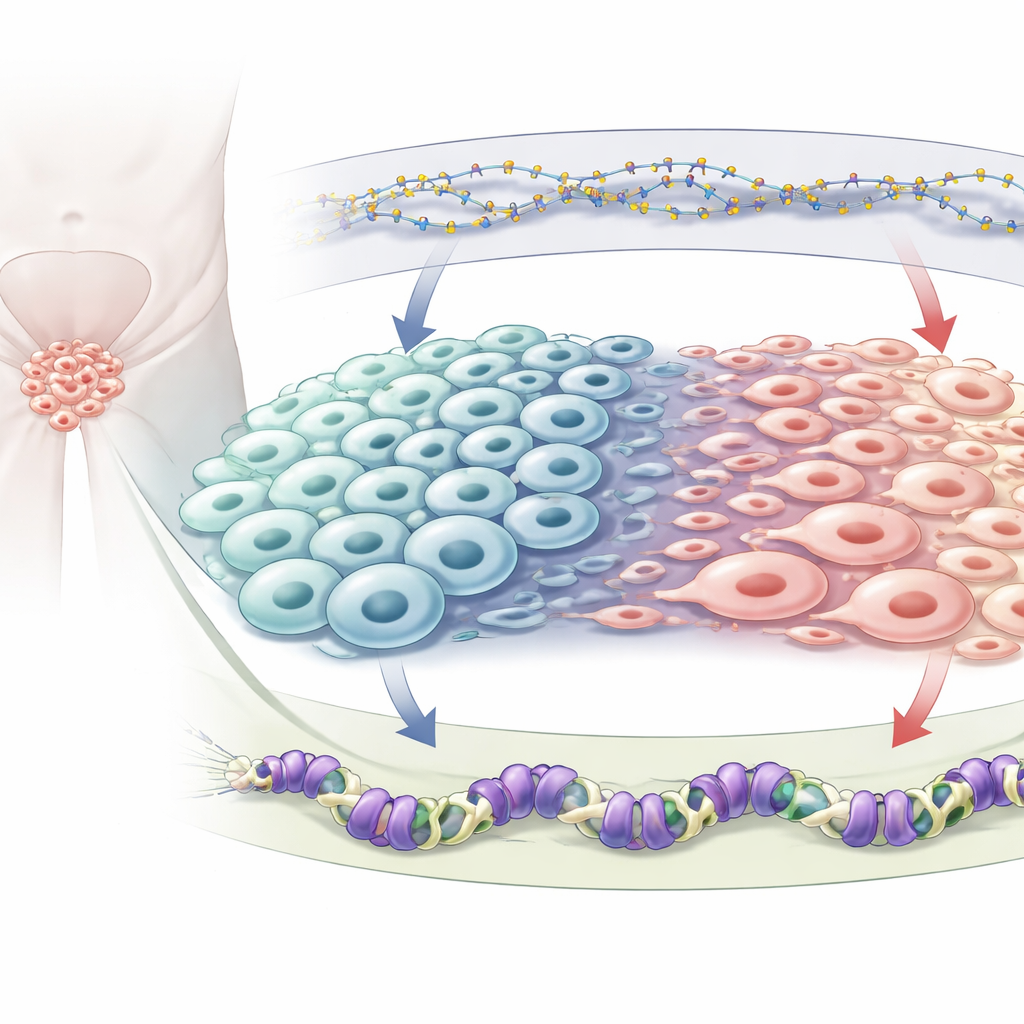
Dos frenos químicos en el genoma
Cada célula porta los mismos genes, pero las etiquetas químicas deciden cuáles están activados o desactivados. Los autores se centran en dos tipos de marcas represoras. Una es la metilación del ADN, en la que pequeños grupos químicos se añaden directamente al ADN y por lo general silencian genes cercanos; esto lo mantiene una enzima llamada DNMT1. La otra es una marca llamada H3K27me3 que se sitúa en las proteínas que envuelven el ADN y la coloca una proteína denominada EZH2, parte del complejo represor polycomb 2. Se sabe que ambos sistemas cambian en el cáncer de próstata, especialmente cuando los tumores se vuelven neuroendocrinos, pero no se había mapeado claramente cómo se influyen entre sí y dirigen en conjunto la identidad celular.
Patrones que señalan tumores de próstata agresivos
Usando ratones genéticamente modificados, muestras tumorales de pacientes y minitumores cultivados en el laboratorio, los investigadores compararon el adenocarcinoma prostático resistente a la castración típico con el cáncer de próstata neuroendocrino. Encontraron cambios consistentes en la metilación del ADN entre los dos estados: cientos de regiones del genoma perdieron metilación, mientras que otras la ganaron. De forma llamativa, las regiones que se desmetilaron en tumores neuroendocrinos a menudo acumularon más de la marca H3K27me3 asociada a EZH2, aunque normalmente se piensa que estos dos sistemas represores se evitan entre sí. Muchas de estas regiones estaban cerca de genes implicados en rasgos neuronales y en los llamados promotores bivalentes, que mantienen genes del desarrollo en un estado listo para activarse o silenciarse rápidamente.
Qué ocurre cuando se libera uno de los frenos
Para sondear causa y efecto, el equipo desactivó EZH2 en modelos de ratón propensos a evolucionar hacia tumores neuroendocrinos y, por separado, trató organoides derivados de pacientes con un fármaco inhibidor de EZH2. En ambos escenarios, el paisaje global de metilación del ADN se reconfiguró extensamente. Regiones que antes eran diana de EZH2 a menudo se volvieron más metiladas, mientras que otros tramos perdieron metilación y activaron genes vinculados a la diferenciación neural y a firmas conocidas neuroendocrinas. En otras palabras, eliminar el freno basado en H3K27me3 permitió que el sistema de metilación del ADN entrara y mantuviera silenciosos muchos de los mismos genes, mientras aflojaba el control en otros sitios que refuerzan el estado neuroendocrino.
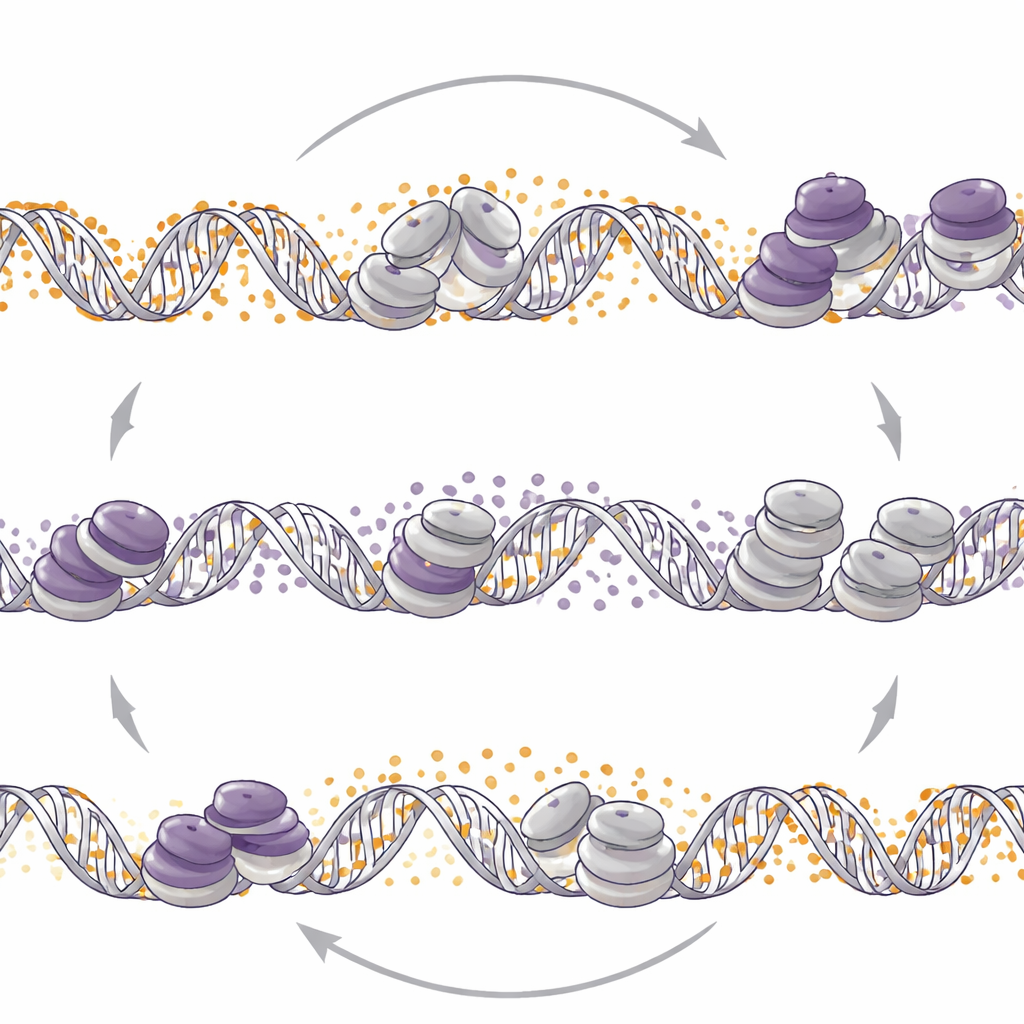
Al invertir el otro interruptor se remodela el control
Los científicos se preguntaron entonces si lo inverso también era cierto: ¿alterar la metilación del ADN reposiciona las marcas de EZH2? Cuando eliminaron DNMT1 o usaron el fármaco que reduce la metilación del ADN decitabina en modelos neuroendocrinos, observaron una amplia redistribución de H3K27me3 a lo largo del genoma. En estos tumores, reducir la metilación del ADN condujo a más H3K27me3 en ciertos promotores en estado de preparación, pérdida de una marca histona activadora y disminución de la actividad de genes neuroendocrinos. En contraste, en una línea celular de adenocarcinoma prostático, la pérdida de DNMT1 disminuyó H3K27me3 en regiones similares en estado de preparación e incrementó la marca activadora, liberando genes relacionados con lo neuroendocrino. Así, el mismo empujón molecular —debilitar DNMT1— puede tanto atenuar como encender programas neuroendocrinos según el contexto tumoral.
Qué significa esto para futuros tratamientos
En conjunto, estos experimentos revelan que la metilación del ADN y las marcas histonas impulsadas por EZH2 se comportan como dos frenos coordinados que pueden intercambiarse para mantener genes críticos silenciados o en estado de preparación, ayudando a los tumores prostáticos a cambiar de identidad y resistir la terapia. Interferir con un sistema por sí solo a menudo desencadena cambios compensatorios en el otro, lo que puede limitar el beneficio duradero de fármacos que apuntan solo a EZH2 o a la metilación del ADN. El trabajo sugiere que estrategias cuidadosamente diseñadas que tengan en cuenta esta pugna molecular —posiblemente incluyendo combinaciones o el uso temporizado de ambos tipos de fármacos epigenéticos— podrían algún día ofrecer formas mejores de prevenir o tratar las formas más agresivas y resistentes a la terapia del cáncer de próstata.
Cita: Singh, R., Venkadakrishnan, V.B., Imada, E. et al. Crosstalk between EZH2 and DNA methylation mediates neuroendocrine prostate cancer lineage plasticity. Nat Commun 17, 2992 (2026). https://doi.org/10.1038/s41467-026-69308-0
Palabras clave: cáncer de próstata, tumores neuroendocrinos, epigenética, metilación del ADN, EZH2