Clear Sky Science · tr
EZH2 ile DNA metilasyonu arasındaki karşılıklı etkileşim nöroendokrin prostat kanseri soy hattı plastisitesini düzenliyor
Neden kanser hücresi kimliği önemlidir
Prostat tümörleri zaman içinde aynı kalmayabilir. Bazıları başlangıçta erkek hormonlarına bağımlı olup standart tedavilere yanıt verirken, daha sonra nöroendokrin prostat kanseri olarak adlandırılan çok daha agresif bir forma dönüşebilir. Soy hattı plastisitesi olarak bilinen bu şekil değiştirme yeteneği, tümörlerin tedaviden kaçmasına yardımcı olur ve tedavi başarısızlıklarının başlıca nedenlerinden biridir. Burada özetlenen çalışma, DNA ve onun paketlenmesindeki iki kimyasal “kapatma anahtarının” bu tehlikeli kimlik değişimini birlikte nasıl kontrol ettiğini ve bir anahtarın engellenmesinin diğerinin telafiye nasıl yol açtığını araştırıyor.
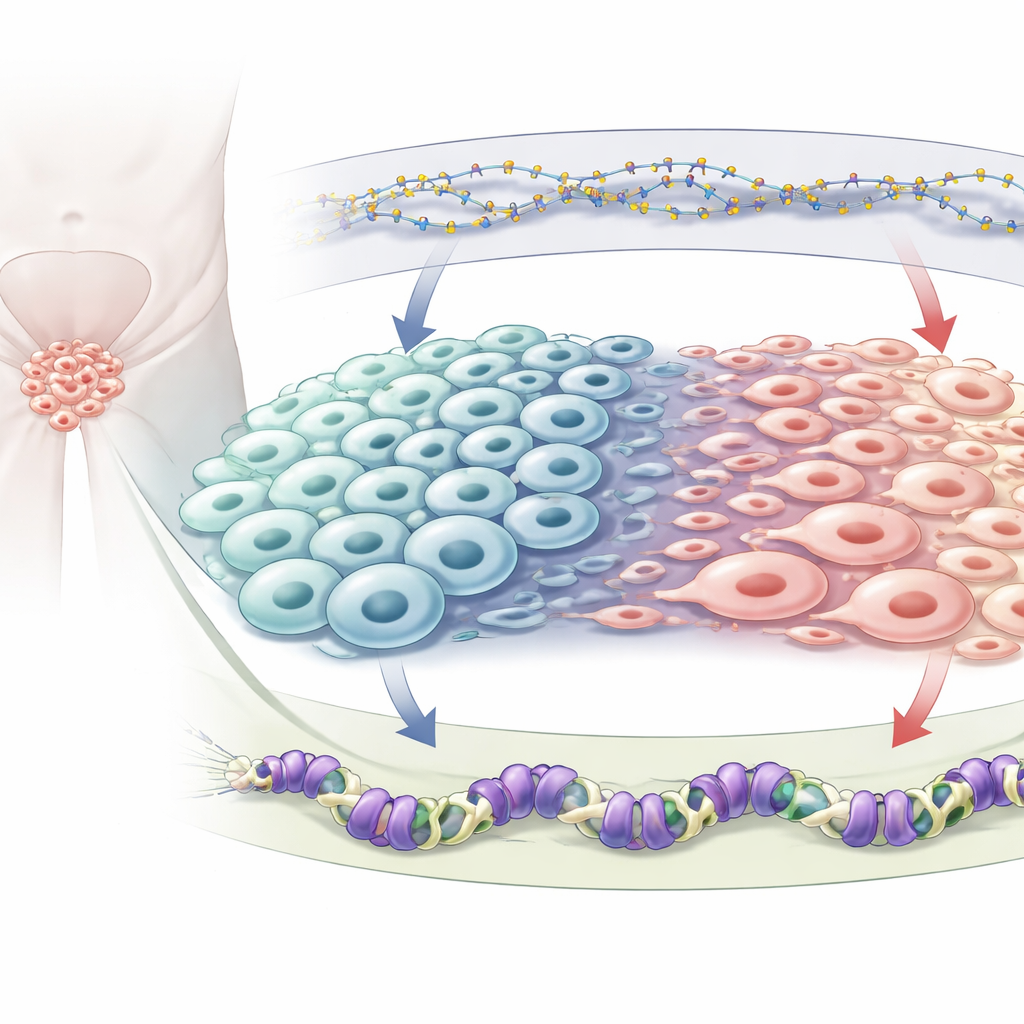
Genom üzerindeki iki kimyasal fren
Her hücre aynı genleri taşır, ancak kimyasal etiketler hangilerinin açık veya kapalı olacağına karar verir. Yazarlar iki tür baskılayıcı etikete odaklanır. Birincisi DNA metilasyonu olup, küçük kimyasal grupların doğrudan DNA’ya eklenmesiyle yakındaki genleri genellikle susturur; bu durum DNMT1 adlı bir enzim tarafından sürdürülür. Diğeri ise H3K27me3 adı verilen ve DNA’yı saran proteinlerin üzerine konulan bir işaret olup, polikomb baskılayıcı kompleks 2’nin bir üyesi olan EZH2 adlı protein tarafından yerleştirilir. Her iki sistemin de prostat kanserinde, özellikle tümörler nöroendokrin hale geldiğinde değiştiği bilinmekle birlikte, birbirlerini nasıl etkiledikleri ve birlikte hücre kimliğini nasıl yönlendirdikleri net bir biçimde haritalanmamıştı.
Agresif prostat tümörlerini işaretleyen desenler
Genetik olarak değiştirilmiş fareler, hasta tümör örnekleri ve laboratuvarda büyütülen mini tümörler kullanarak araştırmacılar tipik kastrasyon‑dirençli prostat adenokarsinomasını nöroendokrin prostat kanseriyle karşılaştırdılar. İki durum arasında DNA metilasyonunda tutarlı kaymaları buldular: yüzlerce genomik bölge metilasyon kaybederken, diğerleri metilasyon kazandı. Dikkat çekici biçimde, nöroendokrin tümörlerde daha az metile olmuş bölgeler sıklıkla EZH2 ile ilişkilendirilen H3K27me3 işaretini daha çok topladı; oysa bu iki baskılayıcı sistem genellikle birbirinden kaçınır gibi düşünülür. Bu bölgelerin birçoğu sinir‑benzeri özelliklerle ilişkili genlerin yakınında ve gelişim genlerini hızlıca açıp kapalı tutmaya hazır halde tutan sözde bivalent promotörlerde yer alıyordu.
Bir fren serbest bırakıldığında ne olur
Neden‑sonuç ilişkisini incelemek için ekip, nöroendokrin tümörlere evrilmeye eğilimli fare modellerinde EZH2’yi devre dışı bıraktı ve ayrı olarak hasta kaynaklı organoidleri EZH2 engelleyici bir ilaçla tedavi etti. Her iki ortamda da küresel DNA metilasyon manzarası büyük ölçüde yeniden düzenlendi. Önceden EZH2 tarafından hedeflenen bölgeler genellikle daha fazla metile olurken, diğer bölgeler metilasyon kaybedip sinir farklılaşması ve bilinen nöroendokrin imzalarla ilişkili genleri açtı. Başka bir deyişle, H3K27me3 temelli freni kaldırmak DNA metilasyon sisteminin devreye girip birçok aynı geni susturmaya devam etmesine izin verirken, aynı zamanda nöroendokrin durumu pekiştiren diğer bölgelerde kontrolü gevşetiyordu.
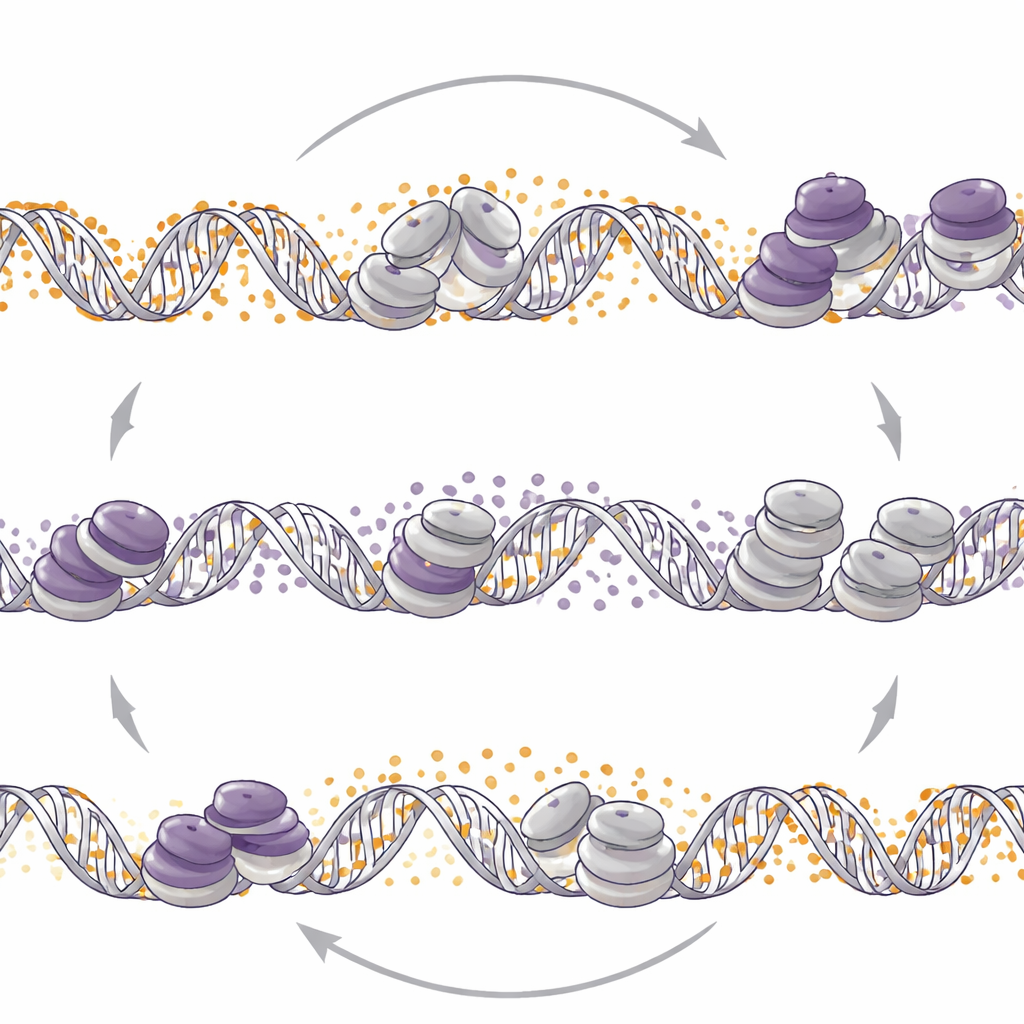
Diğer anahtarı çevirmek kontrolü yeniden şekillendiriyor
Bilim insanları daha sonra tersinin de doğru olup olmadığını sordular: DNA metilasyonunu değiştirmek EZH2 işaretlerini yeniden konumlandırır mı? DNMT1’i sildiklerinde veya nöroendokrin modellerde DNA metilasyonunu azaltan decitabin ilacını kullandıklarında, tüm genomda H3K27me3’ün geniş çapta yeniden dağılımını gözlediler. Bu tümörlerde DNA metilasyonunu azaltmak belirli hazır promotörlerde daha fazla H3K27me3’ye, etkinleştirici bir histon işaretinin kaybına ve nöroendokrin genlerin aktivitesinin azalmasına yol açtı. Buna karşılık, bir prostat adenokarsinoma hücre hattında DNMT1 kaybı benzer hazır bölgelerde H3K27me3’ü azalttı ve etkinleştirici işareti artırarak nöroendokrin‑ilişkili genleri serbest bıraktı. Böylece aynı moleküler müdahale—DNMT1’i zayıflatmak—tümör bağlamına bağlı olarak ya nöroendokrin programları bastırabilir ya da ateşleyebilir.
Gelecek tedaviler için bunun anlamı
Birlikte ele alındığında, bu deneyler DNA metilasyonu ile EZH2 kaynaklı histon işaretlemesinin, kritik genleri susturmak veya hazır tutmak için yer değiştirebilen, koordineli iki fren gibi davrandığını; bunun da prostat tümörlerinin kimlik değiştirmesine ve tedaviye direnmesine yardımcı olduğunu ortaya koyuyor. Tek bir sistemi hedeflemek genellikle diğerinde telafi edici değişiklikleri tetikleyebilir; bu da yalnız başına EZH2’yi veya DNA metilasyonunu hedefleyen ilaçların kalıcı faydasını sınırlayabilir. Çalışma, bu moleküler çekişmeyi göz önünde bulunduran—muhtemelen her iki tip epigenetik ilacın kombinasyonu veya zamanlanmış kullanımı gibi—özenle tasarlanmış stratejilerin bir gün en agresif, tedaviye dirençli prostat kanseri formlarını önleme veya tedavi etmede daha iyi yollar sunabileceğini öne sürüyor.
Atıf: Singh, R., Venkadakrishnan, V.B., Imada, E. et al. Crosstalk between EZH2 and DNA methylation mediates neuroendocrine prostate cancer lineage plasticity. Nat Commun 17, 2992 (2026). https://doi.org/10.1038/s41467-026-69308-0
Anahtar kelimeler: prostat kanseri, nöroendokrin tümörler, epigenetik, DNA metilasyonu, EZH2