Clear Sky Science · it
Interazione tra EZH2 e metilazione del DNA media la plasticità di linea nel carcinoma prostatico neuroendocrino
Perché l’identità delle cellule tumorali conta
I tumori prostatici non rimangono sempre uguali nel tempo. Alcuni dipendono inizialmente dagli ormoni maschili e rispondono ai trattamenti standard, ma poi possono trasformarsi in una forma molto più aggressiva chiamata carcinoma prostatico neuroendocrino. Questa capacità di cambiare aspetto, nota come plasticità di linea, aiuta i tumori a sfuggire alla terapia ed è una delle principali cause del fallimento terapeutico. Lo studio riassunto qui esplora come due "freni" chimici sul DNA e sul suo impacchettamento lavorino insieme per controllare questo pericoloso cambiamento di identità e come il blocco di un freno possa indurre l’altro a compensare.
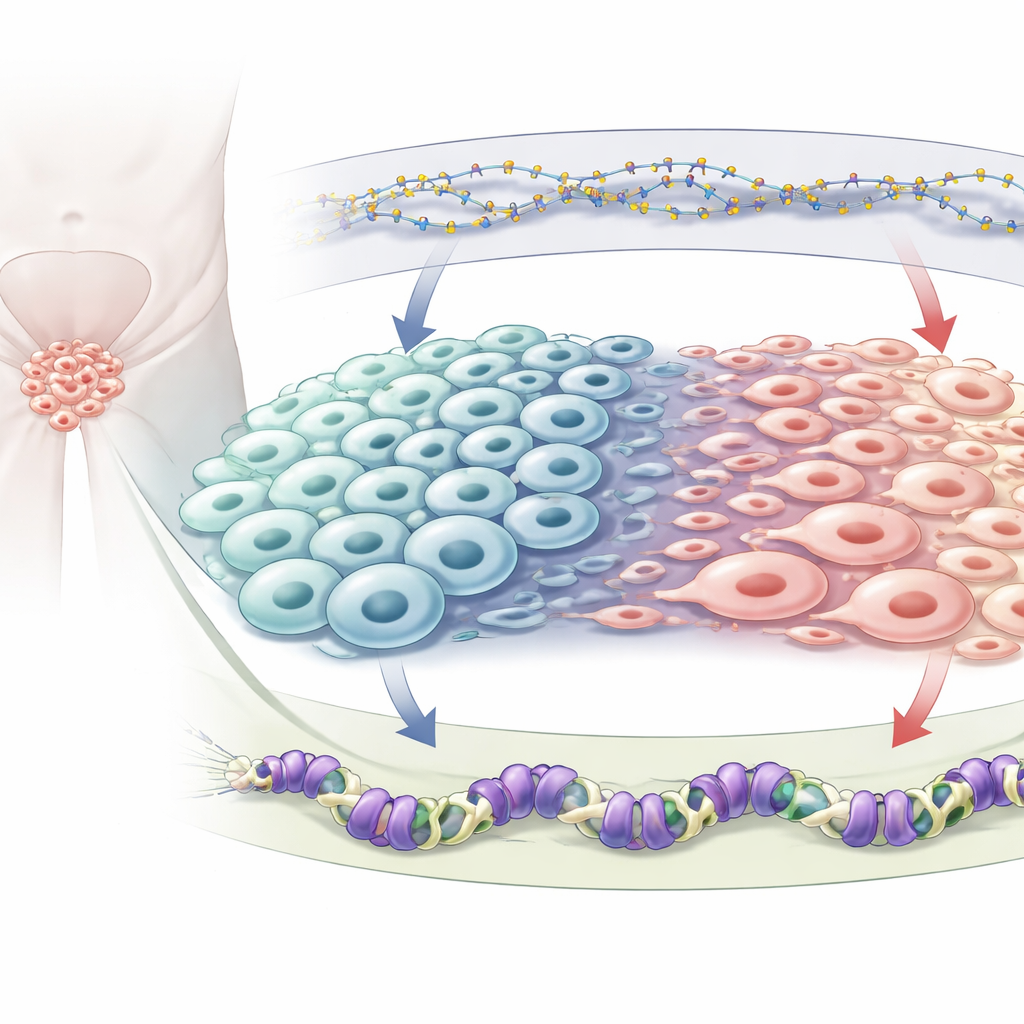
Due freni chimici sul genoma
Ogni cellula porta gli stessi geni, ma i marcatori chimici decidono quali sono attivi o spenti. Gli autori si concentrano su due tipi di marcatori repressivi. Uno è la metilazione del DNA, in cui piccoli gruppi chimici vengono aggiunti direttamente al DNA e di solito silenziano i geni vicini; questo viene mantenuto da un enzima chiamato DNMT1. L’altro è un marcatore chiamato H3K27me3 che si trova sulle proteine attorno al DNA ed è posto lì da una proteina chiamata EZH2, parte del complesso repressivo Polycomb 2. Entrambi i sistemi sono noti per cambiare nel cancro prostatico, specialmente quando i tumori diventano neuroendocrini, ma non era chiaro come influenzassero l’un l’altro e insieme guidassero l’identità cellulare.
Modelli che contrassegnano i tumori prostatici aggressivi
Usando topi geneticamente modificati, campioni tumorali di pazienti e mini-tumori coltivati in laboratorio, i ricercatori hanno confrontato l’adenocarcinoma prostatico resistente alla castrazione tipico con il carcinoma prostatico neuroendocrino. Hanno riscontrato cambiamenti coerenti nella metilazione del DNA tra i due stati: centinaia di regioni genomiche hanno perso metilazione, mentre altre l’hanno guadagnata. In modo sorprendente, le regioni che hanno perso metilazione nei tumori neuroendocrini spesso accumulavano più del marcatore legato a EZH2, H3K27me3, nonostante questi due sistemi repressivi siano generalmente ritenuti reciprocamente esclusivi. Molte di queste regioni si trovavano vicino a geni coinvolti in caratteristiche neuronali e in cosiddetti promotori bivalenti, che mantengono i geni dello sviluppo pronti per essere rapidamente attivati o silenziati.
Cosa succede quando un freno viene rilasciato
Per indagare causalità, il gruppo ha disabilitato EZH2 in modelli murini predisposti a evolvere in tumori neuroendocrini e, separatamente, ha trattato organoidi derivati da pazienti con un farmaco inibitore di EZH2. In entrambi i contesti, il paesaggio globale della metilazione del DNA è stato ampiamente riorganizzato. Le regioni precedentemente bersaglio di EZH2 spesso diventavano più metilate, mentre altri tratti perdevano metilazione e attivavano geni legati alla differenziazione neurale e a noti segnali neuroendocrini. In altre parole, rimuovere il freno basato su H3K27me3 ha permesso al sistema della metilazione del DNA di avanzare e mantenere silenziati molti degli stessi geni, pur allentando contemporaneamente il controllo in altri siti che rafforzano lo stato neuroendocrino.
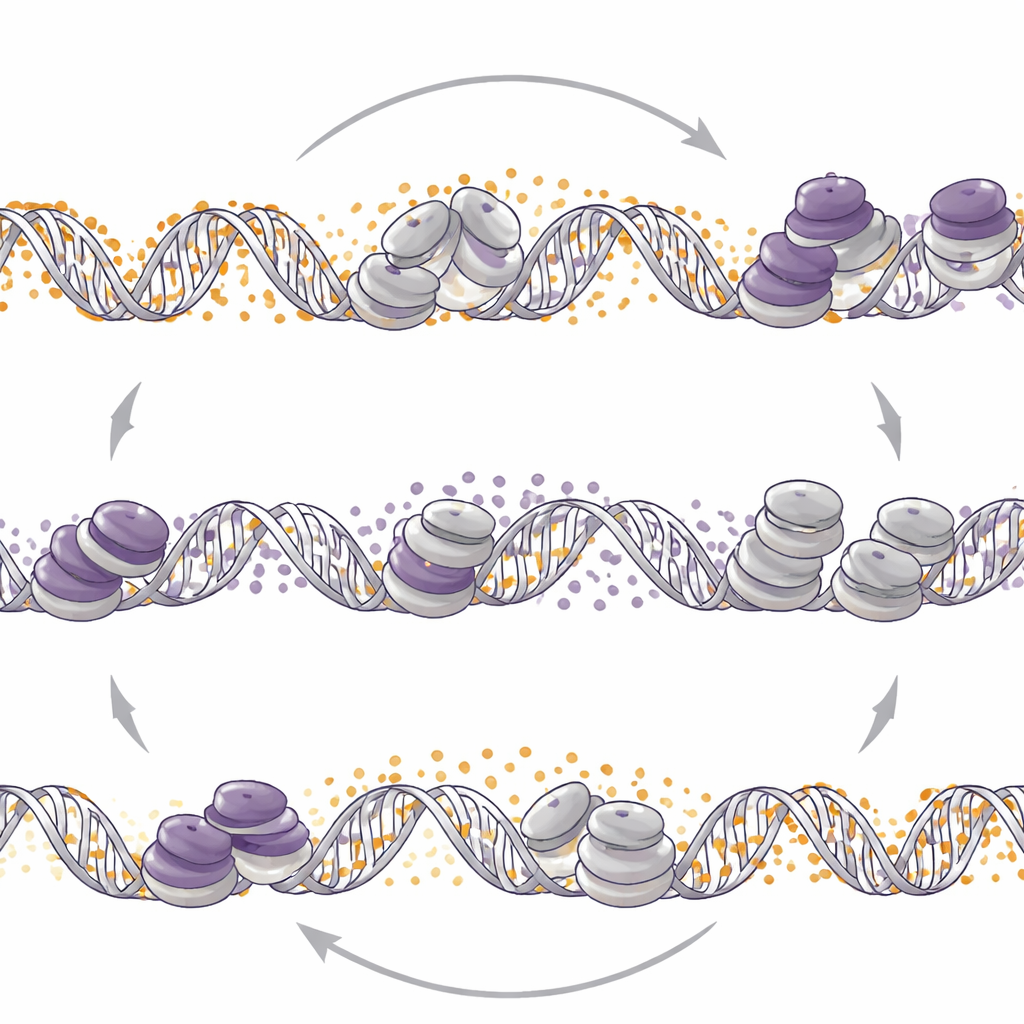
Invertire l’altro interruttore rimodella il controllo
Gli scienziati hanno quindi chiesto se valesse anche il contrario: alterare la metilazione del DNA riposiziona i marcatori di EZH2? Quando hanno eliminato DNMT1 o hanno usato il farmaco demetilante decitabina in modelli neuroendocrini, hanno osservato un’ampia ridistribuzione di H3K27me3 nel genoma. In questi tumori, ridurre la metilazione del DNA conduceva a più H3K27me3 su certi promotori in stato di prontezza, perdita di un marcatore istonico attivante e ridotta attività dei geni neuroendocrini. Al contrario, in una linea cellulare di adenocarcinoma prostatico, la perdita di DNMT1 diminuiva H3K27me3 in regioni bivalenti simili e aumentava il marcatore attivante, scatenando i geni correlati al fenotipo neuroendocrino. Così lo stesso spunto molecolare — indebolire DNMT1 — può sia attenuare sia accendere i programmi neuroendocrini a seconda del contesto tumorale.
Cosa significa per i trattamenti futuri
Complessivamente, questi esperimenti rivelano che la metilazione del DNA e la marcatura istonica guidata da EZH2 si comportano come due freni coordinati che possono alternarsi per mantenere critici geni silenziati o in stato di prontezza, aiutando i tumori prostatici a cambiare identità e resistere alla terapia. Interferire con un solo sistema spesso innesca cambiamenti compensatori nell’altro, il che può limitare il beneficio duraturo di farmaci che prendono di mira solo EZH2 o la metilazione del DNA. Il lavoro suggerisce che strategie attentamente progettate che tengano conto di questa lotta molecolare — potenzialmente includendo uso combinato o temporizzato di entrambi i tipi di farmaci epigenetici — potrebbero un giorno offrire modi migliori per prevenire o trattare le forme più aggressive e resistenti del cancro alla prostata.
Citazione: Singh, R., Venkadakrishnan, V.B., Imada, E. et al. Crosstalk between EZH2 and DNA methylation mediates neuroendocrine prostate cancer lineage plasticity. Nat Commun 17, 2992 (2026). https://doi.org/10.1038/s41467-026-69308-0
Parole chiave: cancro alla prostata, tumori neuroendocrini, epigenetica, metilazione del DNA, EZH2