Clear Sky Science · ar
التفاعل بين EZH2 والميثلة على الحمض النووي يوسّع مرونة سلالة سرطان البروستاتا العصبي الصماوي
لماذا تهم هوية الخلية السرطانية
الأورام البروستاتية لا تبقى دائماً على حالها مع مرور الزمن. بعضها يعتمد في البداية على الهرمونات الذكرية ويستجيب للعلاجات القياسية، لكنه يتحول لاحقاً إلى شكل أكثر عدوانية يُعرف بسرطان البروستاتا العصبي الصماوي. هذه القدرة على تغيير الهوية، المسماة بالمرونة النسيجية، تساعد الأورام على الهروب من العلاج وتُعد سبباً رئيسياً لفشل العلاج. تدرس الدراسة الموجزة هنا كيف يتعاون اثنان من "مفاتيح الإيقاف" الكيميائية على الحمض النووي وتغليفه للتحكم في هذا التغير الخطر في الهوية، وكيف أن حجب أحد المفتاحين قد يدفع الآخر للتعويض.
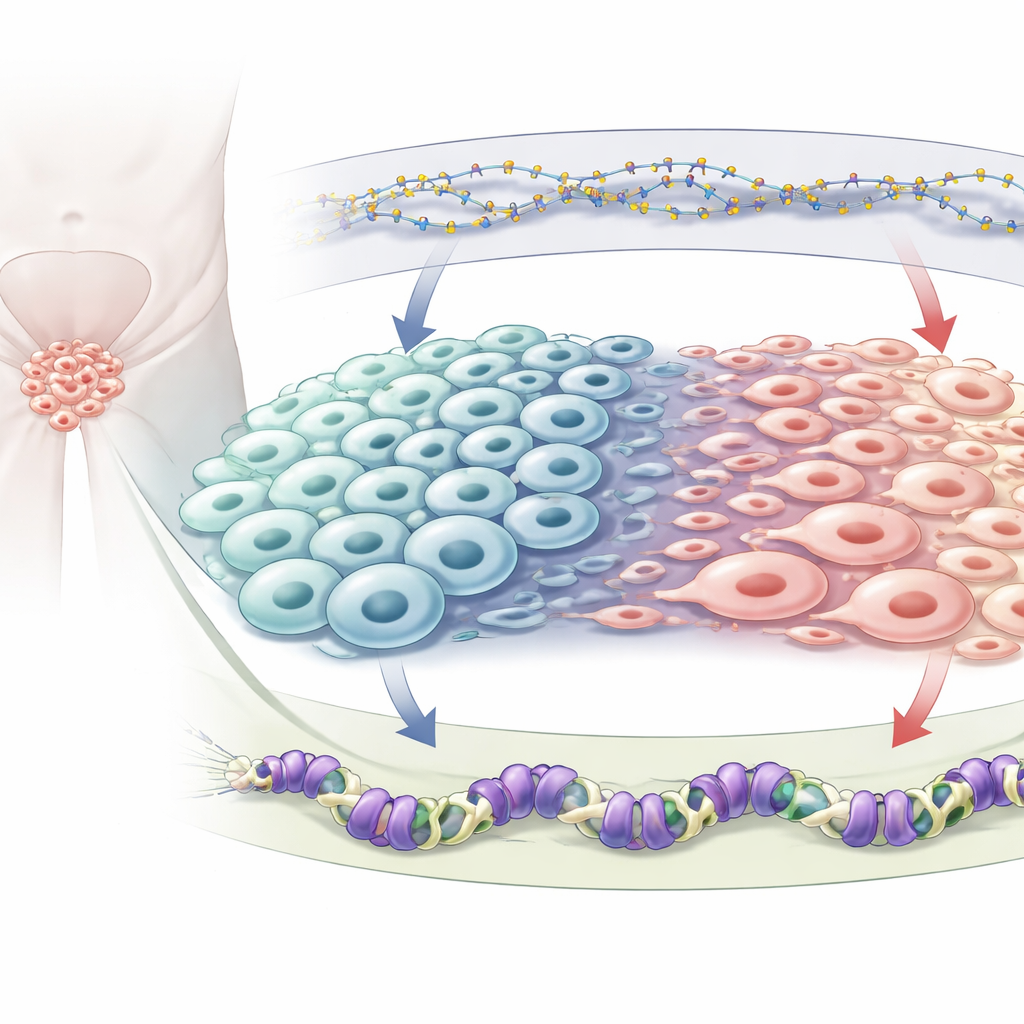
فرامل كيميائية مزدوجة على الجينوم
كل خلية تحمل نفس الجينات، لكن العلامات الكيميائية تقرر أيها يعمل أو لا يعمل. يركز الباحثون على نوعين من العلامات الكابحة. أحدهما هو ميثلة الحمض النووي، حيث تُضاف مجموعات كيميائية صغيرة مباشرة على الحمض النووي وعادة ما تُخمد الجينات القريبة؛ ويحافظ عليها إنزيم يُدعى DNMT1. الآخر علامة تُسمى H3K27me3 تجلس على بروتينات التفاف الحمض النووي وتوضع هناك بواسطة بروتين اسمه EZH2، جزء من مركب البوليكوم الكابح 2. كلا النظامين معروفان بتغيّرهما في سرطان البروستاتا، خصوصاً عندما تصبح الأورام عصبية صماوية، لكن كيفية تأثير كل واحد منهما على الآخر وكيف يشتركان في توجيه هوية الخلية لم تكن واضحة جيداً.
أنماط تميّز الأورام البروستاتية العدوانية
باستخدام فئران معدلة وراثياً وعينات أورام مرضى وأورام مصغرة مزروعة في المختبر، قارن الباحثون سرطان غدي البروستاتا المقاوم للاستئصال الهرموني المعتاد مع سرطان البروستاتا العصبي الصماوي. وجدوا تحولات متسقة في ميثلة الحمض النووي بين الحالتين: فقدت مئات المناطق الجينومية ميثلة بينما اكتسبت مناطق أخرى ميثلة. اللافت أن المناطق التي فقدت الميثلة في الأورام العصبية الصماوية غالباً ما تراكمت بها علامة H3K27me3 المرتبطة بـ EZH2، رغم أن هذين النظامين الكابحين يُعتقدان عادة أنهما يتجنّبان بعضهما البعض. وكان العديد من هذه المناطق بالقرب من جينات مشاركة في صفات شبيهة بالعصبونات وفي ما يُسمى بالمروج المتأرجحة (bivalent promoters) التي تُبقي جينات التطور جاهزة للتشغيل أو الإيقاف بسرعة.
ماذا يحدث عند تحرير إحدى الفرامل
لفحص السببية، عطّل الفريق EZH2 في نماذج فأرية معرضة للتطور إلى أورام عصبية صماوية، وبشكل منفصل عالجوا أوريجاينو مشتق من المرضى بعقار يثبط EZH2. في كلا الإعدادين، أعيد تشكيل مشهد ميثلة الحمض النووي على نطاق واسع. المناطق التي كانت مُستهدفة سابقاً بواسطة EZH2 أصبحت غالباً أكثر ميثلة، في حين فقدت مناطق أخرى الميثلة وتحولت لتشغيل جينات مرتبطة بالتمايز العصبي والتواقيع المعروفة للأورام العصبية الصماوية. بعبارة أخرى، سمح رفع فرملة H3K27me3 لنظام ميثلة الحمض النووي بالتدخل وإبقاء العديد من نفس الجينات مكتومة، بينما في الوقت نفسه خفف السيطرة عند مواقع أخرى تعزز الحالة العصبية الصماوية.
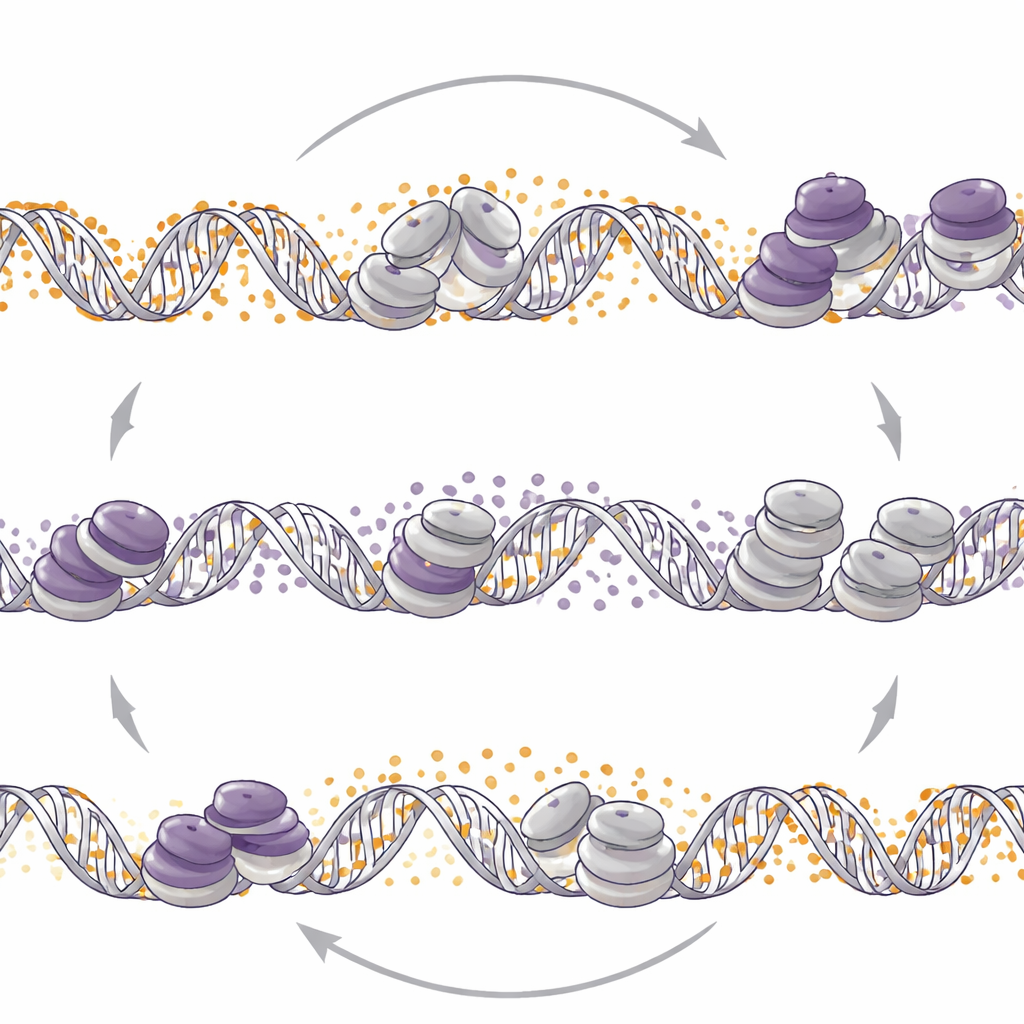
قلب المفتاح الآخر يعيد تشكيل السيطرة
سأل العلماء بعد ذلك إن كان العكس صحيحاً أيضاً: هل يؤدي تعديل ميثلة الحمض النووي إلى إعادة تموضع علامات EZH2؟ عندما حذفوا DNMT1 أو استخدموا الدواء المقلل لميثلة الحمض النووي ديسيتابين في نماذج عصبية صماوية، لاحظوا إعادة توزيع واسعة لـ H3K27me3 عبر الجينوم. في هذه الأورام، أدى تقليل ميثلة الحمض النووي إلى زيادة H3K27me3 عند بعض المروج المتأهبة، وفقدان علامة هستون منشّطة، وانخفاض نشاط جينات عصبية صماوية. بالمقابل، في خط خلوي لسرطان غدي البروستاتا، أدى فقدان DNMT1 إلى خفض H3K27me3 في مناطق متأهبة مماثلة وزيادة العلامة المنشطة، مما أطلق جينات مرتبطة بالصفات العصبية الصماوية. وهكذا، يمكن للدفع الجزيئي ذاته — إضعاف DNMT1 — أن يثبط أو يشعل البرامج العصبية الصماوية اعتماداً على سياق الورم.
ماذا يعني هذا للعلاجات المستقبلية
تكشف هذه التجارب معاً أن ميثلة الحمض النووي ووضعية الهستون المدفوعة بواسطة EZH2 تتصرفان كفرامل منسقة يمكن أن تتبادل الأدوار لإبقاء جينات حاسمة مكتومة أو متأهبة، مما يساعد أورام البروستاتا على تغيير هويتها ومقاومة العلاج. التدخّل في أحد النظامين بمفرده غالباً ما يثير تغيّرات تعويضية في الآخر، ما قد يحد من الفائدة الدائمة للأدوية التي تستهدف EZH2 أو ميثلة الحمض النووي بشكل منفرد. تشير النتائج إلى أن استراتيجيات مصممة بعناية تأخذ بالحسبان هذا الصراع الجزيئي — وربما تشمل الجمع بين أو توقيت استخدام كلا نوعي الأدوية فوق الجينية — قد توفر في المستقبل طرقاً أفضل لمنع أو علاج الأشكال الأكثر عدوانية والمقاومة للعلاج من سرطان البروستاتا.
الاستشهاد: Singh, R., Venkadakrishnan, V.B., Imada, E. et al. Crosstalk between EZH2 and DNA methylation mediates neuroendocrine prostate cancer lineage plasticity. Nat Commun 17, 2992 (2026). https://doi.org/10.1038/s41467-026-69308-0
الكلمات المفتاحية: سرطان البروستاتا, الأورام العصبيّة الصماوية, علم التخلق فوق الجيني, ميثلة الحمض النووي, EZH2