Clear Sky Science · ru
Взаимодействие между EZH2 и метилированием ДНК опосредует пластичность линии при нейроэндокринном раке простаты
Почему имеет значение идентичность раковых клеток
Опухоли предстательной железы не всегда остаются неизменными со временем. Некоторые из них первоначально зависят от андрогенов и отвечают на стандартные методы лечения, но позже переходят в куда более агрессивную форму, называемую нейроэндокринным раком простаты. Эта способность к смене облика, известная как пластичность линии, помогает опухолям уклоняться от терапии и является основной причиной неэффективности лечения. В изложенном здесь исследовании изучается, как два химических «тормоза» на ДНК и её упаковке действуют совместно, контролируя это опасное изменение идентичности, и как блокирование одного тормоза может привести к компенсации со стороны другого.
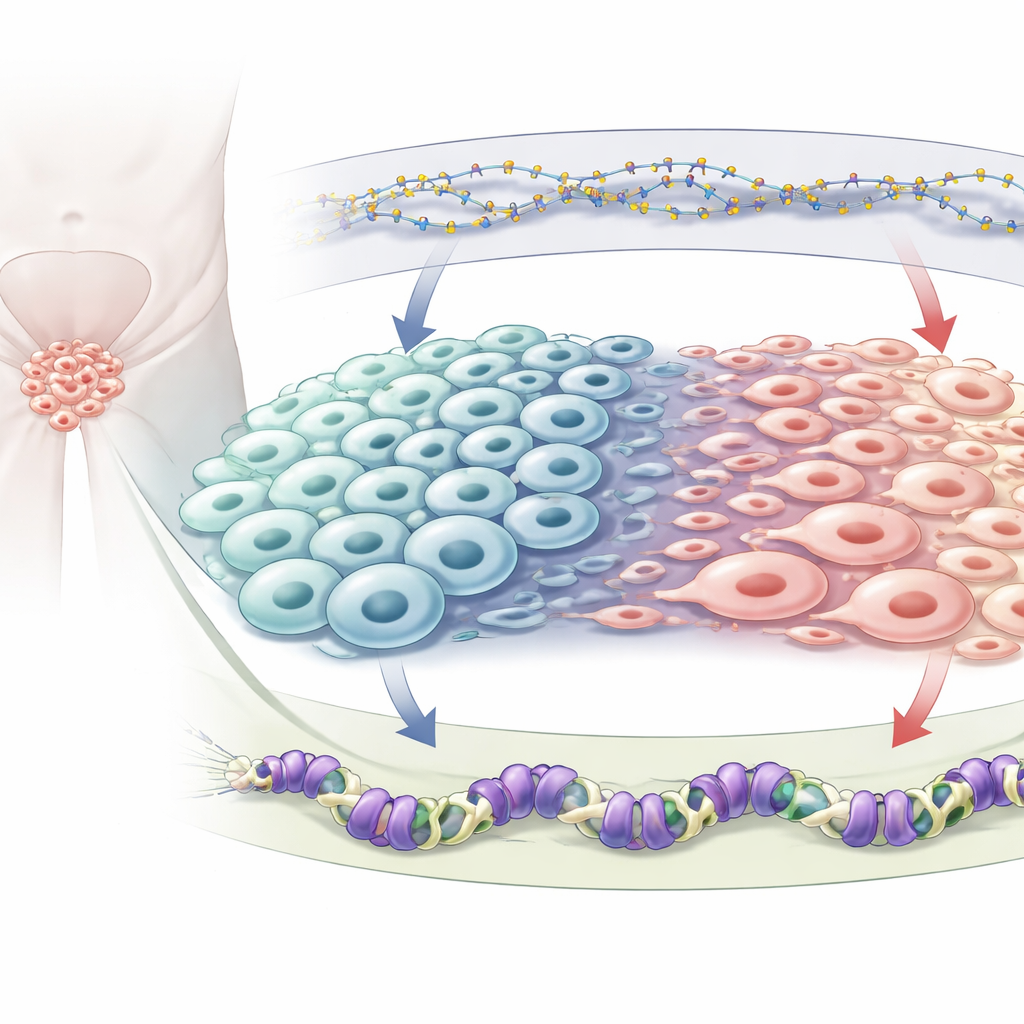
Два химических тормоза генома
Каждая клетка несёт одинаковый набор генов, но химические метки определяют, какие из них включены или выключены. Авторы сосредоточились на двух типах репрессивных меток. Одна — метилирование ДНК, при котором к самой ДНК присоединяются небольшие химические группы и обычно подавляют соседние гены; за это отвечает фермент DNMT1. Другая — метка H3K27me3, находящаяся на белках, вокруг которых обвита ДНК, и наносимая белком EZH2, входящим в состав комплекса polycomb repressive complex 2. Оба механизма известны тем, что меняются при раке простаты, особенно когда опухоли становятся нейроэндокринными, но то, как они взаимно влияют друг на друга и совместно направляют клеточную идентичность, ранее было недостаточно ясно.
Шаблоны, отмечающие агрессивные опухоли простаты
Используя генетически модифицированных мышей, образцы опухолей пациентов и миниатюрные опухоли, выращенные в лаборатории, исследователи сравнили типичную кастрационно‑резистентную аденокарциному простаты с нейроэндокринным раком простаты. Они обнаружили последовательные сдвиги в метилировании ДНК между этими двумя состояниями: сотни регионов генома теряли метилирование, тогда как другие его приобретали. Поразительно, что регионы, которые теряли метилирование в нейроэндокринных опухолях, часто одновременно накапливали метку H3K27me3, связанную с EZH2, хотя эти два репрессивных механизма обычно считаются взаимоисключающими. Многие из этих регионов располагались рядом с генами, вовлечёнными в нервоподобные функции, а также в так называемых бивалентных промоторах, которые держат гены развития в состоянии готовности к быстрому включению или выключению.
Что происходит, когда один тормоз отпускать
Чтобы установить причинно‑следственные связи, команда инактивировала EZH2 в мышиных моделях, склонных к переходу в нейроэндокринные опухоли, и отдельно обрабатывала органоиды, полученные от пациентов, препаратом‑ингибитором EZH2. В обоих случаях глобальный ландшафт метилирования ДНК претерпел крупную перестройку. Регионы, ранее мишенями EZH2, часто становились более метилированными, в то время как другие участки теряли метилирование и активировали гены, связанные с нейронной дифференцировкой и известными нейроэндокринными сигнатурами. Иными словами, удаление тормоза на основе H3K27me3 позволило системе метилирования ДНК вмешаться и сохранить молчание многих тех же генов, одновременно ослабив контроль в других местах, что усиливало нейроэндокринное состояние.
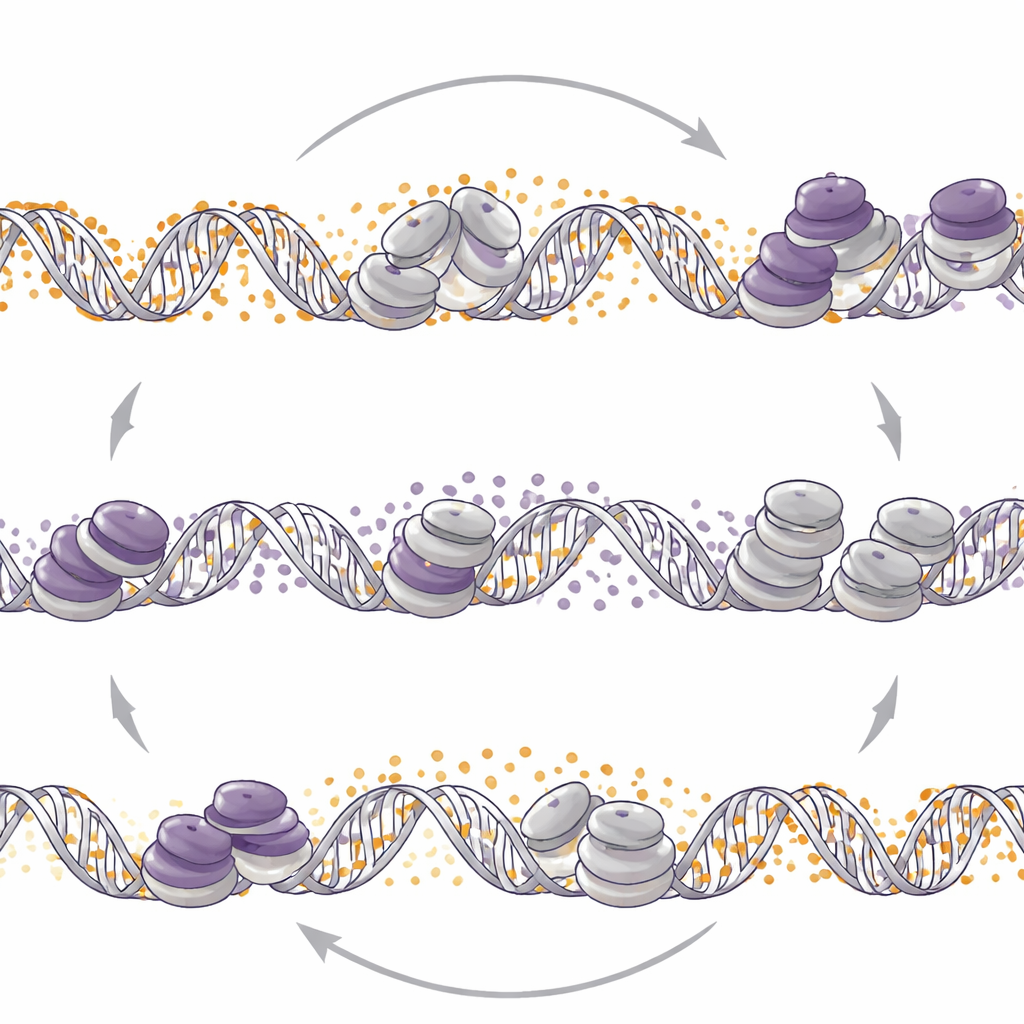
Переключение другого тумблера меняет управление
Учёные затем спросили, верно ли обратное: переставляет ли изменение метилирования ДНК метки EZH2? Когда они удаляли DNMT1 или применяли препарат, снижающий метилирование ДНК — децитабин, — в нейроэндокринных моделях, они наблюдали широкую перераспределённость H3K27me3 по геному. В этих опухолях снижение метилирования ДНК приводило к росту H3K27me3 в определённых подготовленных промоторах, потере активирующей гистоновой метки и снижению активности нейроэндокринных генов. В отличие от этого, в клеточной линии аденокарциномы простаты потеря DNMT1 уменьшала H3K27me3 в аналогичных подготовленных регионах и повышала уровень активирующей метки, что запускало нейроэндокринные программы. Таким образом одно и то же молекулярное воздействие — ослабление DNMT1 — может либо подавлять, либо инициировать нейроэндокринные программы в зависимости от контекста опухоли.
Что это означает для будущих методов лечения
Вместе эти эксперименты показывают, что метилирование ДНК и модификации гистонов под управлением EZH2 действуют как два скоординированных тормоза, которые могут менять местами свои роли, чтобы держать важные гены в молчании или в состоянии готовности, помогая опухолям простаты менять идентичность и сопротивляться терапии. Вмешательство в одну систему само по себе часто вызывает компенсаторные изменения в другой, что может ограничивать длительную пользу от препаратов, нацеленных только на EZH2 или только на метилирование ДНК. Работа предполагает, что тщательно продуманные стратегии, учитывающие эту молекулярную борьбу — возможно, включая комбинированное или временно разнесённое применение обоих типов эпигенетических препаратов — со временем могут дать лучшие способы предотвратить или лечить наиболее агрессивные, резистентные к терапии формы рака простаты.
Цитирование: Singh, R., Venkadakrishnan, V.B., Imada, E. et al. Crosstalk between EZH2 and DNA methylation mediates neuroendocrine prostate cancer lineage plasticity. Nat Commun 17, 2992 (2026). https://doi.org/10.1038/s41467-026-69308-0
Ключевые слова: рак простаты, нейроэндокринные опухоли, эпигенетика, метилирование ДНК, EZH2