Clear Sky Science · pt
Interação entre EZH2 e metilação do DNA media a plasticidade de linhagem no câncer de próstata neuroendócrino
Por que a identidade das células cancerosas importa
Os tumores de próstata nem sempre permanecem iguais ao longo do tempo. Alguns dependem inicialmente de hormônios masculinos e respondem aos tratamentos padrão, mas depois se transformam em uma forma muito mais agressiva chamada câncer de próstata neuroendócrino. Essa capacidade de mudar de forma, conhecida como plasticidade de linhagem, ajuda os tumores a escapar da terapia e é uma das principais causas de falha no tratamento. O estudo resumido aqui explora como dois “freios” químicos no DNA e em seu empacotamento atuam em conjunto para controlar essa mudança perigosa de identidade, e como bloquear um desses freios pode levar o outro a compensar.
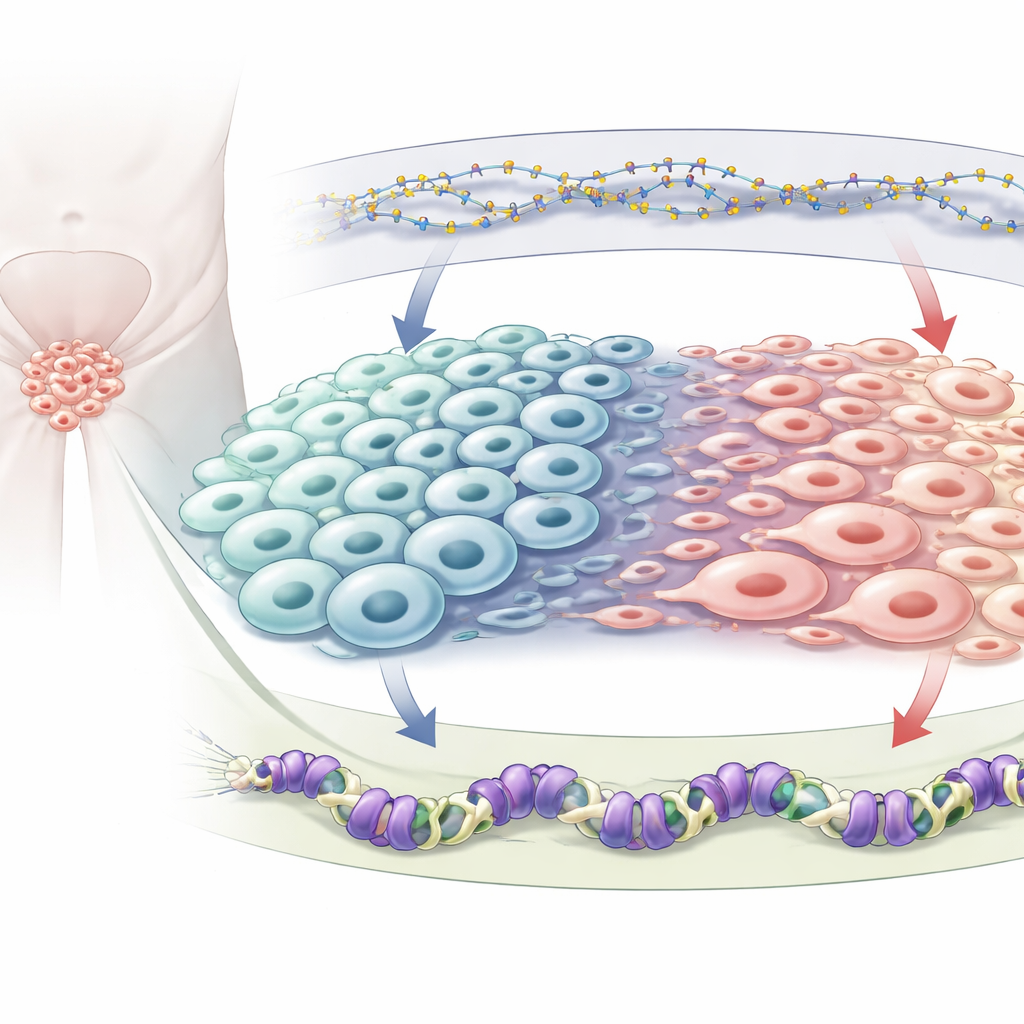
Dois freios químicos no genoma
Cada célula carrega os mesmos genes, mas marcas químicas decidem quais estão ligados ou desligados. Os autores focam em dois tipos de marcas repressivas. Uma é a metilação do DNA, em que pequenos grupos químicos são adicionados diretamente ao DNA e geralmente silenciam genes próximos; isso é mantido por uma enzima chamada DNMT1. A outra é uma marca chamada H3K27me3 que se assenta nas proteínas que enrolam o DNA e é colocada ali por uma proteína chamada EZH2, parte do complexo repressivo polycomb 2. Sabe‑se que ambos os sistemas mudam no câncer de próstata, especialmente quando os tumores se tornam neuroendócrinos, mas como eles se influenciam mutuamente e conjuntamente orientam a identidade celular ainda não estava claramente mapeado.
Padrões que marcam tumores de próstata agressivos
Usando camundongos geneticamente modificados, amostras de tumores de pacientes e mini‑tumores cultivados em laboratório, os pesquisadores compararam o adenocarcinoma de próstata resistente à castração típico com o câncer de próstata neuroendócrino. Eles encontraram mudanças consistentes na metilação do DNA entre os dois estados: centenas de regiões genômicas perderam metilação, enquanto outras a ganharam. Surpreendentemente, regiões que ficaram menos metiladas em tumores neuroendócrinos frequentemente acumularam mais da marca ligada à EZH2, H3K27me3, mesmo que esses dois sistemas repressivos geralmente sejam considerados excludentes. Muitas dessas regiões ficavam próximas a genes envolvidos em características semelhantes a neurônios e em chamados promotores bivalentes, que mantêm genes de desenvolvimento prontos para serem rapidamente ativados ou silenciados.
O que acontece quando um freio é liberado
Para sondar causa e efeito, a equipe desativou EZH2 em modelos murinos propensos a evoluir para tumores neuroendócrinos e, separadamente, tratou organoides derivados de pacientes com um fármaco que bloqueia EZH2. Em ambos os contextos, o panorama global da metilação do DNA foi amplamente reprogramado. Regiões anteriormente alvo da EZH2 frequentemente se tornaram mais metiladas, enquanto outros trechos perderam metilação e ativaram genes ligados à diferenciação neural e a assinaturas neuroendócrinas conhecidas. Em outras palavras, remover o freio baseado em H3K27me3 permitiu que o sistema de metilação do DNA ocupasse o lugar e mantivesse muitos dos mesmos genes silenciados, ao mesmo tempo em que afrouxava o controle em outros sítios que reforçam o estado neuroendócrino.
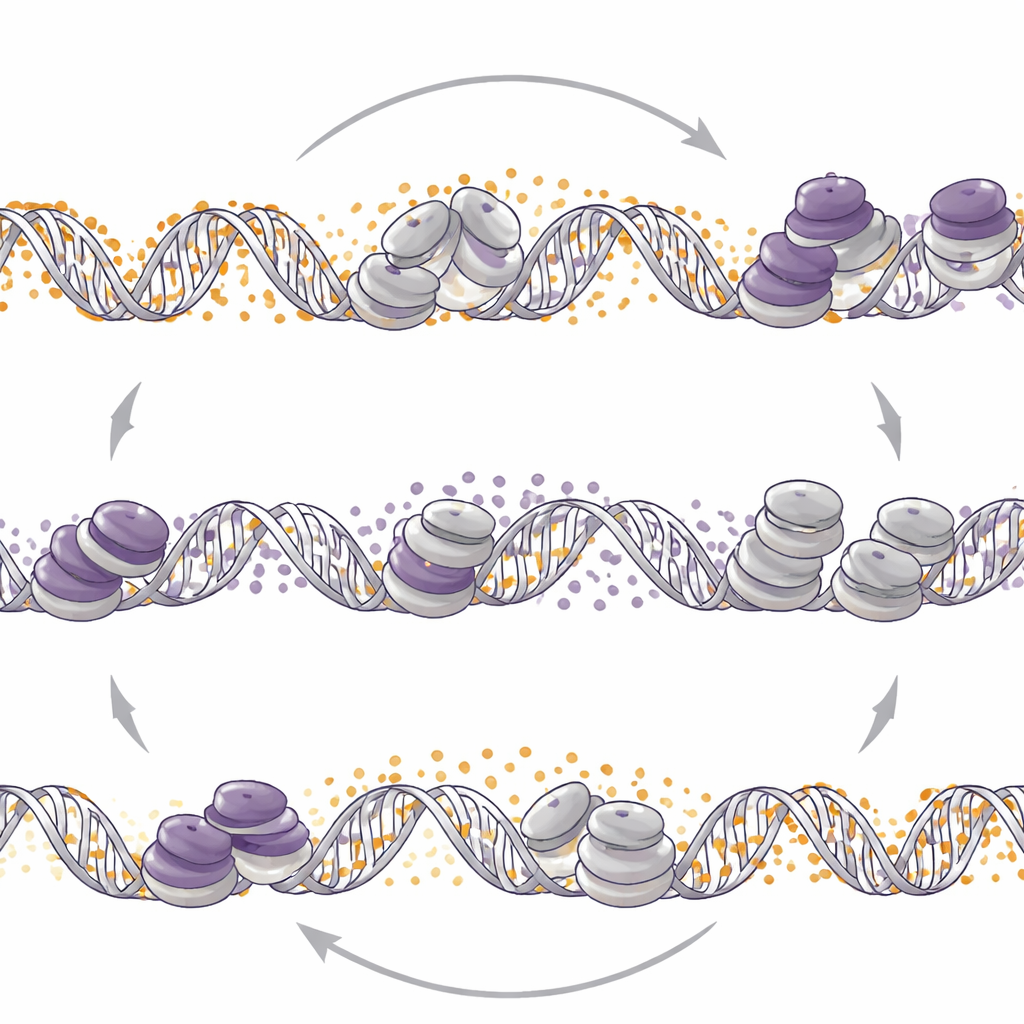
Virar o outro interruptor remodela o controle
Os cientistas então questionaram se o inverso também ocorria: alterar a metilação do DNA reposicionaria as marcas da EZH2? Quando deletaram DNMT1 ou usaram o fármaco decitabina, que reduz a metilação do DNA, em modelos neuroendócrinos, observaram ampla redistribuição de H3K27me3 pelo genoma. Nesses tumores, reduzir a metilação do DNA levou a mais H3K27me3 em certos promotores em prontidão, perda de uma marca de histona ativadora e atividade reduzida de genes neuroendócrinos. Em contraste, em uma linha celular de adenocarcinoma de próstata, a perda de DNMT1 diminuiu H3K27me3 em regiões prontas semelhantes e aumentou a marca ativadora, liberando genes relacionados ao fenótipo neuroendócrino. Assim, o mesmo empurrão molecular — enfraquecer DNMT1 — pode tanto frear quanto acender programas neuroendócrinos dependendo do contexto tumoral.
O que isso significa para tratamentos futuros
Em conjunto, esses experimentos revelam que a metilação do DNA e a marcação de histonas dirigida por EZH2 funcionam como dois freios coordenados que podem trocar de lugar para manter genes críticos silenciados ou em prontidão, ajudando tumores de próstata a trocar de identidade e resistir à terapia. Interferir em apenas um dos sistemas frequentemente desencadeia mudanças compensatórias no outro, o que pode limitar o benefício duradouro de fármacos que visam apenas EZH2 ou apenas a metilação do DNA. O trabalho sugere que estratégias cuidadosamente projetadas que levem em conta essa disputa molecular — possivelmente incluindo uso combinado ou temporizado de ambos os tipos de drogas epigenéticas — poderão um dia oferecer maneiras melhores de prevenir ou tratar as formas mais agressivas e resistentes ao tratamento do câncer de próstata.
Citação: Singh, R., Venkadakrishnan, V.B., Imada, E. et al. Crosstalk between EZH2 and DNA methylation mediates neuroendocrine prostate cancer lineage plasticity. Nat Commun 17, 2992 (2026). https://doi.org/10.1038/s41467-026-69308-0
Palavras-chave: câncer de próstata, tumores neuroendócrinos, epigenética, metilação do DNA, EZH2