Clear Sky Science · nl
Interactie tussen EZH2 en DNA-methylering bemiddelt lineage-plasticiteit bij neuro-endocriene prostaatkanker
Waarom de identiteit van kankercellen ertoe doet
Prostaattumoren blijven niet altijd hetzelfde in de loop van de tijd. Sommige zijn aanvankelijk afhankelijk van mannelijke hormonen en reageren op standaardbehandelingen, maar schakelen later over naar een veel agressievere vorm die neuro-endocriene prostaatkanker wordt genoemd. Dit vermogen om van vorm te veranderen, bekend als lineage-plasticiteit, helpt tumoren therapie te ontlopen en is een belangrijke oorzaak van behandelingsfalen. De hier samengevatte studie onderzoekt hoe twee chemische "uit-schakelaars" op het DNA en zijn verpakking samenwerken om deze gevaarlijke identiteitsverandering te beheersen, en hoe het blokkeren van de ene schakel de ander kan laten compenseren.
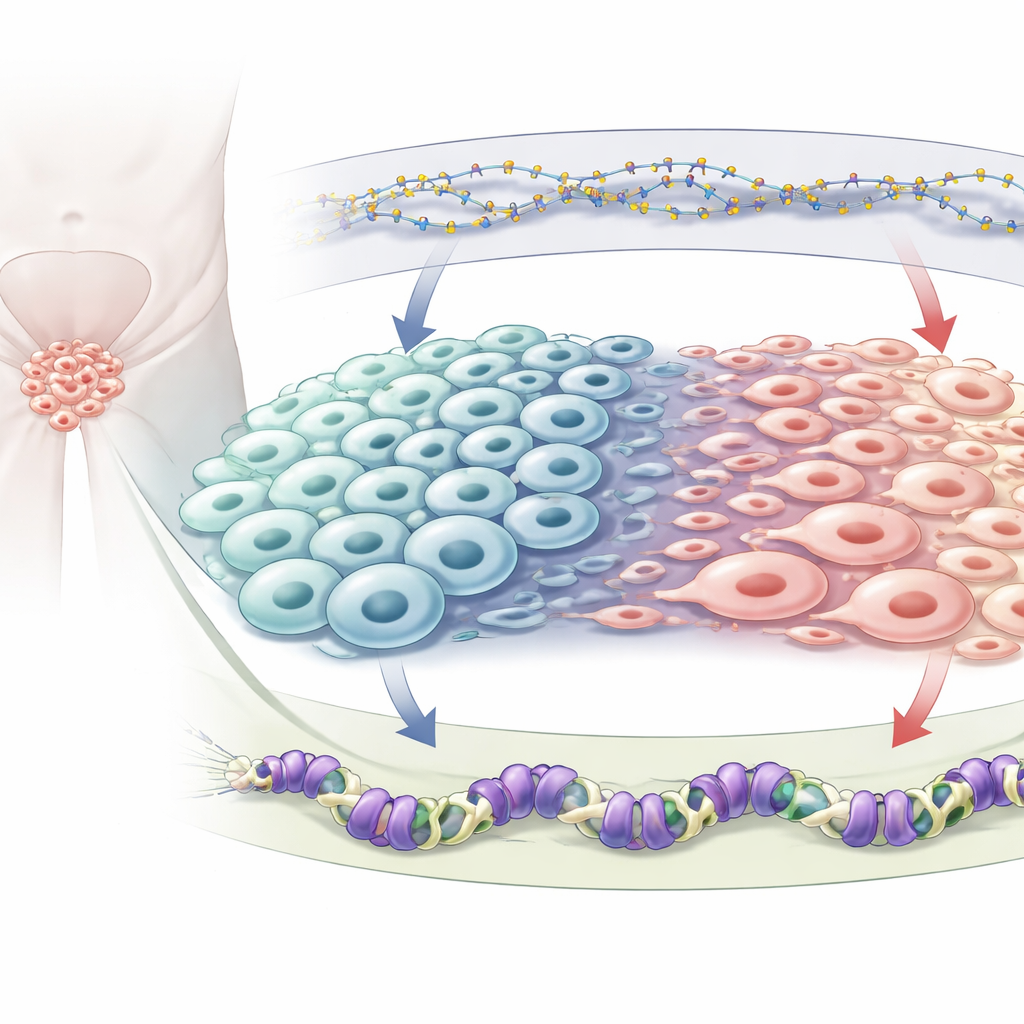
Twee chemische remmen op het genoom
Elke cel draagt dezelfde genen, maar chemische markeringen bepalen welke aan of uit staan. De auteurs richten zich op twee soorten repressieve markeringen. De ene is DNA-methylering, waarbij kleine chemische groepjes direct op DNA worden gezet en meestal nabije genen uitschakelen; dit wordt in stand gehouden door een enzym genaamd DNMT1. De andere is een markering genaamd H3K27me3 die op DNA-opwikkelende eiwitten zit en wordt aangebracht door een eiwit genaamd EZH2, onderdeel van het polycomb repressive complex 2. Beide systemen staan bekend om veranderingen in prostaatkanker, vooral wanneer tumoren neuro-endocrien worden, maar hoe ze elkaar beïnvloeden en samen de celidentiteit sturen, was niet duidelijk in kaart gebracht.
Patronen die agressieve prostaattumoren kenmerken
Met behulp van genetisch gemodificeerde muizen, patiëntentumor-monsters en miniatuurtumoren gekweekt in het laboratorium, vergeleken de onderzoekers typische castratie-resistente prostaatadenocarcinomen met neuro-endocriene prostaatkanker. Ze vonden consistente verschuivingen in DNA-methylering tussen de twee toestanden: honderden genomische regio's verloren methylering, terwijl andere deze wonnen. Opvallend was dat regio's die minder gemethyleerd werden in neuro-endocriene tumoren vaak juist meer van het EZH2-gekoppelde H3K27me3-mark kregen, ook al worden deze twee repressieve systemen gewoonlijk gedacht elkaar te vermijden. Veel van deze regio's lagen nabij genen die betrokken zijn bij zenuwachtige kenmerken en bij zogenaamde bivalente promoters, die ontwikkelingsgenen in gereedheid houden voor snelle activering of uitschakeling.
Wat er gebeurt als één rem wordt losgelaten
Om oorzaak en gevolg te onderzoeken, schakelde het team EZH2 uit in muismodellen die geneigd zijn uit te groeien tot neuro-endocriene tumoren, en behandelde afzonderlijk patient-afgeleide organoïden met een EZH2-remmend middel. In beide instellingen werd het globale DNA-methyleringslandschap ingrijpend herschikt. Regio's die eerder door EZH2 werden getarget, werden vaak juist meer gemethyleerd, terwijl andere stukken methylering verloren en genen activeerden die gekoppeld zijn aan neurale differentiatie en bekende neuro-endocriene signaturen. Met andere woorden, het weghalen van de H3K27me3-gebaseerde rem liet het DNA-methyleringssysteem toe in te grijpen en veel van dezelfde genen stil te houden, terwijl tegelijkertijd de controle op andere locaties werd versoepeld die de neuro-endocriene toestand versterken.
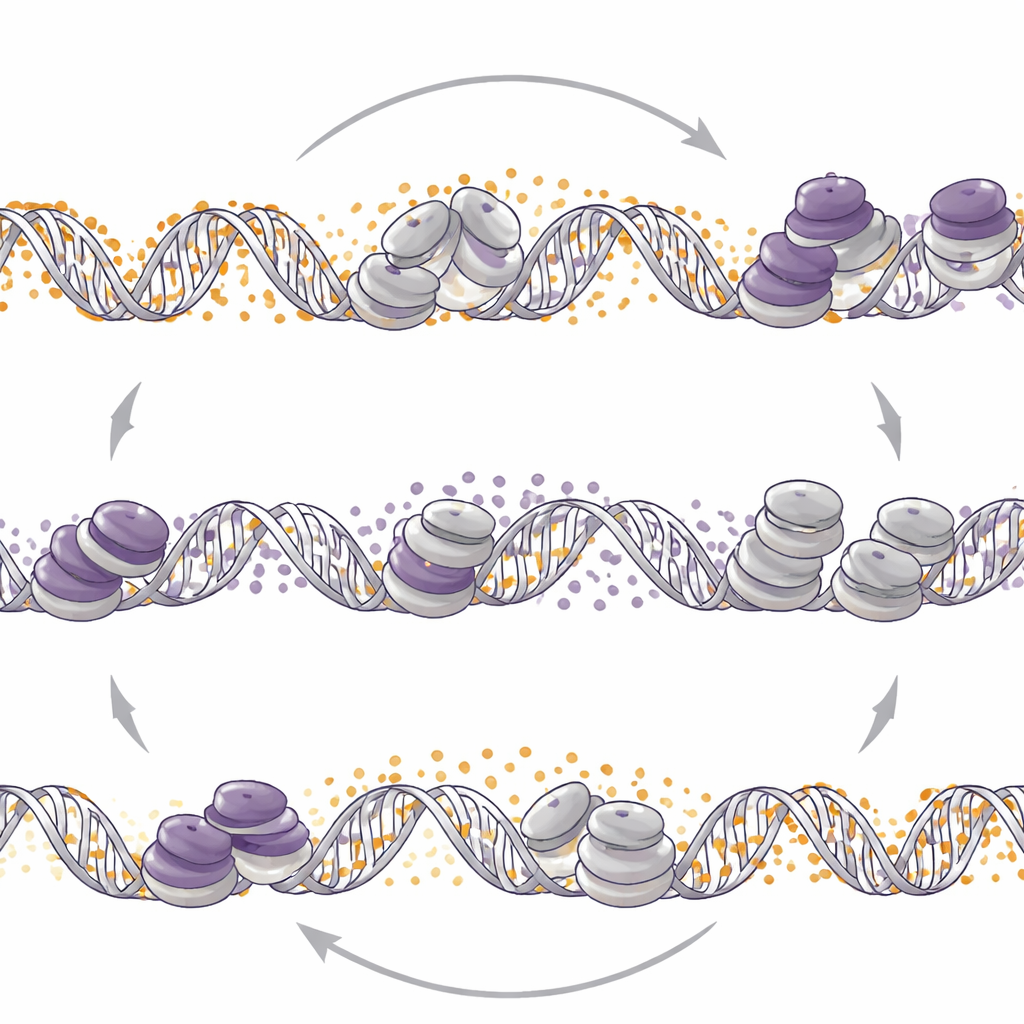
De andere schakel omzetten hervormt de controle
De wetenschappers vroegen zich vervolgens af of het omgekeerde ook gold: herschikt het veranderen van DNA-methylering de EZH2-markeringen? Toen ze DNMT1 verwijderden of het DNA-methylering-verlagende middel decitabine gebruikten in neuro-endocriene modellen, zagen ze brede herverdeling van H3K27me3 over het genoom. In deze tumoren leidde vermindering van DNA-methylering tot meer H3K27me3 op bepaalde gereedstaande promoters, verlies van een activerende histonmarkering en verminderde activiteit van neuro-endocriene genen. Daarentegen verminderde in een prostaatadenocarcinoomcelijn verlies van DNMT1 H3K27me3 op vergelijkbare gereedstaande regio's en nam de activerende markering toe, waarmee neuro-endocriene-gerelateerde genen werden ontketend. Dus dezelfde moleculaire aansporing — verzwakking van DNMT1 — kan afhankelijk van de tumorcontext ofwel neuro-endocriene programma's dempen of juist aanwakkeren.
Wat dit betekent voor toekomstige behandelingen
Samen laten deze experimenten zien dat DNA-methylering en door EZH2 aangedreven histonmarkering zich gedragen als twee gecoördineerde remmen die van plaats kunnen wisselen om cruciale genen stil of gereed te houden, waardoor prostaattumoren van identiteit kunnen wisselen en therapie kunnen weerstaan. Het verstoren van slechts één systeem roept vaak compenserende veranderingen in het andere op, wat het duurzame nut van geneesmiddelen die alleen EZH2 of DNA-methylering targeten kan beperken. Het werk suggereert dat zorgvuldig ontworpen strategieën die rekening houden met dit moleculaire touwtrekken — mogelijk inclusief combinatie- of getimede inzet van beide typen epigenetische geneesmiddelen — op termijn betere manieren kunnen bieden om de meest agressieve, therapieresistente vormen van prostaatkanker te voorkomen of behandelen.
Bronvermelding: Singh, R., Venkadakrishnan, V.B., Imada, E. et al. Crosstalk between EZH2 and DNA methylation mediates neuroendocrine prostate cancer lineage plasticity. Nat Commun 17, 2992 (2026). https://doi.org/10.1038/s41467-026-69308-0
Trefwoorden: prostaatkanker, neuro-endocriene tumoren, epigenetica, DNA-methylering, EZH2