Clear Sky Science · de
Wechselwirkung zwischen EZH2 und DNA‑Methylierung vermittelt die linien‑plastizität neuroendokriner Prostatakrebszellen
Warum die Identität von Krebszellen wichtig ist
Prostatatumoren bleiben nicht immer gleich. Manche sind anfangs hormonsensitiv und sprechen auf Standardtherapien an, können sich aber später in eine deutlich aggressivere Form verwandeln, den neuroendokrinen Prostatakrebs. Diese Form‑wandlungsfähigkeit, genannt Linienplastizität, hilft Tumoren, Therapien zu entkommen, und ist eine Hauptursache für Therapieversagen. Die hier zusammengefasste Studie untersucht, wie zwei chemische „Abschalter“ auf der DNA und ihrer Verpackung zusammenwirken, um diesen gefährlichen Identitätswechsel zu steuern, und wie das Blockieren eines Schalters dazu führt, dass der andere kompensiert.
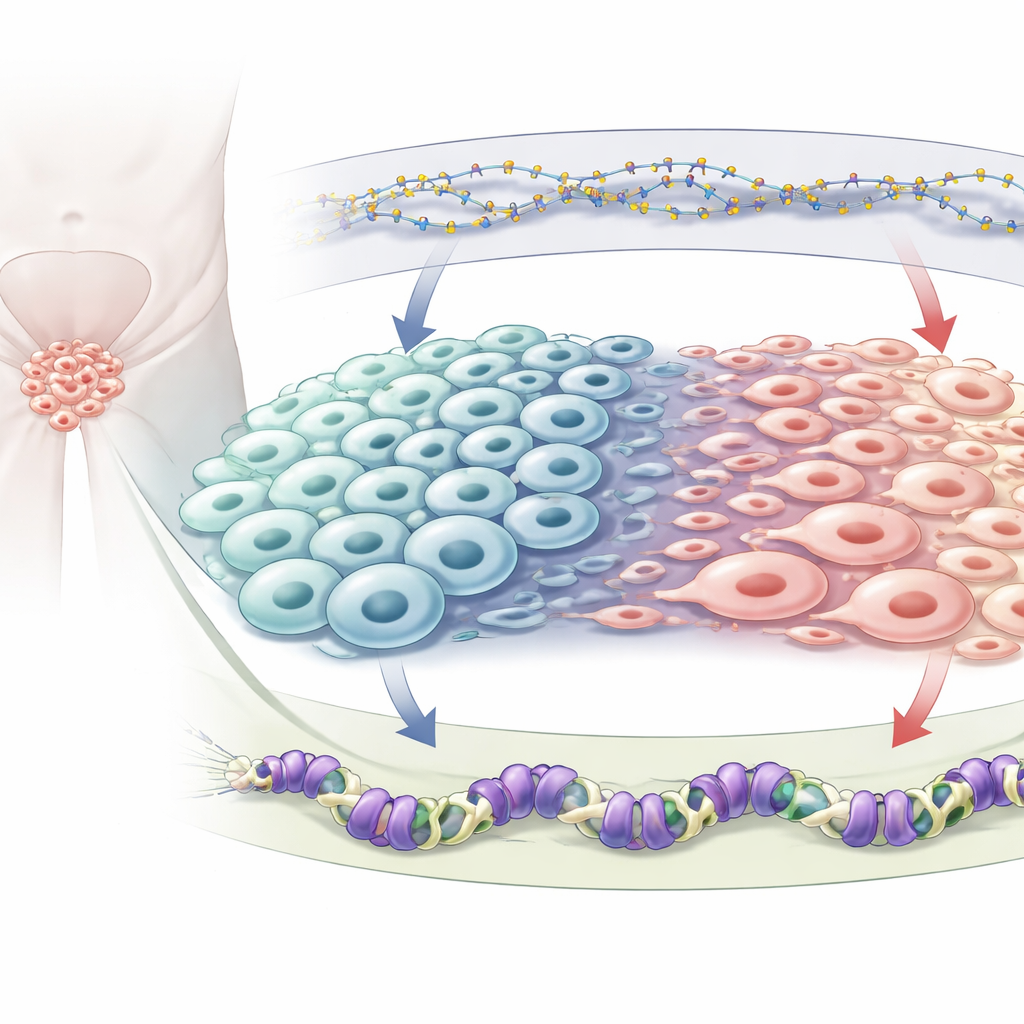
Zwei chemische Bremsen im Genom
Jede Zelle trägt dieselben Gene, doch chemische Markierungen entscheiden, welche Gene an- oder ausgeschaltet sind. Die Autoren konzentrieren sich auf zwei Typen repressiver Markierungen. Die eine ist die DNA‑Methylierung, bei der kleine chemische Gruppen direkt an die DNA angefügt werden und in der Regel nahegelegene Gene stummschalten; sie wird durch ein Enzym namens DNMT1 aufrechterhalten. Die andere ist eine Markierung namens H3K27me3, die auf den DNA‑umschlingenden Proteinen sitzt und von einem Protein namens EZH2 angebracht wird, das Teil des Polycomb‑Repressivkomplexes 2 ist. Beide Systeme verändern sich bekanntermaßen beim Prostatakrebs, insbesondere wenn Tumoren neuroendokrin werden, doch wie sie sich gegenseitig beeinflussen und gemeinsam die Zellidentität lenken, war bisher nicht klar kartiert.
Muster, die aggressive Prostatatumoren kennzeichnen
Mit genetisch veränderten Mäusen, Patientenproben und im Labor gezüchteten Miniaturtumoren verglichen die Forscher typisches kastrationsresistentes Prostataadenokarzinom mit neuroendokrinem Prostatakrebs. Sie fanden konsistente Verschiebungen der DNA‑Methylierung zwischen den beiden Zuständen: Hunderte genomische Regionen verloren Methylierung, andere gewannen sie. Auffallend war, dass Regionen, die in neuroendokrinen Tumoren weniger methyliert wurden, häufig mehr der EZH2‑verknüpften H3K27me3‑Markierung akkumulierten, obwohl davon ausgegangen wird, dass diese beiden repressiven Systeme sich normalerweise gegenseitig meiden. Viele dieser Regionen lagen in der Nähe von Genen, die an nervenähnlichen Eigenschaften beteiligt sind, sowie an sogenannten bivalenten Promotoren, die Entwicklungsgene in Bereitschaft halten, schnell ein- oder ausgeschaltet zu werden.
Was passiert, wenn eine Bremse gelöst wird
Um Ursache und Wirkung zu prüfen, schaltete das Team EZH2 in Mausmodellen aus, die dazu neigen, sich in neuroendokrine Tumoren zu entwickeln, und behandelte getrennt patientenabgeleitete Organoide mit einem EZH2‑Blocker. In beiden Systemen wurde die globale DNA‑Methylierungslandschaft umfassend umgestaltet. Regionen, die zuvor von EZH2 betroffen waren, wurden oft stärker methyliert, während andere Abschnitte Methylierung verloren und Gene aktivierten, die mit neuronaler Differenzierung und bekannten neuroendokrinen Signaturen verknüpft sind. Anders gesagt: Das Entfernen der H3K27me3‑basierten Bremse erlaubte dem DNA‑Methylierungssystem, einzurücken und viele derselben Gene weiterhin stummzuhalten, während gleichzeitig an anderen Stellen die Kontrolle gelockert wurde, die den neuroendokrinen Zustand verstärken.
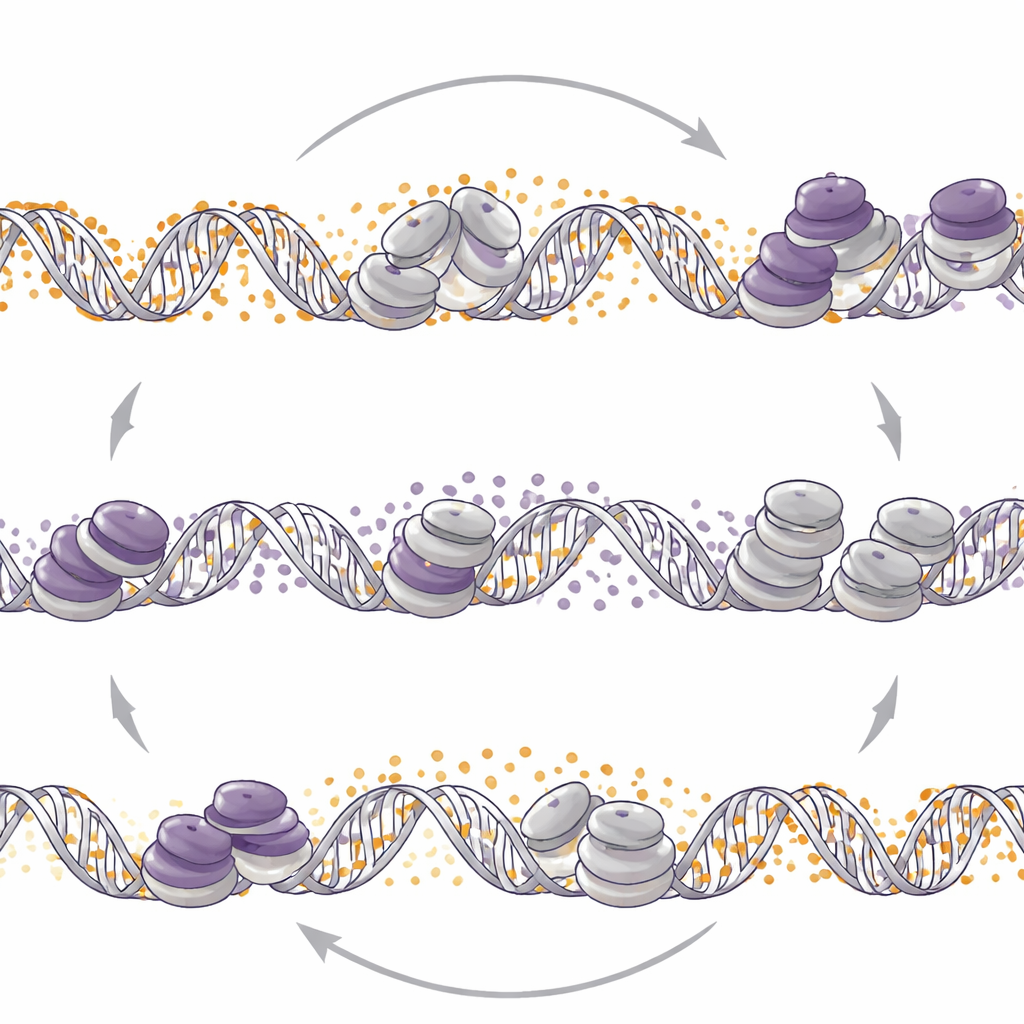
Den anderen Schalter umlegen verändert die Kontrolle
Die Wissenschaftler fragten dann, ob es auch umgekehrt gilt: Verschiebt die Veränderung der DNA‑Methylierung die EZH2‑Marken? Als sie DNMT1 löschten oder das DNA‑Methylierungssenkende Medikament Decitabin in neuroendokrinen Modellen einsetzten, beobachteten sie eine breite Umverteilung von H3K27me3 im Genom. In diesen Tumoren führte die Reduktion der DNA‑Methylierung zu mehr H3K27me3 an bestimmten bereitstehenden Promotoren, zum Verlust einer aktivierenden Histonmarke und zu verminderter Aktivität neuroendokriner Gene. Im Gegensatz dazu verringerte in einer Prostataadenokarzinom‑Zelllinie der Verlust von DNMT1 H3K27me3 an ähnlichen bereitstehenden Regionen und erhöhte die aktivierende Marke, wodurch neuroendokrine Gene entfesselt wurden. Somit kann dieselbe molekulare Veränderung—Schwächung von DNMT1—je nach Tumorkontext entweder neuroendokrine Programme dämpfen oder entfachen.
Was das für künftige Behandlungen bedeutet
Zusammen zeigen diese Experimente, dass DNA‑Methylierung und EZH2‑vermittelte Histonmarkierung wie zwei koordinierte Bremsen agieren, die Plätze tauschen können, um kritische Gene stumm oder bereit zu halten und so Prostatatumoren zu helfen, ihre Identität zu wechseln und Therapien zu widerstehen. Die alleinige Beeinflussung eines Systems löst häufig kompensatorische Veränderungen im anderen aus, was den anhaltenden Nutzen von Medikamenten, die nur EZH2 oder nur die DNA‑Methylierung anvisieren, einschränken könnte. Die Arbeit legt nahe, dass sorgfältig gestaltete Strategien, die diesen molekularen Tauziehen‑Effekt berücksichtigen—möglicherweise Kombinationen oder zeitlich abgestimmter Einsatz beider Arten epigenetischer Wirkstoffe—eines Tages bessere Möglichkeiten bieten könnten, die aggressivsten, therapieresistenten Formen des Prostatakrebses zu verhindern oder zu behandeln.
Zitation: Singh, R., Venkadakrishnan, V.B., Imada, E. et al. Crosstalk between EZH2 and DNA methylation mediates neuroendocrine prostate cancer lineage plasticity. Nat Commun 17, 2992 (2026). https://doi.org/10.1038/s41467-026-69308-0
Schlüsselwörter: Prostatakrebs, neuroendokrine Tumoren, Epigenetik, DNA‑Methylierung, EZH2