Clear Sky Science · fr
Interférence entre EZH2 et la méthylation de l’ADN médiant la plasticité de lignée du cancer de la prostate neuroendocrine
Pourquoi l’identité des cellules cancéreuses compte
Les tumeurs prostatiques ne restent pas toujours identiques au fil du temps. Certaines dépendent initialement des hormones mâles et répondent aux traitements standards, mais évoluent ensuite vers une forme beaucoup plus agressive appelée cancer de la prostate neuroendocrine. Cette capacité à changer de forme, dite plasticité de lignée, aide les tumeurs à échapper aux thérapies et constitue une cause majeure d’échec des traitements. L’étude résumée ici examine comment deux « interrupteurs » chimiques sur l’ADN et son empaquetage collaborent pour contrôler ce changement d’identité dangereux, et comment le blocage d’un interrupteur peut amener l’autre à compenser.
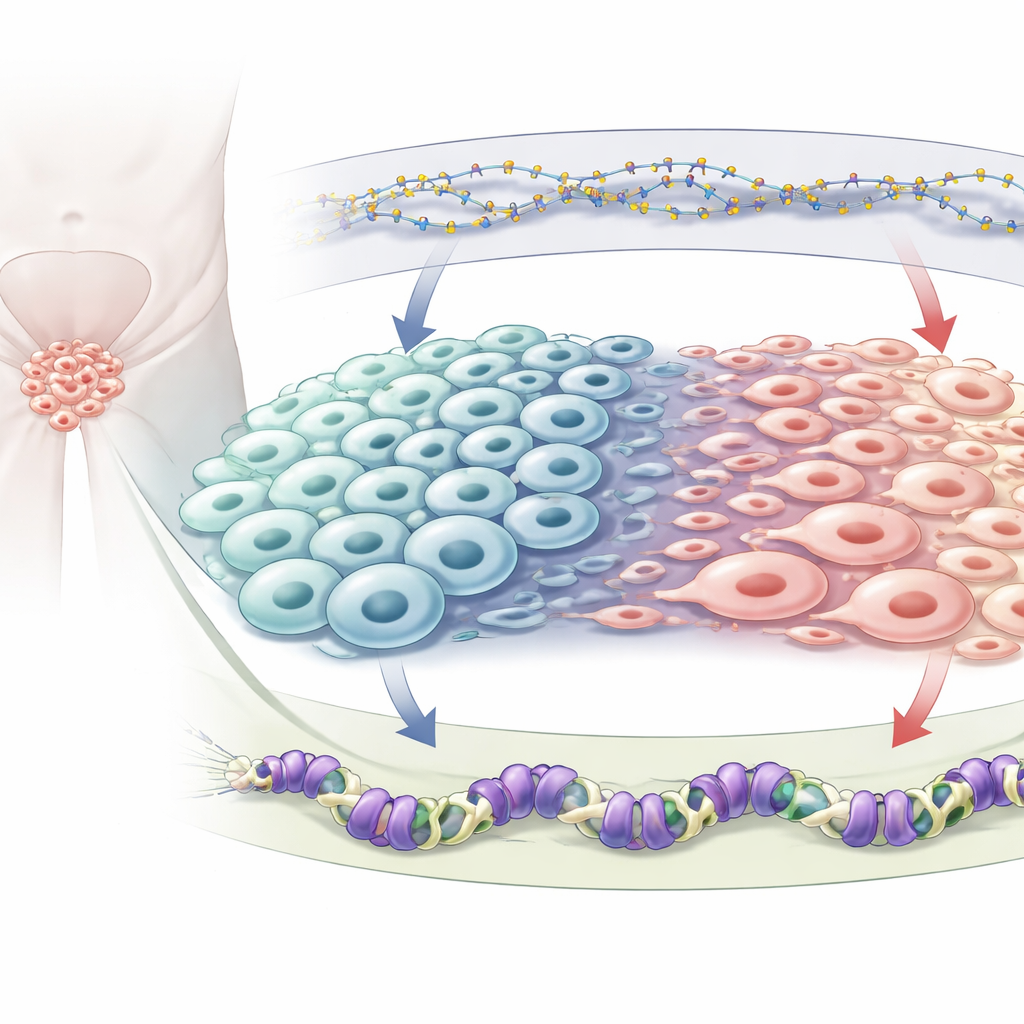
Deux freins chimiques sur le génome
Chaque cellule porte les mêmes gènes, mais des étiquettes chimiques décident lesquels sont activés ou désactivés. Les auteurs se concentrent sur deux types d’étiquettes répressives. L’une est la méthylation de l’ADN, où de petits groupes chimiques sont ajoutés directement sur l’ADN et silencient généralement les gènes voisins ; elle est maintenue par une enzyme appelée DNMT1. L’autre est une marque appelée H3K27me3 qui se situe sur les protéines autour desquelles l’ADN s’enroule et est déposée par une protéine nommée EZH2, composante du complexe répressif Polycomb 2. On sait que les deux systèmes changent dans le cancer de la prostate, en particulier lorsque les tumeurs deviennent neuroendocrines, mais la façon dont ils s’influencent mutuellement et guident ensemble l’identité cellulaire n’avait pas été clairement cartographiée.
Des motifs qui caractérisent les tumeurs prostatiques agressives
En utilisant des souris génétiquement modifiées, des échantillons de tumeurs humaines et des organoïdes tumoraux cultivés en laboratoire, les chercheurs ont comparé l’adénocarcinome prostatique résistant à la castration typique au cancer de la prostate neuroendocrine. Ils ont observé des changements cohérents de la méthylation de l’ADN entre les deux états : des centaines de régions génomiques perdaient de la méthylation, tandis que d’autres en gagnaient. Fait frappant, les régions devenues moins méthylées dans les tumeurs neuroendocrines accumulaient souvent davantage la marque liée à EZH2, H3K27me3, alors que ces deux systèmes répressifs sont généralement considérés comme s’excluant mutuellement. Beaucoup de ces régions se situaient à proximité de gènes impliqués dans des caractéristiques de type nerveux et de promoteurs dits bivalents, qui maintiennent les gènes de développement prêts à être rapidement activés ou réprimés.
Que se passe-t-il quand un frein est relâché
Pour étudier la cause et l’effet, l’équipe a désactivé EZH2 dans des modèles murins susceptibles d’évoluer en tumeurs neuroendocrines, et a séparément traité des organoïdes dérivés de patients avec un médicament inhibant EZH2. Dans les deux contextes, le paysage global de la méthylation de l’ADN a été largement remanié. Les régions précédemment ciblées par EZH2 devenaient souvent davantage méthylées, tandis que d’autres segments perdaient leur méthylation et activaient des gènes liés à la différenciation neuronale et aux signatures neuroendocrines connues. Autrement dit, supprimer le frein basé sur H3K27me3 a permis au système de méthylation de l’ADN d’intervenir et de maintenir l’inhibition de nombreux mêmes gènes, tout en desserrant le contrôle à d’autres sites qui renforcent l’état neuroendocrine.
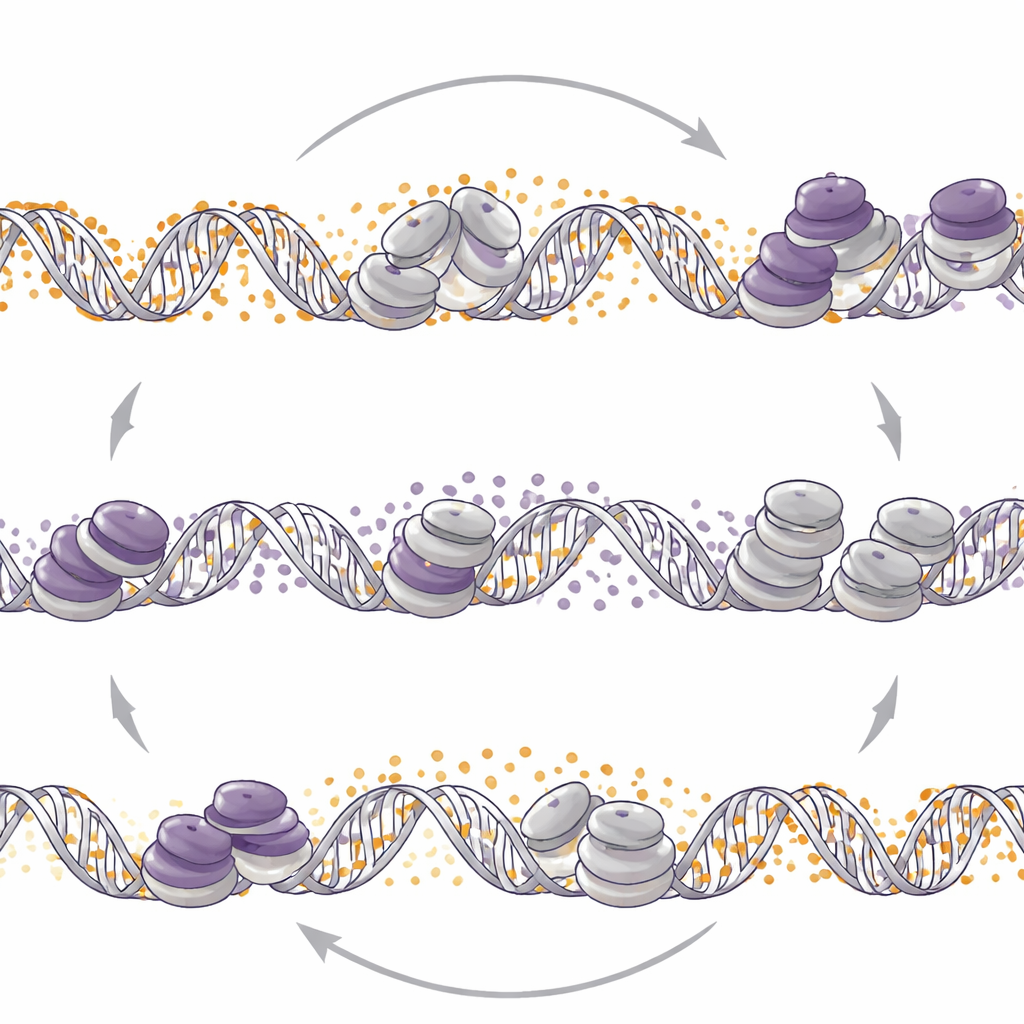
Inverser l’autre interrupteur redessine le contrôle
Les scientifiques ont ensuite demandé si l’inverse était vrai : altérer la méthylation de l’ADN repositionne‑t‑il les marques d’EZH2 ? Lorsqu’ils ont supprimé DNMT1 ou utilisé le médicament décitabine réduisant la méthylation de l’ADN dans des modèles neuroendocrines, ils ont observé une redistribution large de H3K27me3 à travers le génome. Dans ces tumeurs, la réduction de la méthylation de l’ADN conduisait à davantage de H3K27me3 à certains promoteurs en attente, à la perte d’une marque d’histone activatrice et à une activité réduite des gènes neuroendocrines. En revanche, dans une lignée cellulaire d’adénocarcinome prostatique, la perte de DNMT1 diminuait H3K27me3 à des régions bivalentes similaires et augmentait la marque activatrice, déclenchant l’expression de gènes liés au phénotype neuroendocrine. Ainsi, la même impulsion moléculaire — affaiblir DNMT1 — peut soit atténuer, soit déclencher des programmes neuroendocrines selon le contexte tumoral.
Ce que cela signifie pour les traitements futurs
Ensemble, ces expériences révèlent que la méthylation de l’ADN et le marquage histone piloté par EZH2 agissent comme deux freins coordonnés qui peuvent se remplacer pour garder des gènes critiques silencieux ou en état de prédisposition, aidant les tumeurs prostatiques à changer d’identité et à résister aux thérapies. Interférer avec un seul système déclenche souvent des changements compensatoires dans l’autre, ce qui peut limiter le bénéfice durable des traitements ciblant isolément EZH2 ou la méthylation de l’ADN. Ces travaux suggèrent que des stratégies soigneusement conçues tenant compte de cette lutte moléculaire — incluant potentiellement des combinaisons ou des utilisations temporisées des deux types de médicaments épigénétiques — pourraient un jour offrir de meilleures façons de prévenir ou de traiter les formes les plus agressives et résistantes du cancer de la prostate.
Citation: Singh, R., Venkadakrishnan, V.B., Imada, E. et al. Crosstalk between EZH2 and DNA methylation mediates neuroendocrine prostate cancer lineage plasticity. Nat Commun 17, 2992 (2026). https://doi.org/10.1038/s41467-026-69308-0
Mots-clés: cancer de la prostate, tumeurs neuroendocrines, épigénétique, méthylation de l’ADN, EZH2