Clear Sky Science · ja
EZH2とDNAメチル化の相互作用が神経内分泌前立腺がんの系統可塑性を仲介する
なぜがん細胞の“アイデンティティ”が重要か
前立腺腫瘍は時間とともに同じままでいるとは限りません。初期には男性ホルモンに依存し標準治療に反応することが多くても、後に神経内分泌前立腺がんと呼ばれるはるかに悪性の形態へと変化することがあります。この形を変える能力は系統可塑性として知られ、腫瘍が治療から逃れるのを助け、治療失敗の主要因となります。本稿で概説する研究は、DNAとその包装に付く二つの化学的な「オフスイッチ」が協調してこの危険なアイデンティティ変化を制御する仕組みと、片方のスイッチを遮断するともう一方が補償する様子を探っています。
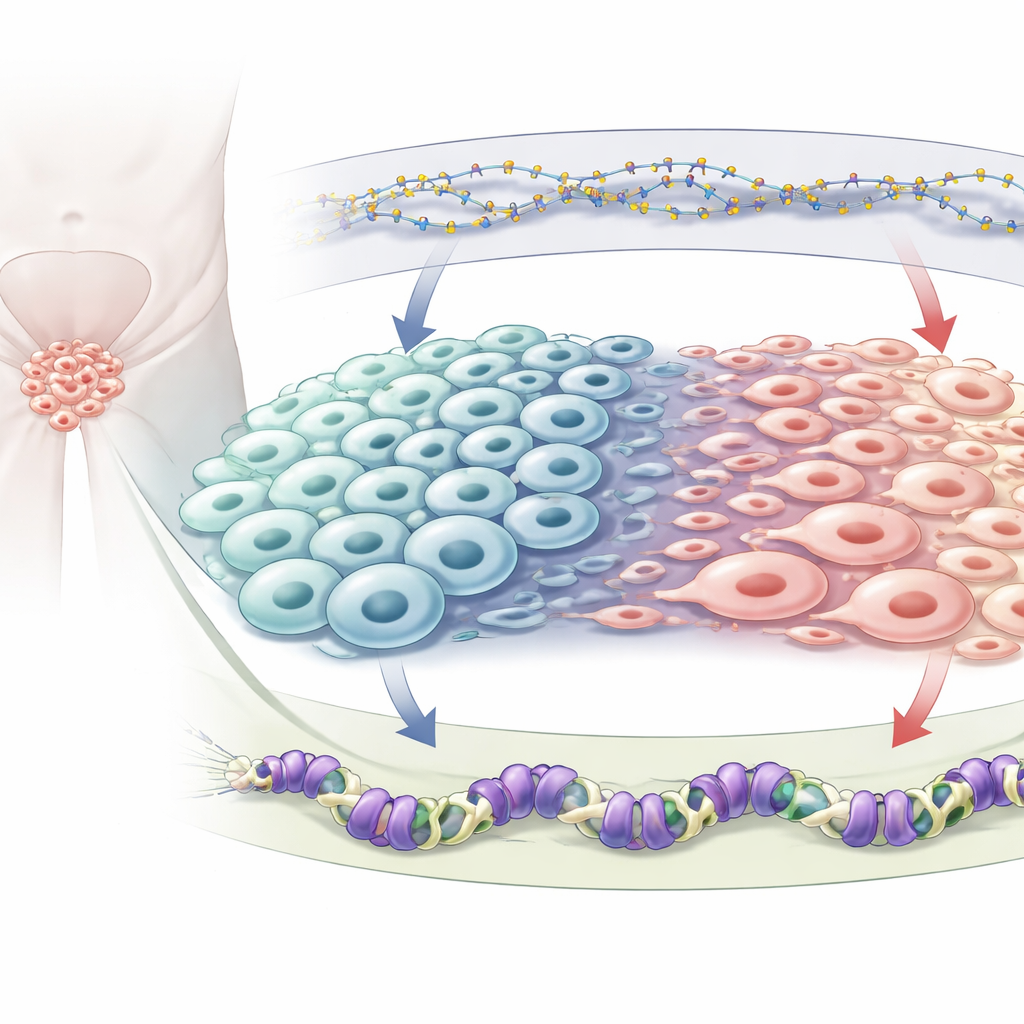
ゲノムにかかる二つの化学的ブレーキ
すべての細胞は同じ遺伝子を持っていますが、化学的なタグがどの遺伝子をオンにするかオフにするかを決めます。著者らが注目するのは二種類の抑制的タグです。一つはDNAメチル化で、小さな化学基がDNA自体に付加されて近傍の遺伝子を通常は沈黙させます。これを維持する酵素がDNMT1です。もう一つはH3K27me3と呼ばれるタグで、DNAを巻くヒストンに付けられ、ポリコーム抑制複合体2の一部であるタンパク質EZH2によって付与されます。これら両方のシステムは前立腺がん、特に腫瘍が神経内分泌化する際に変化することが知られていますが、互いにどう影響し合い、細胞のアイデンティティをどのように共同で導くかは明確に解明されていませんでした。
攻撃的な前立腺腫瘍を特徴づけるパターン
遺伝子工学的マウス、患者由来腫瘍サンプル、培養で育てたミニ腫瘍を用いて、研究者らは典型的な去勢抵抗性前立腺腺がんと神経内分泌前立腺がんを比較しました。両状態の間で一貫したDNAメチル化の変化が見られました:数百のゲノム領域でメチル化が失われる一方、別の領域ではメチル化が増加していました。注目すべきは、神経内分泌腫瘍でメチル化が減少した領域の多くが、通常は互いに避けると考えられているにもかかわらず、EZH2に関連するH3K27me3マークを蓄積していたことです。これらの領域の多くは神経様の特徴に関与する遺伝子や、発生遺伝子を迅速にオン/オフできるように待機状態に保ついわゆる両価プロモーター付近に位置していました。
片方のブレーキを外すと何が起きるか
因果関係を調べるために、チームは神経内分泌腫瘍へ進展しやすいマウスモデルでEZH2を無効化し、別に患者由来オルガノイドをEZH2阻害薬で処理しました。どちらの場合でも、全体的なDNAメチル化の景観は大きく再配線されました。以前EZH2の標的だった領域はしばしばより多くメチル化されるようになり、他の領域はメチル化を失って神経分化や既知の神経内分泌シグネチャーに結びつく遺伝子が活性化しました。言い換えれば、H3K27me3に基づくブレーキを取り除くとDNAメチル化システムが入り込み、多くの同じ遺伝子を沈黙させ続ける一方で、神経内分泌状態を強化する別の部位での抑制を緩めました。
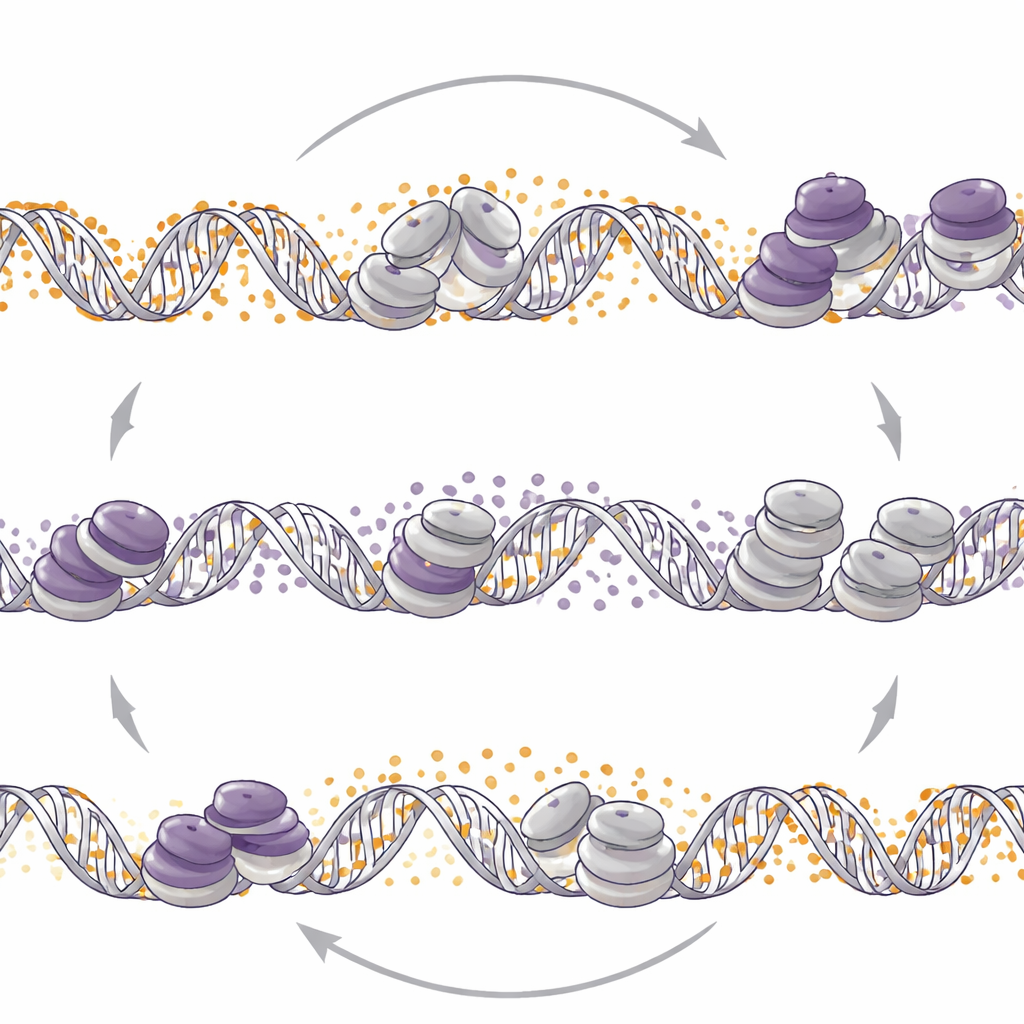
もう一方のスイッチを切り替えると制御が再構築される
研究者らは逆もまた真かを問い、DNAメチル化を変えるとEZH2マークの再配置が起きるかを調べました。DNMT1を欠失させるか、神経内分泌モデルでDNAメチル化を下げる薬デシタビンを使うと、ゲノム全体でH3K27me3の広範な再分布が観察されました。これらの腫瘍ではDNAメチル化を減らすと特定の待機プロモーターでH3K27me3が増加し、活性化に関わるヒストン修飾が失われ、神経内分泌遺伝子の活性が低下しました。対照的に、前立腺腺がんの細胞株ではDNMT1の喪失が同様の待機領域でH3K27me3を減少させ、活性化タグを増加させて神経内分泌関連遺伝子を解き放ちました。したがって同じ分子レベルの変化—DNMT1の弱化—が腫瘍の文脈に応じて神経内分泌プログラムを抑制することも点火することもあり得ます。
将来の治療にとっての意味
これらの実験は、DNAメチル化とEZH2駆動のヒストン修飾が二つの協調するブレーキのように振る舞い、重要な遺伝子を沈黙または待機状態に保つために場所を交換し得ることを示しています。これが前立腺腫瘍に系統変化をもたらし、治療抵抗性を助長します。片方のシステムだけを妨げると、しばしばもう一方に補償的な変化を引き起こし、単独でEZH2やDNAメチル化を標的とする薬剤の持続的な効果を制限する可能性があります。本研究は、この分子間の綱引きを踏まえた慎重に設計された戦略、たとえば両者の薬を組み合わせるかタイミングを調整して用いることが、最も攻撃的で治療抵抗性の高い前立腺がんを予防または治療するためのより良い方法を提供し得ることを示唆しています。
引用: Singh, R., Venkadakrishnan, V.B., Imada, E. et al. Crosstalk between EZH2 and DNA methylation mediates neuroendocrine prostate cancer lineage plasticity. Nat Commun 17, 2992 (2026). https://doi.org/10.1038/s41467-026-69308-0
キーワード: 前立腺がん, 神経内分泌腫瘍, エピジェネティクス, DNAメチル化, EZH2