Clear Sky Science · sv
Korssignalering mellan EZH2 och DNA‑metylering medierar neuroendokrint prostatacancer‑linjeplasticitet
Varför cancercellsidentitet spelar roll
Prostatatumörer förblir inte alltid oförändrade över tid. Vissa är initialt beroende av manliga hormoner och svarar på standardbehandlingar, men kan senare övergå till en mycket mer aggressiv form som kallas neuroendokrint prostatacancer. Denna formskiftande förmåga, känd som linjeplasticitet, hjälper tumörer att undkomma terapi och är en huvudorsak till behandlingssvikt. Den studie som sammanfattas här undersöker hur två kemiska ”avstängningsreglage” på DNA och dess paketering samverkar för att styra denna farliga identitetsförändring, och hur blockering av det ena reglaget kan få det andra att kompensera.
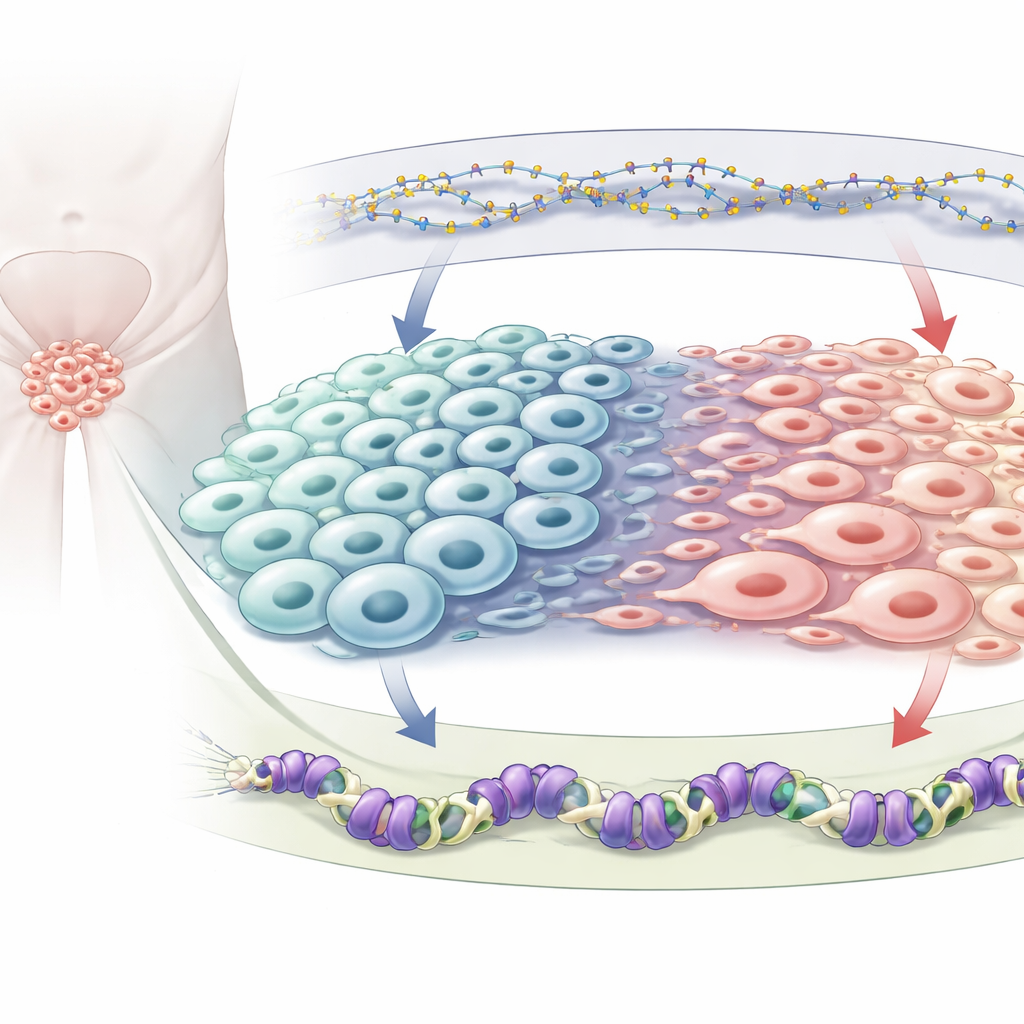
Två kemiska bromsar på genomet
Varje cell bär på samma gener, men kemiska märken avgör vilka som är på eller av. Författarna fokuserar på två typer av repressiva märkningar. Den ena är DNA‑metylering, där små kemiska grupper sätts direkt på DNA och vanligen tystar närliggande gener; detta upprätthålls av ett enzym kallat DNMT1. Den andra är ett märke som kallas H3K27me3 som sitter på DNA‑inpackande proteiner och sätts dit av ett protein som heter EZH2, en del av polycomb repressive complex 2. Båda systemen är kända för att förändras i prostatacancer, särskilt när tumörer blir neuroendokrina, men hur de påverkar varandra och tillsammans styr cellidentitet hade inte tidigare kartlagts tydligt.
Mönster som kännetecknar aggressiva prostatatumörer
Genom att använda genetiskt modifierade möss, patienttumörprover och miniatyrtumörer odlade i labbet, jämförde forskarna typisk kastrationsresistent prostataadenocarcinom med neuroendokrint prostatacancer. De fann konsekventa skift i DNA‑metylering mellan de två tillstånden: hundratals genomiska regioner förlorade metylering, medan andra fick mer. Slående nog ackumulerade regioner som blev mindre metylerade i de neuroendokrina tumörerna ofta mer av EZH2‑kopplat märke H3K27me3, trots att dessa två repressiva system vanligtvis antas undvika varandra. Många av dessa regioner låg nära gener involverade i nervlika egenskaper och vid så kallade bivalenta promotorer, som håller utvecklingsgener i beredskap för snabb aktivering eller tystnad.
Vad som händer när en broms släpps
För att undersöka orsak och verkan inaktiverade forskarna EZH2 i musmodeller som lätt utvecklas till neuroendokrina tumörer, och behandlade separat patient‑härledda organoider med ett EZH2‑blockerande läkemedel. I båda fallen omlades det globala DNA‑metyleringslandskapet i stor utsträckning. Regioner som tidigare var mål för EZH2 blev ofta mer metylerade, medan andra områden förlorade metylering och aktiverade gener kopplade till neural differentiering och kända neuroendokrina signaturer. Med andra ord, att ta bort H3K27me3‑baserade bromsen tillät DNA‑metyleringssystemet att flytta in och hålla många av samma gener tysta, samtidigt som kontrollen lossnade vid andra platser som stärker det neuroendokrina tillståndet.
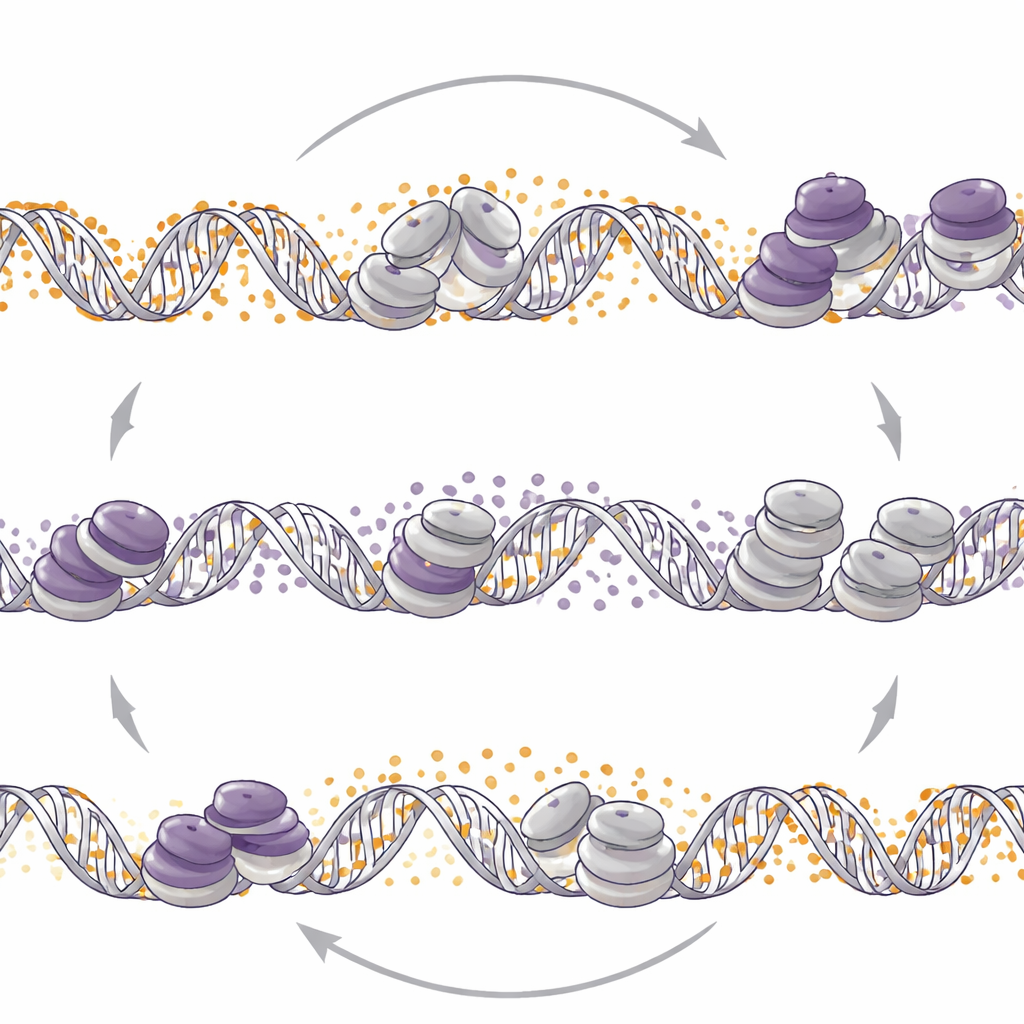
Att växla det andra reglaget omformar kontrollen
Forskarna frågade sedan om det omvända också var sant: om förändring av DNA‑metylering ompositionerar EZH2‑märken? När de tog bort DNMT1 eller använde det DNA‑metyleringssänkande läkemedlet decitabin i neuroendokrina modeller såg de en bred omfördelning av H3K27me3 över genomet. I dessa tumörer ledde minskad DNA‑metylering till mer H3K27me3 vid vissa beredda promotors, förlust av ett aktiverande histonmärke och reducerad aktivitet hos neuroendokrina gener. I kontrast, i en prostatacarcinom‑cellinje minskade förlust av DNMT1 H3K27me3 vid liknande beredda regioner och ökade det aktiverande märket, vilket frigjorde neuroendokrina relaterade gener. Således kan samma molekylära knuff — försvagning av DNMT1 — antingen dämpa eller tända neuroendokrina program beroende på tumörens kontext.
Vad detta betyder för framtida behandlingar
Tillsammans visar dessa experiment att DNA‑metylering och EZH2‑driven histonmärkning beter sig som två samordnade bromsar som kan byta plats för att hålla viktiga gener tysta eller i beredskap, vilket hjälper prostatatumörer att byta identitet och motstå behandling. Att störa endast ett system utlöser ofta kompensatoriska förändringar i det andra, vilket kan begränsa den varaktiga nyttan av läkemedel som riktar sig enbart mot EZH2 eller DNA‑metylering. Arbetet antyder att noggrant utformade strategier som tar hänsyn till detta molekylära dragkamp — potentiellt inklusive kombinations‑ eller tidsbestämd användning av båda typerna av epigenetiska läkemedel — en dag kan erbjuda bättre sätt att förebygga eller behandla de mest aggressiva, terapiresistenta formerna av prostatacancer.
Citering: Singh, R., Venkadakrishnan, V.B., Imada, E. et al. Crosstalk between EZH2 and DNA methylation mediates neuroendocrine prostate cancer lineage plasticity. Nat Commun 17, 2992 (2026). https://doi.org/10.1038/s41467-026-69308-0
Nyckelord: prostatacancer, neuroendokrina tumörer, epigenetik, DNA‑metylering, EZH2