Clear Sky Science · pl
Interakcja między EZH2 a metylacją DNA pośredniczy w plastyczności linii komórkowej w neuroendokrynnej raku prostaty
Dlaczego tożsamość komórek nowotworowych ma znaczenie
Guzy prostaty nie zawsze pozostają takie same w czasie. Niektóre początkowo zależą od hormonów męskich i odpowiadają na standardowe leczenie, lecz później przechodzą w znacznie agresywniejszą postać zwaną neuroendokrynnym rakiem prostaty. Ta zdolność do zmiany kształtu — nazywana plastycznością linii komórkowej — pomaga nowotworom unikać terapii i jest główną przyczyną niepowodzeń leczenia. Przedstawione tu badanie analizuje, jak dwa chemiczne „wyłączniki” działające na DNA i jego opakowanie współpracują, by kontrolować tę niebezpieczną zmianę tożsamości, oraz jak zablokowanie jednego wyłącznika może spowodować kompensację przez drugi.
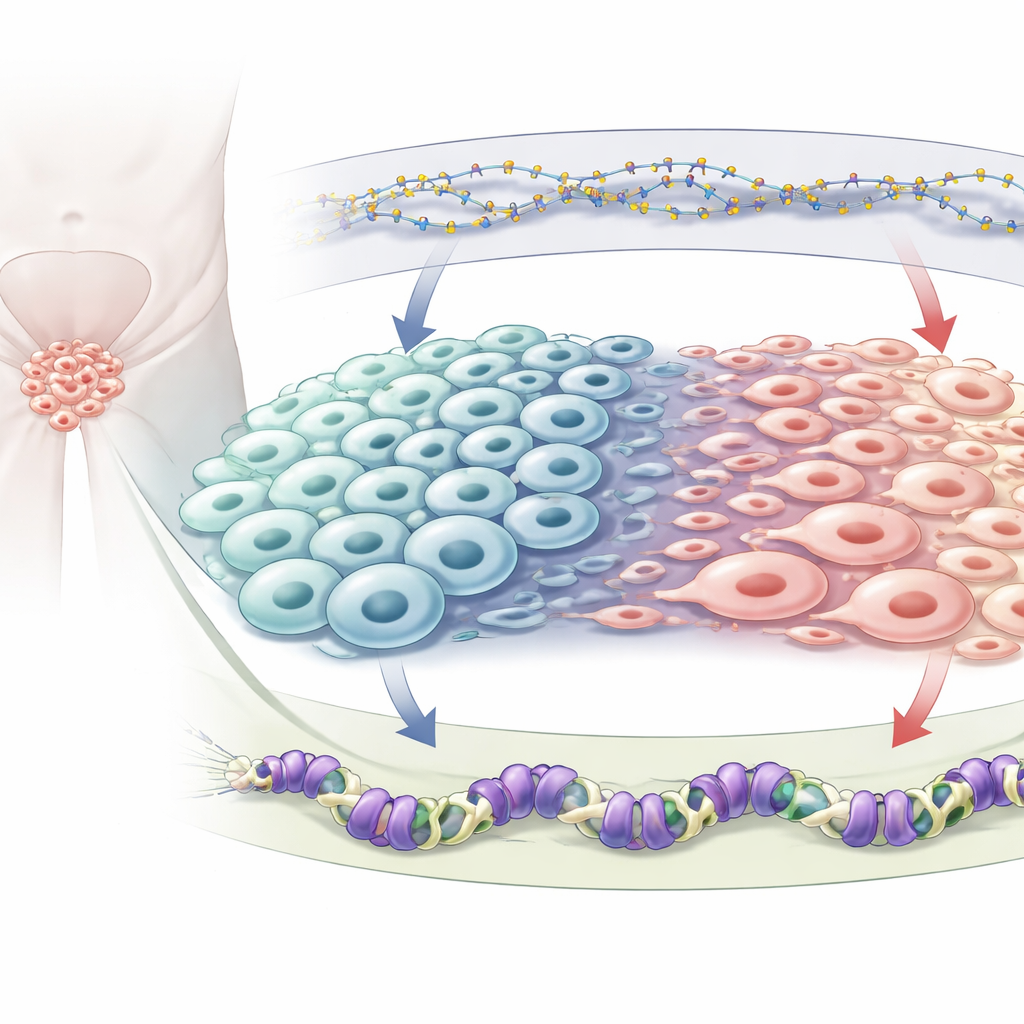
Dwa chemiczne hamulce genomu
Każda komórka zawiera te same geny, ale chemiczne znaczniki decydują, które z nich są włączone lub wyłączone. Autorzy koncentrują się na dwóch typach represyjnych znaczników. Jeden to metylacja DNA, w której małe grupy chemiczne są dodawane bezpośrednio do DNA i zwykle wyciszają pobliskie geny; proces ten podtrzymuje enzym zwany DNMT1. Drugi to znacznik H3K27me3, umieszczany na białkach owijających DNA i nanoszony przez białko EZH2, będące częścią kompleksu represyjnego Polycomb 2. Oba systemy wiadomo, że zmieniają się w przebiegu raka prostaty, szczególnie gdy guzy stają się neuroendokrynne, lecz nie było jasne, jak wzajemnie na siebie wpływają i wspólnie kierują tożsamością komórkową.
Wzorce oznaczające agresywne guzy prostaty
Wykorzystując genetycznie zmodyfikowane myszy, próbki guzów od pacjentów i miniaturowe guzy hodowane w laboratorium, badacze porównali typowego kastracjiopornego gruczolakoraka prostaty z neuroendokrynnym rakiem prostaty. Stwierdzili powtarzalne przesunięcia w metylacji DNA między tymi dwoma stanami: setki regionów genomu straciły metylację, podczas gdy inne zyskały ją. Co zaskakujące, regiony, które stały się mniej metylowane w guzach neuroendokrynnych, często akumulowały więcej znacznika powiązanego z EZH2 — H3K27me3 — mimo że te dwa represyjne systemy były zwykle postrzegane jako wzajemnie wykluczające się. Wiele z tych regionów leżało blisko genów związanych z cechami neuronopodobnymi oraz tzw. promotorów bivalencyjnych, które utrzymują geny rozwojowe w stanie przygotowania do szybkiego włączenia lub wyłączenia.
Co się dzieje, gdy jeden hamulec zostaje zwolniony
Aby zbadać zależności przyczynowo‑skutkowe, zespół wyłączył EZH2 w modelach mysich predysponowanych do przechodzenia w guzy neuroendokrynne, a oddzielnie zastosował lek hamujący EZH2 w organoidach pochodzących od pacjentów. W obu ustawieniach globalny krajobraz metylacji DNA uległ gruntownemu przekształceniu. Regiony wcześniej celowane przez EZH2 często stały się bardziej metylowane, podczas gdy inne odcinki straciły metylację i uruchomiły geny powiązane z różnicowaniem neuronowym oraz znane sygnatury neuroendokrynne. Innymi słowy, usunięcie hamulca opartego na H3K27me3 pozwoliło systemowi metylacji DNA wejść na scenę i utrzymać wyciszenie wielu tych samych genów, jednocześnie poluzowując kontrolę w innych miejscach, co wzmacnia stan neuroendokrynny.
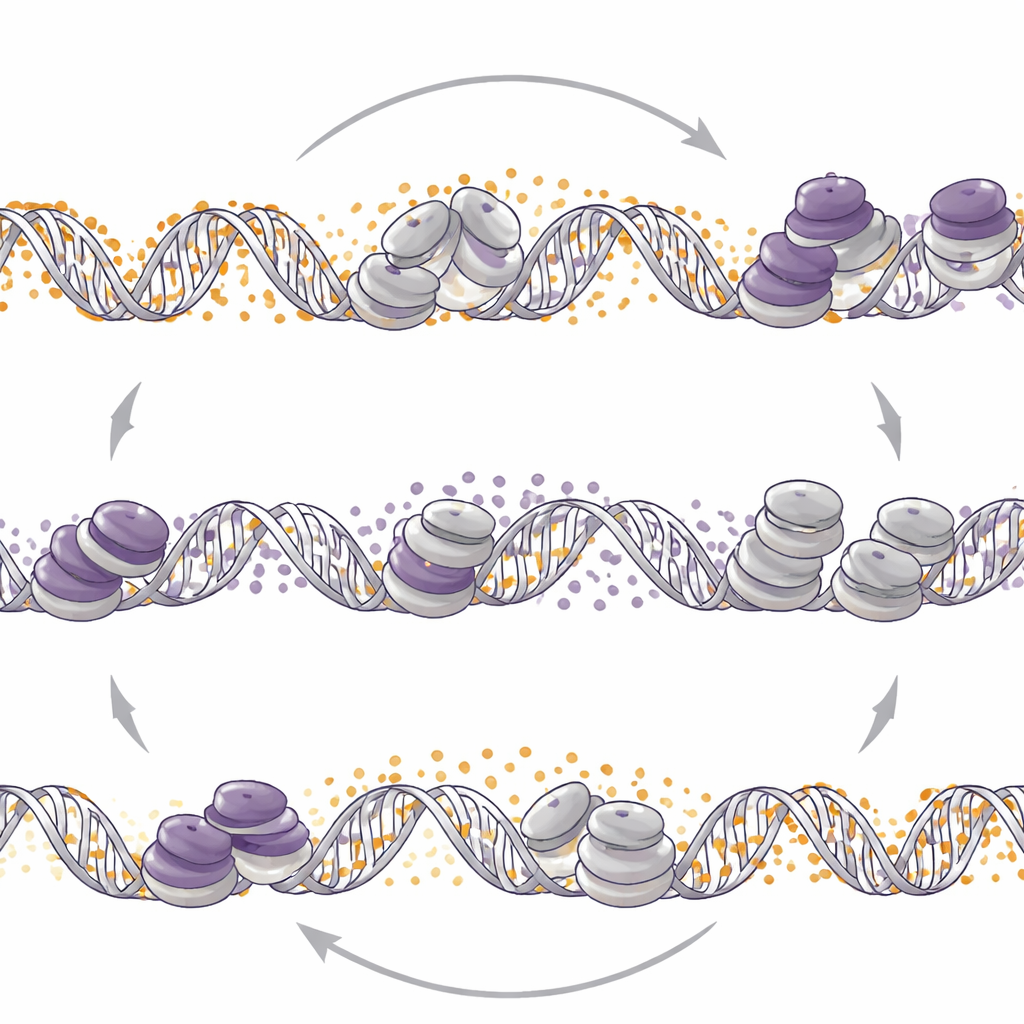
Przełączenie drugiego wyłącznika zmienia kontrolę
Naukowcy zapytali następnie, czy działa to w drugą stronę: czy zmiana metylacji DNA przemieszcza znaczniki EZH2? Kiedy usunęli DNMT1 lub zastosowali lek obniżający metylację DNA — decytabinę — w modelach neuroendokrynnych, zaobserwowali szeroką redystrybucję H3K27me3 w całym genomie. W tych guzach zmniejszenie metylacji DNA prowadziło do wzrostu H3K27me3 przy pewnych promotorach w stanie gotowości, utraty aktywującego znacznika histonowego i zmniejszenia aktywności genów neuroendokrynnych. W przeciwieństwie do tego, w linii komórkowej gruczolakoraka prostaty utrata DNMT1 zmniejszała H3K27me3 w podobnych regionach w stanie gotowości i zwiększała znacznik aktywujący, uwalniając geny związane z programami neuroendokrynnymi. Zatem ten sam molekularny impuls — osłabienie DNMT1 — może albo stłumić, albo zapalić programy neuroendokrynne, zależnie od kontekstu guza.
Co to oznacza dla przyszłych terapii
Razem te eksperymenty pokazują, że metylacja DNA i znaczniki histonowe napędzane przez EZH2 zachowują się jak dwa skoordynowane hamulce, które mogą się wymieniać rolami, aby utrzymywać krytyczne geny w stanie wyciszenia lub gotowości, pomagając guzom prostaty zmieniać tożsamość i opierać się terapii. Zakłócenie jednego systemu samo w sobie często wywołuje kompensacyjne zmiany w drugim, co może ograniczać trwały efekt leków celujących wyłącznie EZH2 lub metylację DNA. Praca sugeruje, że starannie zaprojektowane strategie uwzględniające tę molekularną przeciąganie liny — potencjalnie obejmujące terapię skojarzoną lub czasowane użycie obu typów leków epigenetycznych — mogłyby pewnego dnia zaoferować lepsze sposoby zapobiegania lub leczenia najbardziej agresywnych, opornych na leczenie postaci raka prostaty.
Cytowanie: Singh, R., Venkadakrishnan, V.B., Imada, E. et al. Crosstalk between EZH2 and DNA methylation mediates neuroendocrine prostate cancer lineage plasticity. Nat Commun 17, 2992 (2026). https://doi.org/10.1038/s41467-026-69308-0
Słowa kluczowe: rak prostaty, guzy neuroendokrynne, epigenetyka, metylacja DNA, EZH2