Clear Sky Science · zh
GluA4 AMPA 受体激活与构象可塑性的结构基础
为何这种脑通道重要
你体内的每一次思考、记忆和运动都依赖于在神经元之间传递的微弱电信号。许多此类信号由 AMPA 受体承载,这些分子“闸门”在感知到神经递质谷氨酸时开启。本研究聚焦于一种罕见的闸门变体,称为 GluA4,它在快速放电的神经元和小脑中特别集中。由于 GluA4 的改变与癫痫、智力障碍甚至脑肿瘤有关,理解该受体在原子水平上的工作方式可能揭示其强大功能的原因——以及未来药物如何针对它。
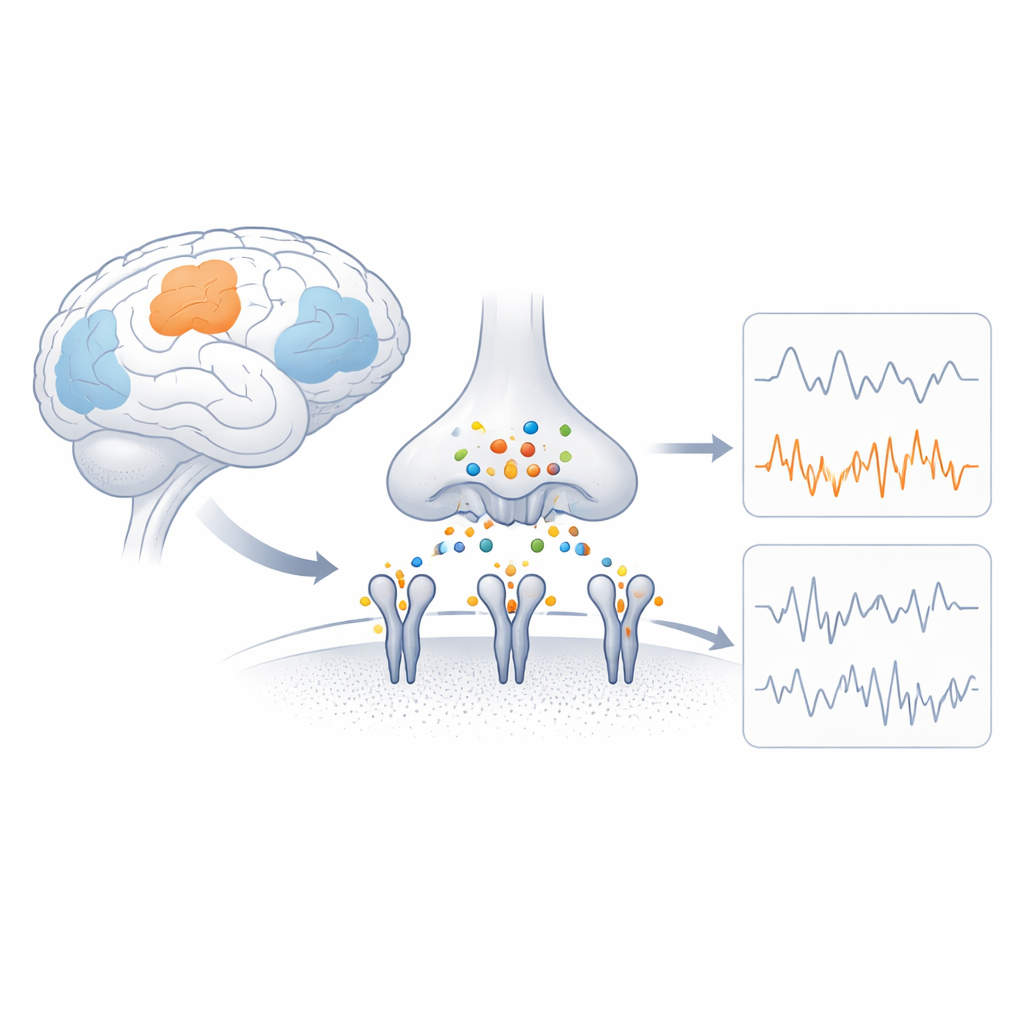
大脑的快速开关
AMPA 受体是位于神经元膜上的蛋白复合体,它们通过允许带电粒子流动,将化学信号转换为电流。每个受体由四个相关亚基组成,亚基的组合决定通道开启速度、电流大小以及钙是否能进入。GluA4 是一种透钙亚基,在某些特定细胞类型(如阳性钙结合蛋白抑制性神经元及某些听觉和小脑神经元)中异常丰富。遗传学研究表明,GluA4 基因的损伤性变化可导致癫痫和认知问题,这提示其特殊特性对脑功能至关重要,但其结构机制一直未被阐明。
捕捉 GluA4 的工作瞬间
为揭示 GluA4 的运作方式,研究者使用了冷冻电子显微镜,这是一种可在近原子分辨率下成像闪冻分子的技术。他们纯化了完全由 GluA4 组成且与一个称为 TARPγ2 的辅助伴侣蛋白紧密结合的受体,该蛋白在大脑中自然与 GluA4 结合并调节其行为。团队用谷氨酸和一种阻止通道失活的药物将受体锁定在活性、非脱敏状态。来自人工膜的电生理记录证实,这些纯化复合体表现得像真实的 AMPA 受体,产生短时与长时开启,且具有多个电流水平。
既灵活又完整的构象
结构图谱显示,GluA4 受体保持了其他 AMPA 受体中常见的经典 Y 形布局:位于细胞外的顶部“头部”区域感知谷氨酸,下方的核心形成穿过膜的离子通道。最上层的氨基末端结构域出人意料地具有高度可动性,能采纳多种不同位置,同时仍维持将四个亚基连结在一起的关键接触。这表明 GluA4 的外部支架虽然完整,但高度柔性,可能允许它在不同脑区与多样的伴侣蛋白相互作用而不解体。
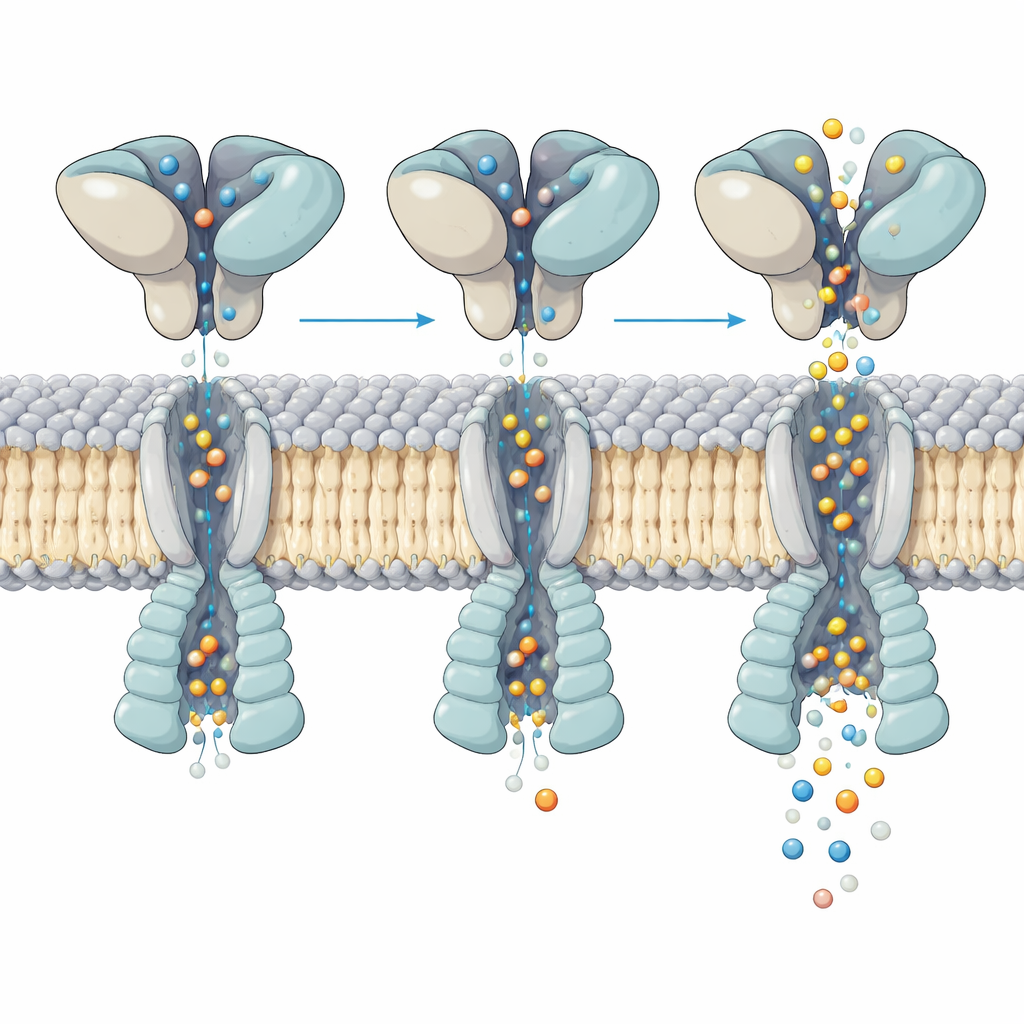
构象变化如何控制离子流
对激活态通道的细致观察揭示了位于上方的谷氨酸结合层的运动如何被传递为下方孔道的开启。四个结合口都充满了谷氨酸,但组成闸门的螺旋在四个亚基间以不均匀、非对称的方式弯曲。通过分析数十万颗粒,团队解析出同一激活受体的五个不同“亚态”。在每个亚态中,上层结构相对膜核心略有摇摆与扭转,这种小幅重排改变了孔道中关键螺旋弯曲的位置与强度。这些细微差异改变了孔道在关键点的宽度,与单通道记录中观察到的多个电导水平相对应,即便谷氨酸占位相同。
将结构与疾病相关变体联系起来
该研究确定了孔道形成螺旋中一段高度保守短序列中的几乎每个氨基酸都能作为弯曲铰链。有几个位点正是在人类 GluA4 中发现致病突变的位置,这些突变存在于癫痫和智力障碍患者中。作者提出,这些变体可能改变螺旋弯曲的难易程度,从而改变通道开启亚水平之间的平衡或改变钙进入附近结合位点的能力。实际上,该铰链区的微小变化可能会过度或不足地调节含 GluA4 受体传递的电信号,对依赖极快、精确放电的神经回路产生重大影响。
这对大脑健康的意义
通过显示 GluA4 在结构上既稳定又具有异常的构象可塑性,这项工作重新构架了科学家对 AMPA 受体功能的理解。与其把不同电流水平仅仅视为谷氨酸分子占位多少的结果,不如将所见解读为:即便受体被充分装载,也仍能取样多种构象,每种构象对应不同的孔道开启程度。这种“构象可塑性”为 GluA4 通道的分级响应提供了结构学解释,也提示药物或伴侣蛋白可能通过何种方式调节其活性。从长远看,描绘这些微观形变或能为以 GluA4 为关键因子的疾病(从某些癫痫到精神病和与癌症相关的脑信号改变)提供治疗方向。
引用: Hale, W.D., Wang, H., Huganir, R.L. et al. Structural basis for activation and conformational plasticity of the GluA4 AMPA receptor. Nat Commun 17, 2932 (2026). https://doi.org/10.1038/s41467-026-68953-9
关键词: AMPA 受体, GluA4, 突触传递, 冷冻电子显微镜, 离子通道门控