Clear Sky Science · de
Strukturelle Grundlage für Aktivierung und konformationelle Plastizität des GluA4‑AMPA‑Rezeptors
Warum dieser Gehirnkanal wichtig ist
Jeder Gedanke, jede Erinnerung und jede Bewegung Ihres Körpers beruht auf winzigen elektrischen Signalen, die zwischen Nervenzellen übertragen werden. Viele dieser Signale werden von AMPA‑Rezeptoren getragen, molekularen „Toren“, die sich öffnen, wenn sie den Botenstoff Glutamat erkennen. Diese Studie konzentriert sich auf eine seltene Variante dieses Tores, genannt GluA4, die in schnell feuernden Nervenzellen und im Kleinhirn besonders stark vorkommt. Da Veränderungen in GluA4 mit Epilepsie, geistiger Behinderung und sogar Hirntumoren in Verbindung gebracht wurden, könnte das Verständnis, wie dieser Rezeptor auf atomarer Ebene funktioniert, erklären, warum er so wirkungsvoll ist — und wie er möglicherweise von künftigen Medikamenten gezielt beeinflusst werden kann.
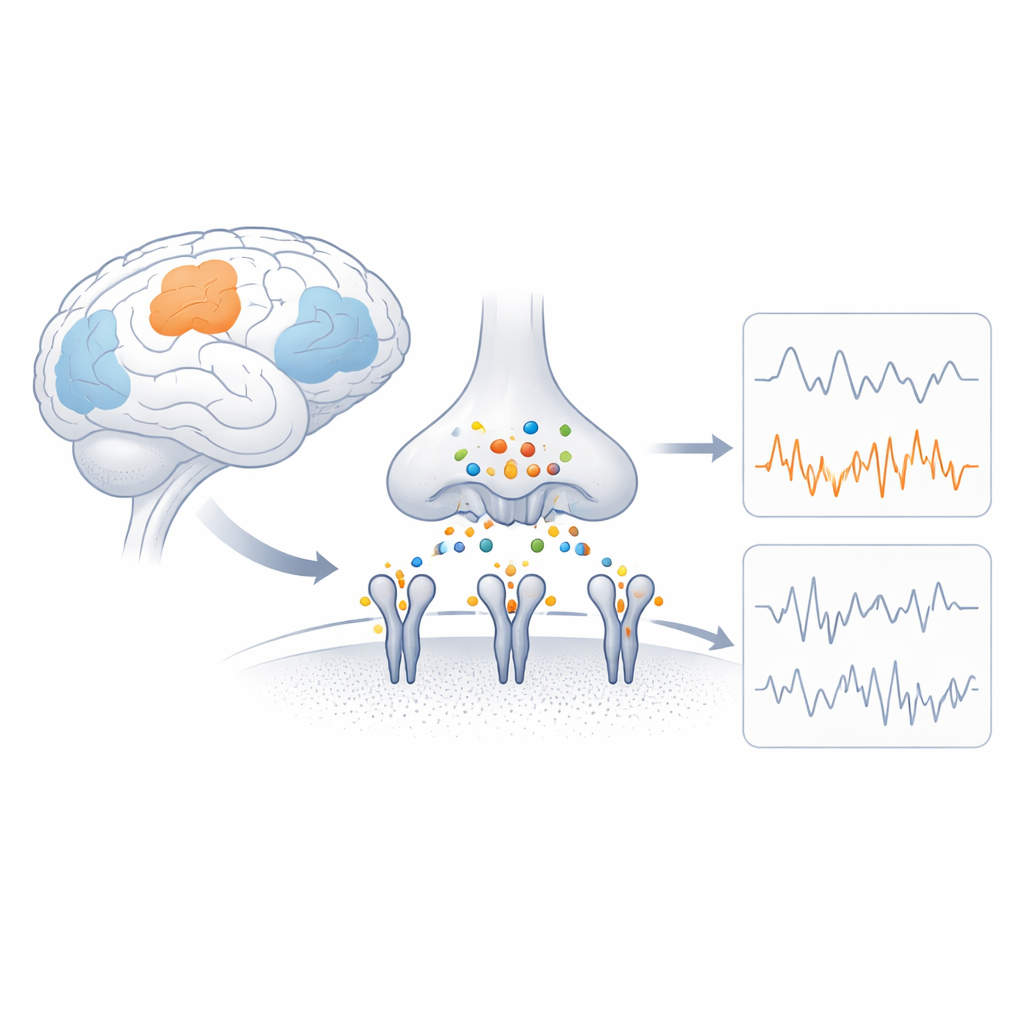
Die schnellen Schalter des Gehirns
AMPA‑Rezeptoren sind Proteinkomplexe in der Membran von Nervenzellen, die ein chemisches Signal in einen elektrischen Strom umwandeln, indem sie geladene Teilchen durchlassen. Jeder Rezeptor besteht aus vier verwandten Teilen (Untereinheiten), und die Zusammensetzung dieser Untereinheiten bestimmt, wie schnell der Kanal öffnet, wie viel Strom fließt und ob Calcium eindringen kann. GluA4 ist eine calciumdurchlässige Untereinheit, die in bestimmten Zelltypen ungewöhnlich häufig vorkommt, etwa in parvalbuminpositiven Inhibitionsneuronen sowie in bestimmten auditorischen und kleinhirnartigen Neuronen. Genetische Studien zeigen, dass schädigende Veränderungen im GluA4‑Gen Krampfanfälle und kognitive Probleme auslösen können, was darauf hinweist, dass seine besonderen Eigenschaften für die Gehirnfunktion entscheidend sind, obwohl seine Struktur bislang rätselhaft blieb.
GluA4 in Aktion einfangen
Um zu zeigen, wie GluA4 arbeitet, nutzten die Forscher Cryo‑Elektronenmikroskopie, eine Technik, die blitzgefrostete Moleküle mit nahezu atomarer Auflösung abbildet. Sie reinigten Rezeptoren, die ausschließlich aus GluA4 bestanden und fest mit einem Hilfsprotein namens TARPγ2 verbunden waren, das natürlicherweise mit GluA4 im Gehirn assoziiert und dessen Verhalten feinjustiert. Das Team brachte die Rezeptoren in einen aktiven, nicht desensibilisierten Zustand, indem sie Glutamat zusammen mit einem Wirkstoff verwendeten, der das Schließen des Kanals verhindert. Elektrische Messungen an künstlichen Membranen bestätigten, dass diese gereinigten Komplexe wie echte AMPA‑Rezeptoren funktionierten und kurz- sowie lang andauernde Öffnungen mit mehreren Stromstufen zeigten.
Eine flexible, aber intakte Architektur
Die Strukturbilder zeigten, dass GluA4‑Rezeptoren die klassische Y‑förmige Anordnung anderer AMPA‑Rezeptoren bewahren: eine obere „Kopf“region außerhalb der Zelle, die Glutamat erkennt, und einen unteren Kern, der den Ionenkanal durch die Membran bildet. Die oberste Schicht, die Aminoterminaldomäne, erwies sich als überraschend beweglich und nahm viele verschiedene Positionen ein, während sie dennoch die entscheidenden Kontakte bewahrte, die die vier Untereinheiten zusammenhalten. Das zeigt, dass das äußere Gerüst von GluA4 intakt, aber hochflexibel ist — möglicherweise erlaubt dies Interaktionen mit verschiedenartigen Partnerproteinen in unterschiedlichen Hirnregionen, ohne auseinanderzufallen.
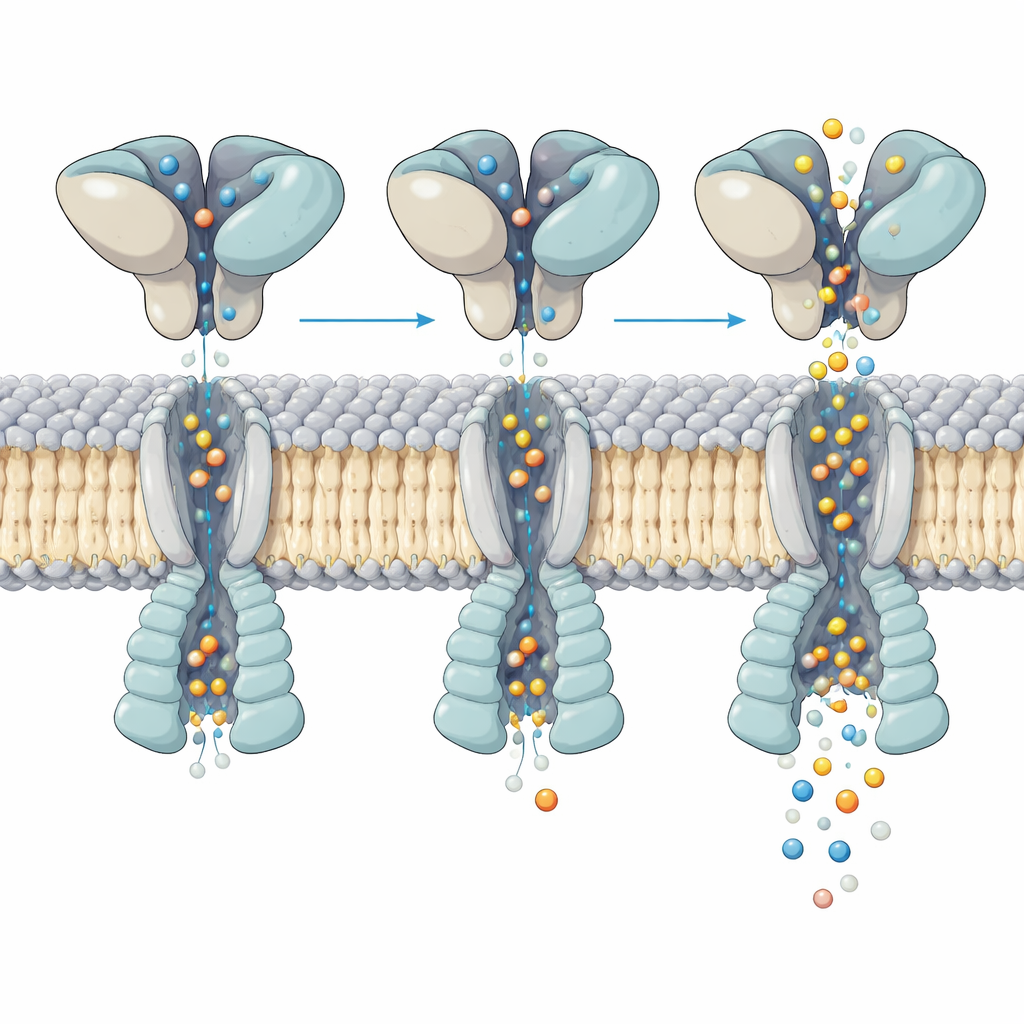
Wie Formwechsel den Ionenfluss steuern
Eine genauere Untersuchung des aktiven Kanals legte offen, wie Bewegungen in der Glutamatbindeschicht darüber in das Öffnen der Pore darunter übersetzt werden. Alle vier Bindetaschen waren mit Glutamat gefüllt, dennoch bogen sich die Helices, die das Tor bilden, ungleichmäßig und asymmetrisch über die vier Untereinheiten hinweg. Durch die Analyse von Hunderttausenden Partikeln löste das Team fünf verschiedene „Subzustände“ desselben aktivierten Rezeptors auf. In jedem Subzustand schaukeln und verdrehen sich die oberen Domänen leicht gegenüber dem Membrankern, und diese kleine Umordnung verschiebt, wo und wie stark sich Schlüsselhelices innerhalb der Pore knicken. Diese subtilen Unterschiede verändern die Breite der Pore an kritischen Stellen und entsprechen den mehreren Leitfähigkeitsstufen, die in Einzelkanalaufzeichnungen beobachtet werden, obwohl die Glutamat‑Belegung gleich bleibt.
Verknüpfung von Struktur mit krankheitsrelevanten Varianten
Die Studie identifiziert nahezu jede Aminosäure in einem kurzen, hochkonservierten Abschnitt der porebildenden Helix als potenzielle Biegeachse. Mehrere dieser Positionen sind genau die Stellen, an denen krankheitsverursachende Mutationen im menschlichen GluA4 bei Patienten mit Epilepsie und geistiger Behinderung gefunden wurden. Die Autoren schlagen vor, dass diese Varianten wahrscheinlich verändern, wie leicht die Helix knickt, wodurch das Gleichgewicht zwischen den Unterstufen der Kanalöffnung verschoben oder der Zugang von Calcium zu einer benachbarten Bindungsstelle verändert wird. Im Effekt könnten winzige Veränderungen in dieser Scharnierzone das elektrische Signal von GluA4‑enthaltenden Rezeptoren über- oder unterstimmen — mit weitreichenden Folgen für neuronale Schaltkreise, die auf extrem schnelles, präzises Feuern angewiesen sind.
Was das für die Gehirngesundheit bedeutet
Indem gezeigt wird, dass GluA4 sowohl strukturell stabil als auch ungewöhnlich formflexibel ist, rückt diese Arbeit die Sichtweise auf AMPA‑Rezeptorfunktion neu. Anstatt unterschiedliche Stromstufen nur als Folge der Anzahl gebundener Glutamatmoleküle zu sehen, unterstützen die Ergebnisse ein Bild, in dem ein voll besetzter Rezeptor weiterhin mehrere Konformationen durchlaufen kann, jede mit einer charakteristischen Porenöffnung. Diese „konformationelle Plastizität“ liefert eine strukturelle Erklärung für die abgestuften Antworten von GluA4‑Kanälen und deutet auf neue Wege hin, wie Medikamente oder Partnerproteine deren Aktivität modulieren könnten. Langfristig könnte die Kartierung dieser mikroskopischen Formänderungen Therapien leiten für Erkrankungen, bei denen GluA4 eine Schlüsselrolle spielt — von bestimmten Epilepsien bis zu Schaltkreisveränderungen bei psychiatrischen Erkrankungen und krebsbedingter Gehirnsignalisierung.
Zitation: Hale, W.D., Wang, H., Huganir, R.L. et al. Structural basis for activation and conformational plasticity of the GluA4 AMPA receptor. Nat Commun 17, 2932 (2026). https://doi.org/10.1038/s41467-026-68953-9
Schlüsselwörter: AMPA‑Rezeptor, GluA4, synaptische Übertragung, Cryo‑Elektronenmikroskopie, Ionenkanal‑Gating