Clear Sky Science · pt
Base estrutural para ativação e plasticidade conformacional do receptor AMPA GluA4
Por que esse canal cerebral importa
Cada pensamento, memória e movimento no seu corpo depende de minúsculos sinais elétricos que passam entre células nervosas. Muitos desses sinais são conduzidos por receptores AMPA, “portões” moleculares que se abrem quando detectam o mensageiro químico glutamato. Este estudo foca em uma versão rara desse portão, chamada GluA4, que se concentra em células cerebrais de disparo rápido e no cerebelo. Como alterações em GluA4 foram ligadas a epilepsia, deficiência intelectual e até tumores cerebrais, entender como esse receptor funciona em nível atômico pode revelar por que ele é tão potente — e como poderia ser alvo de medicamentos futuros.
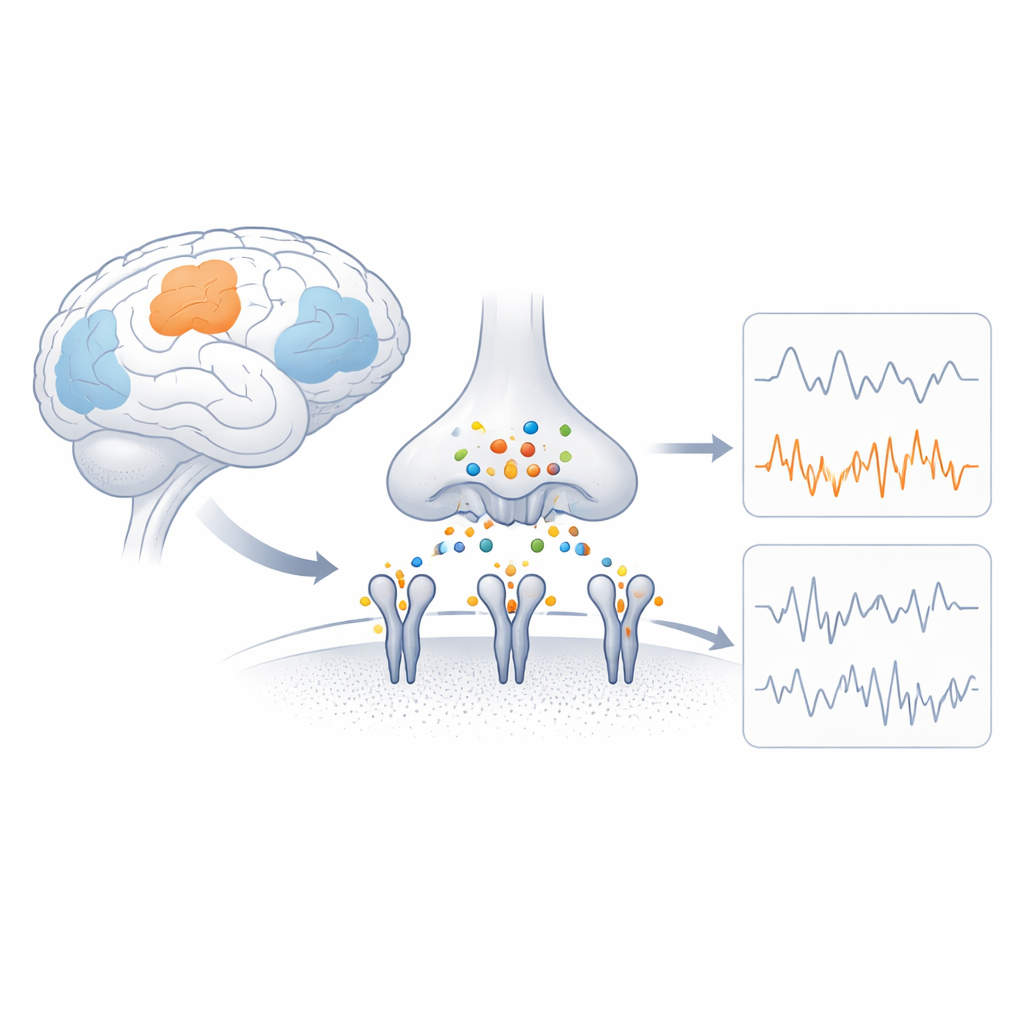
Os interruptores rápidos do cérebro
Receptores AMPA são complexos proteicos que se assentam na membrana das células nervosas e convertem um sinal químico em uma corrente elétrica permitindo o fluxo de partículas carregadas. Cada receptor é formado por quatro partes relacionadas (subunidades), e a combinação dessas subunidades determina quão rapidamente o canal se abre, quanta corrente passa e se o cálcio pode entrar. GluA4 é uma subunidade permeável ao cálcio que é extraordinariamente abundante em tipos celulares específicos, como neurônios inibitórios positivos para parvalbumina e certos neurônios auditivos e cerebelares. Estudos genéticos mostram que alterações prejudiciais no gene de GluA4 podem causar convulsões e problemas cognitivos, sugerindo que suas propriedades especiais são cruciais para a função cerebral, embora sua estrutura tivesse permanecido misteriosa.
Capturando o GluA4 em ação
Para revelar como o GluA4 opera, os pesquisadores utilizaram crio‑microscopia eletrônica, uma técnica que imagem moléculas congeladas rapidamente em resolução quase atômica. Eles purificaram receptores compostos inteiramente por GluA4 e fortemente associados a uma proteína parceira auxiliar chamada TARPγ2, que naturalmente se liga ao GluA4 no cérebro e ajuda a ajustar seu comportamento. A equipe travou os receptores em um estado ativo e não dessensibilizado usando glutamato junto com um fármaco que impede o fechamento do canal. Registros elétricos em membranas artificiais confirmaram que esses complexos purificados se comportavam como receptores AMPA reais, produzindo aberturas breves e longas com múltiplos níveis de corrente.
Uma arquitetura flexível, porém intacta
Os mapas estruturais revelaram que os receptores GluA4 mantêm o arranjo clássico em Y observado em outros receptores AMPA: uma região superior em forma de “cabeça” fora da célula que detecta o glutamato, e um núcleo inferior que forma o canal iônico através da membrana. A camada mais externa, chamada domínio amino terminal, mostrou‑se surpreendentemente móvel, adotando diversas posições diferentes enquanto ainda preservava contatos-chave que mantêm as quatro subunidades unidas. Isso mostra que a estrutura externa do GluA4 está intacta, mas altamente flexível, possivelmente permitindo interações com diversos parceiros proteicos em diferentes regiões do cérebro sem se desmontar.
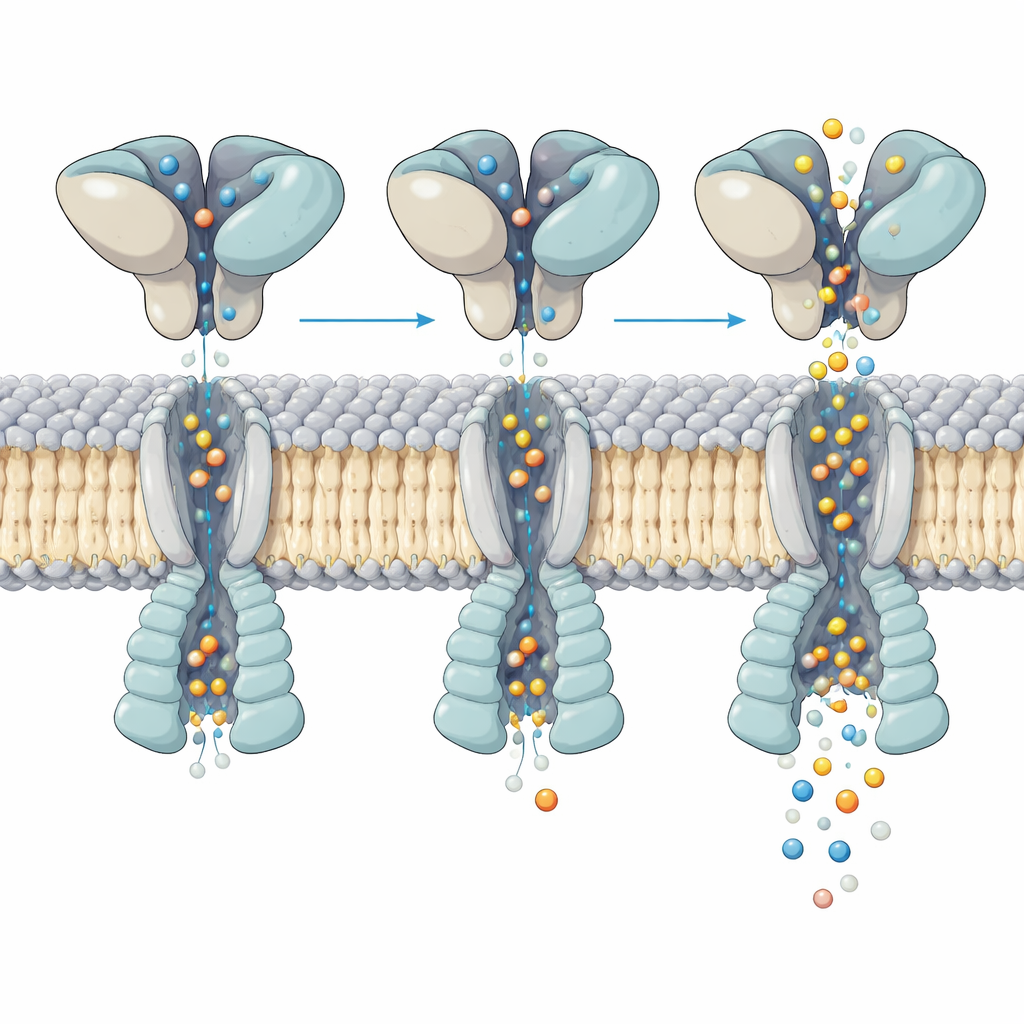
Como a mudança de forma controla o fluxo de íons
Uma inspeção mais detalhada do canal ativo revelou como o movimento na camada de ligação ao glutamato acima é traduzido na abertura do poro abaixo. Os quatro bolsões de ligação estavam preenchidos com glutamato, porém as hélices que formam o portão se dobraram de maneira desigual e assimétrica entre as quatro subunidades. Ao analisar centenas de milhares de partículas, a equipe resolveu cinco “subestados” distintos do mesmo receptor ativado. Em cada subestado, os domínios superiores oscilaram e torceram ligeiramente em relação ao núcleo da membrana, e esse pequeno rearranjo deslocou onde e com que intensidade hélices-chave formam uma curvatura dentro do poro. Essas diferenças sutis alteram a largura do poro em pontos críticos, correspondendo aos múltiplos níveis de condutância observados em registros de canal único, mesmo que a ocupação por glutamato seja a mesma.
Ligando a estrutura a variantes relacionadas a doenças
O estudo identifica quase todos os aminoácidos em um trecho curto e altamente conservado da hélice formadora do poro como capazes de servir de dobradiça para a curvatura. Várias dessas posições coincidem com mutações causadoras de doenças em GluA4 humano encontradas em pacientes com epilepsia e deficiência intelectual. Os autores propõem que essas variantes provavelmente alteram a facilidade com que a hélice pode se dobrar, deslocando o equilíbrio entre subníveis de abertura do canal ou mudando o acesso do cálcio a um sítio de ligação próximo. Em efeito, pequenas alterações nessa zona de dobradiça podem super‑ ou subajustar o sinal elétrico conduzido por receptores contendo GluA4, com grandes consequências para circuitos neurais que dependem de disparos extremamente rápidos e precisos.
O que isso significa para a saúde cerebral
Ao mostrar que o GluA4 é estruturalmente estável e extraordinariamente flexível em forma, este trabalho reframes a forma como os cientistas pensam sobre a função dos receptores AMPA. Em vez de ver diferentes níveis de corrente apenas como resultado do número de moléculas de glutamato ligadas, os achados apoiam uma visão na qual um receptor totalmente carregado ainda pode explorar múltiplas conformações, cada uma com uma abertura de poro distinta. Essa “plasticidade conformacional” fornece uma explicação estrutural para as respostas graduadas dos canais GluA4 e sugere novas maneiras pelas quais fármacos ou proteínas parceiras podem ajustar sua atividade. A longo prazo, mapear essas mudanças microscópicas de forma pode orientar terapias para transtornos em que o GluA4 é um ator-chave — desde certas epilepsias até alterações de circuito em doenças psiquiátricas e sinalização cerebral relacionada ao câncer.
Citação: Hale, W.D., Wang, H., Huganir, R.L. et al. Structural basis for activation and conformational plasticity of the GluA4 AMPA receptor. Nat Commun 17, 2932 (2026). https://doi.org/10.1038/s41467-026-68953-9
Palavras-chave: receptor AMPA, GluA4, transmissão sináptica, crio-microscopia eletrônica, mecanismo de abertura do canal iônico