Clear Sky Science · nl
Structurele basis voor activatie en conformationele plasticiteit van de GluA4 AMPA-receptor
Waarom dit hersenkanaal ertoe doet
Elke gedachte, herinnering en beweging in uw lichaam hangt af van kleine elektrische signalen die tussen zenuwcellen worden doorgegeven. Veel van die signalen worden gedragen door AMPA‑receptoren, moleculaire “poorten” die opengaan wanneer ze de chemische boodschapper glutamaat detecteren. Deze studie richt zich op een zeldzame variant van die poort, GluA4, die geconcentreerd voorkomt in snel vurende hersencellen en in het cerebellum. Omdat veranderingen in GluA4 zijn gekoppeld aan epilepsie, verstandelijke beperkingen en zelfs hersentumoren, kan inzicht in hoe deze receptor op atomair niveau werkt verklaren waarom hij zo krachtig is — en hoe hij mogelijk door toekomstige geneesmiddelen kan worden aangestuurd.
De snelle schakelaars van de hersenen
AMPA‑receptoren zijn eiwitcomplexen in het membraan van zenuwcellen die een chemisch signaal omzetten in een elektrische stroom door geladen deeltjes te laten passeren. Iedere receptor bestaat uit vier verwante onderdelen (subunits) en de samenstelling van deze subunits bepaalt hoe snel het kanaal opengaat, hoeveel stroom het doorlaat en of calcium naar binnen kan stromen. GluA4 is een calciumdoorlaatbare subunit die uitzonderlijk veel voorkomt in specifieke celtypen, zoals parvalbumine‑positieve remmende neuronen en bepaalde auditieve en cerebellaire neuronen. Genetische studies tonen dat schadelijke wijzigingen in het GluA4‑gen aanvallen en cognitieve problemen kunnen veroorzaken, wat suggereert dat de bijzondere eigenschappen ervan cruciaal zijn voor hersenfunctie maar structureel tot nu toe onbegrepen bleven.
GluA4 vastleggen in actie
Om te onthullen hoe GluA4 werkt, gebruikten de onderzoekers kryo‑elektronenmicroscopie, een techniek die ingevroren moleculen beeldt met bijna‑atomaire resolutie. Ze zuiverden receptoren die volledig uit GluA4 bestonden en nauw verbonden waren met een hulp‑eiwit genaamd TARPγ2, dat van nature met GluA4 in de hersenen samenwerkt en zijn gedrag afstemt. Het team vergrendelde de receptoren in een actieve, niet‑gedesensitiseerde toestand met glutamaat samen met een middel dat voorkomt dat het kanaal uitschakelt. Elektrische opnamen van kunstmatige membranen bevestigden dat deze gezuiverde complexen zich als echte AMPA‑receptoren gedroegen, met korte en lange openingen en meerdere stroomniveaus.
Een flexibele maar intacte architectuur
De structurele kaarten toonden aan dat GluA4‑receptoren de klassieke Y‑vormige opbouw behouden die bij andere AMPA‑receptoren is gezien: een bovenste “kop” buiten de cel die glutamaat detecteert, en een onderliggende kern die het ionkanaal door het membraan vormt. De bovenste laag, het amino‑terminaal domein genoemd, bleek verrassend mobiel en nam veel verschillende posities aan terwijl belangrijke contacten die de vier subunits bijeenhouden behouden bleven. Dit laat zien dat het buitenste geraamte van GluA4 intact maar sterk flexibel is, wat het mogelijk maakt dat het in verschillende hersengebieden met uiteenlopende partner‑eiwitten kan interageren zonder uiteen te vallen.
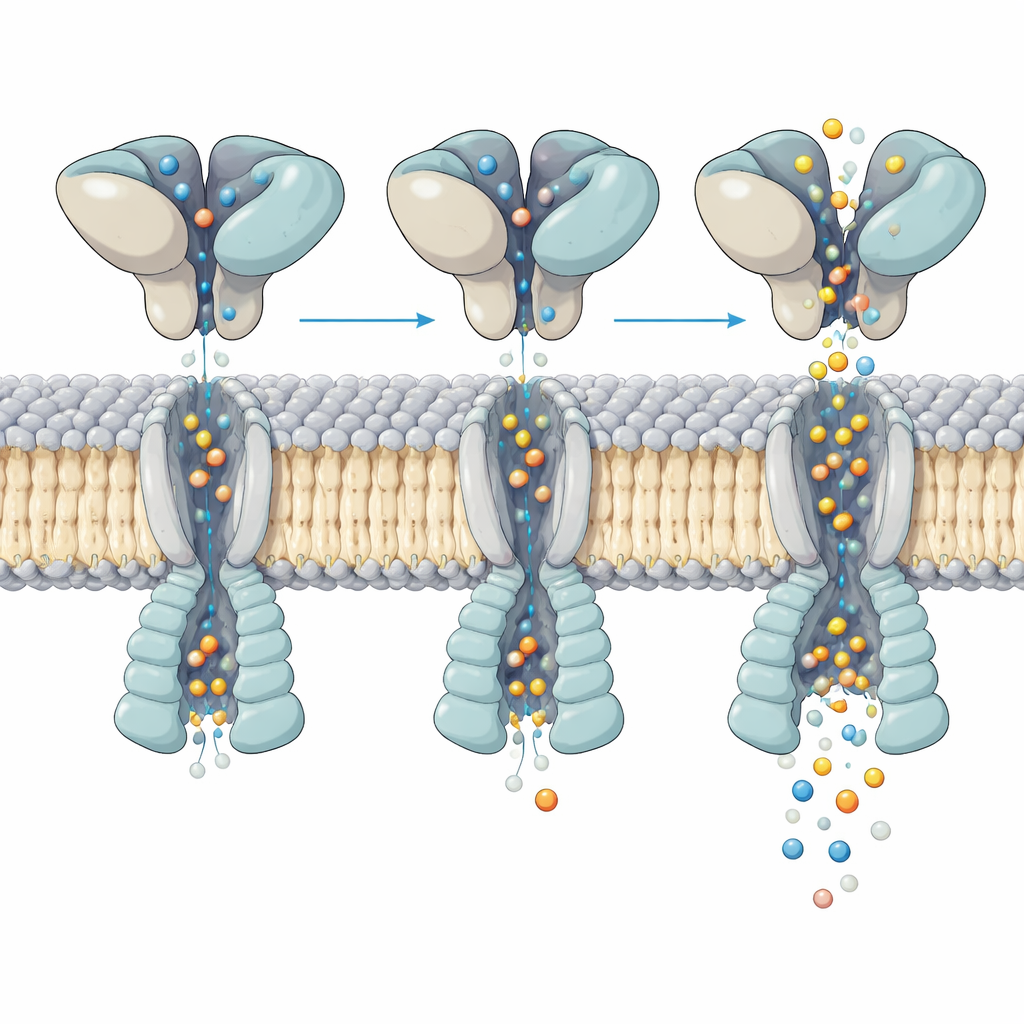
Hoe vormverandering de ionstroom regelt
Nadere bestudering van het actieve kanaal toonde hoe bewegingen in de glutamaatbindende laag erboven worden vertaald naar het openen van de porie beneden. Alle vier de bindingszakjes waren gevuld met glutamaat, maar de helixen die de poort vormen bogen op een ongelijkmatige, asymmetrische manier over de vier subunits. Door honderdduizenden deeltjes te analyseren, loste het team vijf verschillende “substaten” op van dezelfde geactiveerde receptor. In elk substaat wiebelen en draaien de bovenste domeinen licht ten opzichte van de membraankern, en deze kleine herschikking verschuift waar en hoe sterk belangrijke helixen in de porie knikken. Deze subtiele verschillen veranderen de breedte van de porie op kritieke punten, wat overeenkomt met de meerdere conductantieniveaus die in enkelkanaalopnames worden gezien, ook al is de bezetting met glutamaat hetzelfde.
Structuur koppelen aan ziektegerelateerde varianten
De studie identificeert vrijwel elk aminozuur in een korte, sterk geconserveerde sectie van de porievormende helix als potentieel draaiharnas voor buiging. Verschillende van deze posities komen precies overeen met plekken waar ziekteveroorzakende mutaties in menselijke GluA4 zijn gevonden bij patiënten met epilepsie en verstandelijke beperkingen. De auteurs stellen dat deze varianten waarschijnlijk veranderen hoe gemakkelijk de helix kan knikken, waarmee het evenwicht tussen subniveaus van kanaalopening verschuift of de toegang van calcium tot een nabijgelegen bindingsplaats verandert. In feite kunnen kleine wijzigingen in deze scharnierzone het elektrische signaal dat door GluA4‑bevatte receptoren wordt gedragen over‑ of ondertunenen, met grote gevolgen voor neurale circuits die afhankelijk zijn van extreem snelle, precieze vuring.
Wat dit betekent voor hersengezondheid
Door aan te tonen dat GluA4 zowel structureel stabiel als uitzonderlijk vorm‑flexibel is, herinterpreteert dit werk hoe wetenschappers denken over AMPA‑receptorfunctie. In plaats van verschillende stroomniveaus simpelweg toe te schrijven aan hoeveel glutamaatmoleculen gebonden zijn, ondersteunen de bevindingen een beeld waarin een volledig beladen receptor nog steeds meerdere conformaties kan aannemen, elk met een onderscheidende porie‑opening. Deze "conformationele plasticiteit" biedt een structurele verklaring voor de graduele responsen van GluA4‑kanalen en suggereert nieuwe manieren waarop geneesmiddelen of partner‑eiwitten hun activiteit kunnen bijsturen. Op de lange termijn kan het in kaart brengen van deze microscopische vormveranderingen therapieën leiden voor aandoeningen waarbij GluA4 een sleutelrol speelt — van bepaalde vormen van epilepsie tot circuitveranderingen bij psychiatrische aandoeningen en kankergerelateerde hersensignalering.
Bronvermelding: Hale, W.D., Wang, H., Huganir, R.L. et al. Structural basis for activation and conformational plasticity of the GluA4 AMPA receptor. Nat Commun 17, 2932 (2026). https://doi.org/10.1038/s41467-026-68953-9
Trefwoorden: AMPA-receptor, GluA4, synaptische transmissie, kryo-elektronenmicroscopie, ionkanaal‑gating