Clear Sky Science · it
Base strutturale per l’attivazione e la plasticità conformazionale del recettore AMPA GluA4
Perché questo canale cerebrale è importante
Ogni pensiero, memoria e movimento nel corpo dipende da minuscoli segnali elettrici che passano tra le cellule nervose. Molti di questi segnali sono trasmessi dai recettori AMPA, «porte» molecolari che si aprono quando rilevano il mediatore chimico glutammato. Questo studio si concentra su una versione rara di quella porta, chiamata GluA4, concentrata nelle cellule cerebrali a scarica rapida e nel cervelletto. Poiché alterazioni di GluA4 sono state associate a epilessia, disabilità intellettiva e perfino a tumori cerebrali, comprendere come questo recettore funzioni a livello atomico potrebbe rivelare perché è così influente — e come potrebbe essere preso di mira da farmaci futuri.
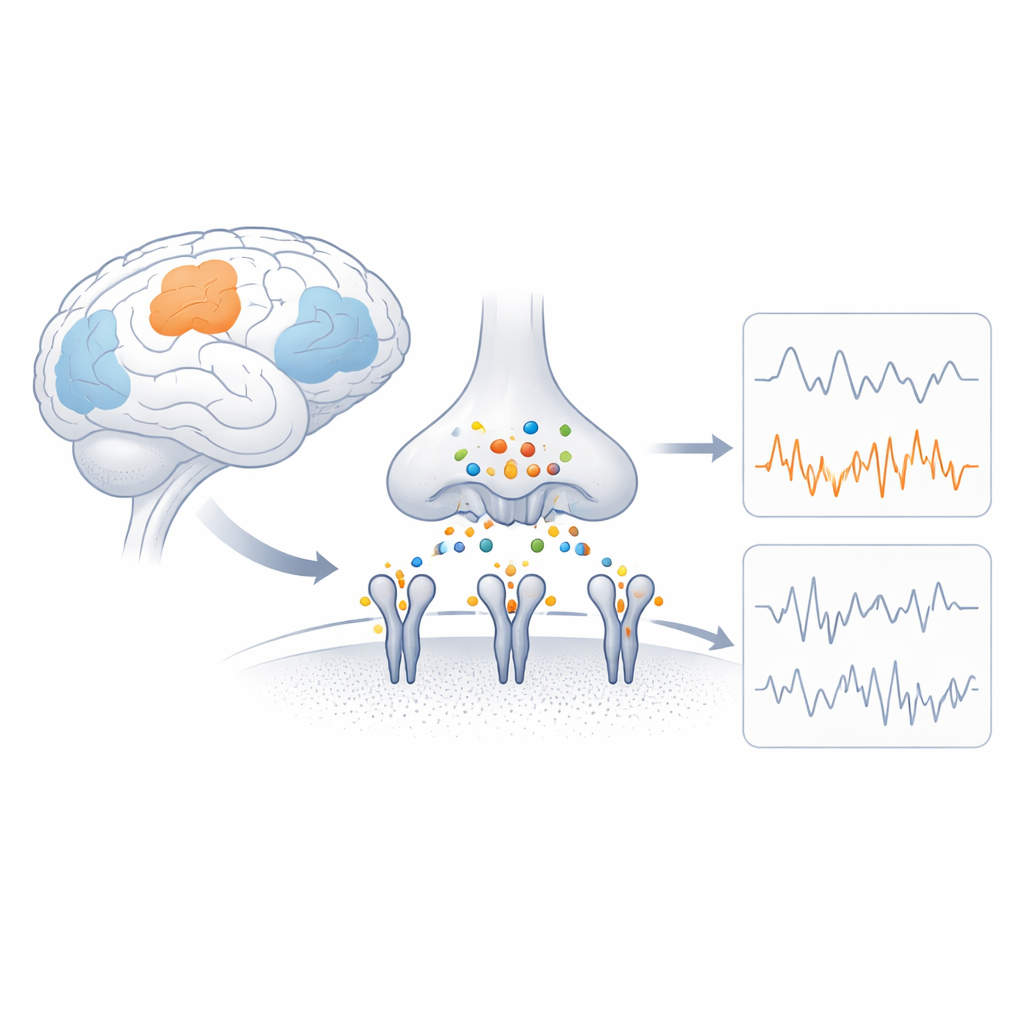
Interruttori rapidi del cervello
I recettori AMPA sono complessi proteici che si trovano nella membrana delle cellule nervose e convertono un segnale chimico in una corrente elettrica permettendo il passaggio di particelle cariche. Ogni recettore è composto da quattro parti correlate (sottounità) e la combinazione di queste sottounità determina quanto velocemente il canale si apre, quanta corrente lascia passare e se il calcio può entrare. GluA4 è una sottounità permeabile al calcio particolarmente abbondante in tipi cellulari specifici, come i neuroni inibitori parvalbumina‑positivi e alcuni neuroni uditivi e cerebellari. Studi genetici mostrano che varianti dannose nel gene di GluA4 possono causare convulsioni e problemi cognitivi, suggerendo che le sue proprietà speciali sono cruciali per la funzione cerebrale ma finora rimaste strutturalmente misteriose.
Cogliere GluA4 in azione
Per rivelare come opera GluA4, i ricercatori hanno utilizzato la crio‑microscopia elettronica, una tecnica che fotografa molecole congelate istantaneamente a risoluzione prossima all’atomica. Hanno purificato recettori composti interamente da GluA4 e strettamente associati a una proteina ausiliaria chiamata TARPγ2, che si lega naturalmente a GluA4 nel cervello e ne modula il comportamento. Il team ha bloccato i recettori in uno stato attivo non desensibilizzato usando glutammato insieme a un farmaco che impedisce al canale di chiudersi. Registrazioni elettriche su membrane artificiali hanno confermato che questi complessi purificati si comportavano come recettori AMPA reali, producendo aperture brevi e lunghe con più livelli di corrente.
Un’architettura flessibile ma integra
Le mappe strutturali hanno rivelato che i recettori GluA4 mantengono il classico schema a Y osservato in altri recettori AMPA: una regione superiore «testa» esterna alla cellula che riconosce il glutammato e un nucleo inferiore che forma il canale ionico attraverso la membrana. Lo strato più alto, chiamato dominio ammino‑terminale, si è dimostrato sorprendentemente mobile, adottando molte posizioni diverse pur mantenendo contatti chiave che tengono insieme le quattro sottounità. Questo indica che l’impalcatura esterna di GluA4 è integra ma altamente flessibile, permettendole potenzialmente di interagire con partner proteici diversi in varie regioni del cervello senza disgregarsi.
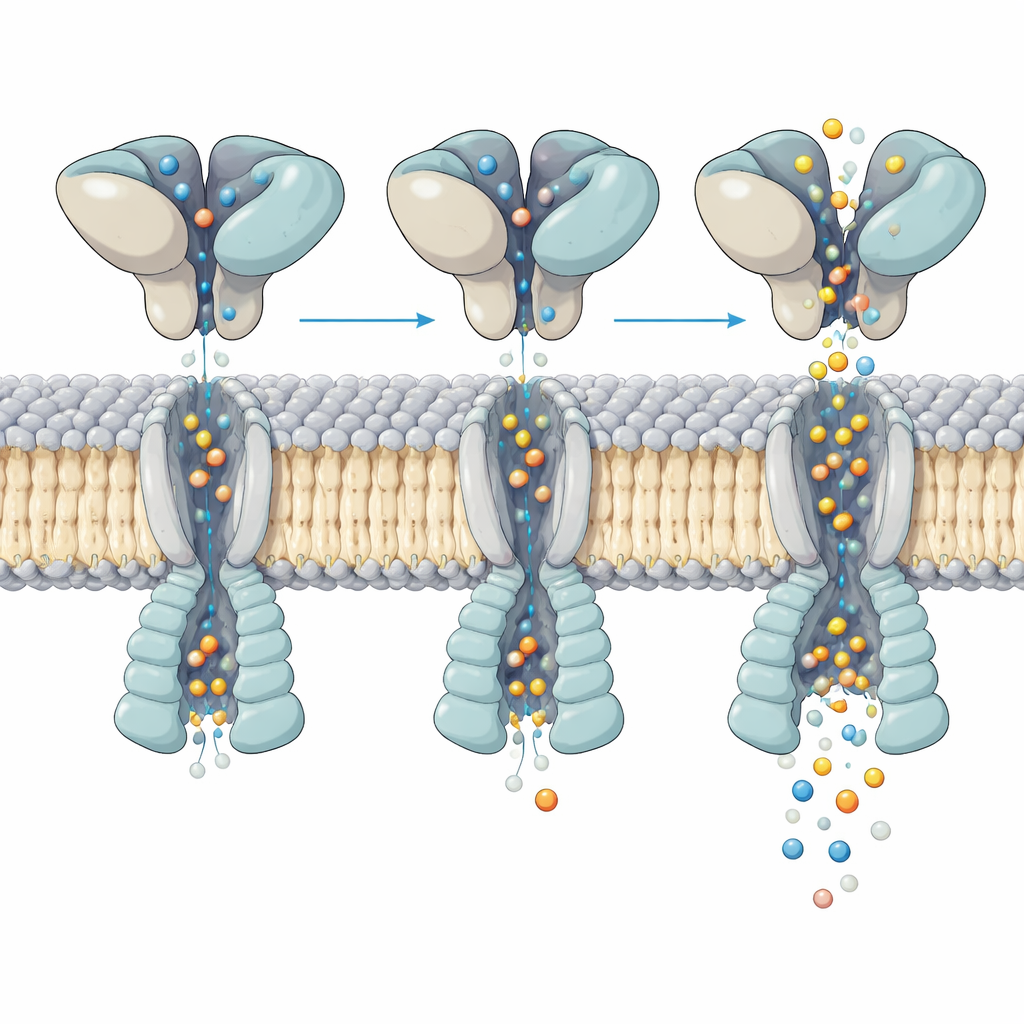
Come il cambiamento di forma controlla il flusso di ioni
Un’ispezione più ravvicinata del canale attivo ha mostrato come il movimento nel livello di legame del glutammato superiore si traduca nell’apertura del poro sottostante. Tutte e quattro le tasche di legame erano occupate dal glutammato, eppure le eliche che formano il cancello si piegavano in modo irregolare e asimmetrico tra le quattro sottounità. Analizzando centinaia di migliaia di particelle, il gruppo ha risolto cinque distinti «sottostati» dello stesso recettore attivato. In ciascun sottostato i domini superiori oscillano e ruotano leggermente rispetto al nucleo di membrana, e questo piccolo riassetto sposta dove e quanto si incurvano le eliche chiave all’interno del poro. Queste sottili differenze modificano la larghezza del poro in punti critici, corrispondendo ai molteplici livelli di conduttanza osservati nelle registrazioni di singoli canali, nonostante l’occupazione di glutammato sia la stessa.
Collegare la struttura alle varianti correlate a malattie
Lo studio identifica quasi ogni amminoacido in un tratto breve e altamente conservato dell’elica che forma il poro come potenzialmente capace di funzionare da cerniera di flessione. Diverse di queste posizioni corrispondono esattamente ai punti in cui sono state trovate mutazioni patogene nella GluA4 umana in pazienti con epilessia e disabilità intellettiva. Gli autori propongono che queste varianti probabilmente alterino la facilità con cui l’elica può piegarsi, spostando l’equilibrio tra i sottolivelli di apertura del canale o modificando l’accesso del calcio a un sito di legame vicino. Di fatto, piccoli cambiamenti in questa zona a cerniera potrebbero sintonizzare eccessivamente o insufficiente il segnale elettrico trasmesso dai recettori contenenti GluA4, con conseguenze importanti per i circuiti neurali che dipendono da scariche estremamente rapide e precise.
Cosa significa per la salute cerebrale
Dimostrando che GluA4 è allo stesso tempo strutturalmente stabile e insolitamente flessibile nella forma, questo lavoro riformula il modo in cui gli scienziati pensano alla funzione dei recettori AMPA. Invece di considerare i diversi livelli di corrente semplicemente come risultato del numero di molecole di glutammato legate, i risultati supportano l’idea secondo cui un recettore completamente carico può comunque campionare molteplici conformazioni, ciascuna con un’apertura del poro distinta. Questa «plasticità conformazionale» fornisce una spiegazione strutturale per le risposte graduate dei canali GluA4 e suggerisce nuovi modi in cui farmaci o proteine partner potrebbero modulare la loro attività. A lungo termine, mappare questi cambiamenti microscopici di forma potrebbe guidare terapie per disturbi in cui GluA4 è un attore chiave — da alcune forme di epilessia ai cambiamenti di circuito nella malattia psichiatrica e nella segnalazione cerebrale legata al cancro.
Citazione: Hale, W.D., Wang, H., Huganir, R.L. et al. Structural basis for activation and conformational plasticity of the GluA4 AMPA receptor. Nat Commun 17, 2932 (2026). https://doi.org/10.1038/s41467-026-68953-9
Parole chiave: Recettore AMPA, GluA4, trasmissione sinaptica, crio‑microscopia elettronica, apertura del canale ionico