Clear Sky Science · pl
Strukturalne podstawy aktywacji i plastyczności konformacyjnej receptora AMPA GluA4
Dlaczego ten kanał mózgowy ma znaczenie
Każda myśl, pamięć i ruch w twoim ciele zależy od drobnych sygnałów elektrycznych przekazywanych między komórkami nerwowymi. Wiele z tych sygnałów przenoszonych jest przez receptory AMPA, molekularne „wrota”, które otwierają się w odpowiedzi na neuroprzekaźnik glutaminian. W tej pracy skupiono się na rzadkiej wersji tych wrót, zwanej GluA4, która występuje obficie w szybko wyładowujących się komórkach mózgu oraz w móżdżku. Ponieważ zmiany w GluA4 powiązano z epilepsją, upośledzeniem intelektualnym, a nawet nowotworami mózgu, poznanie działania tego receptora na poziomie atomowym może wyjaśnić, dlaczego jest tak silny — i w jaki sposób można go potencjalnie ukierunkować lekami w przyszłości.
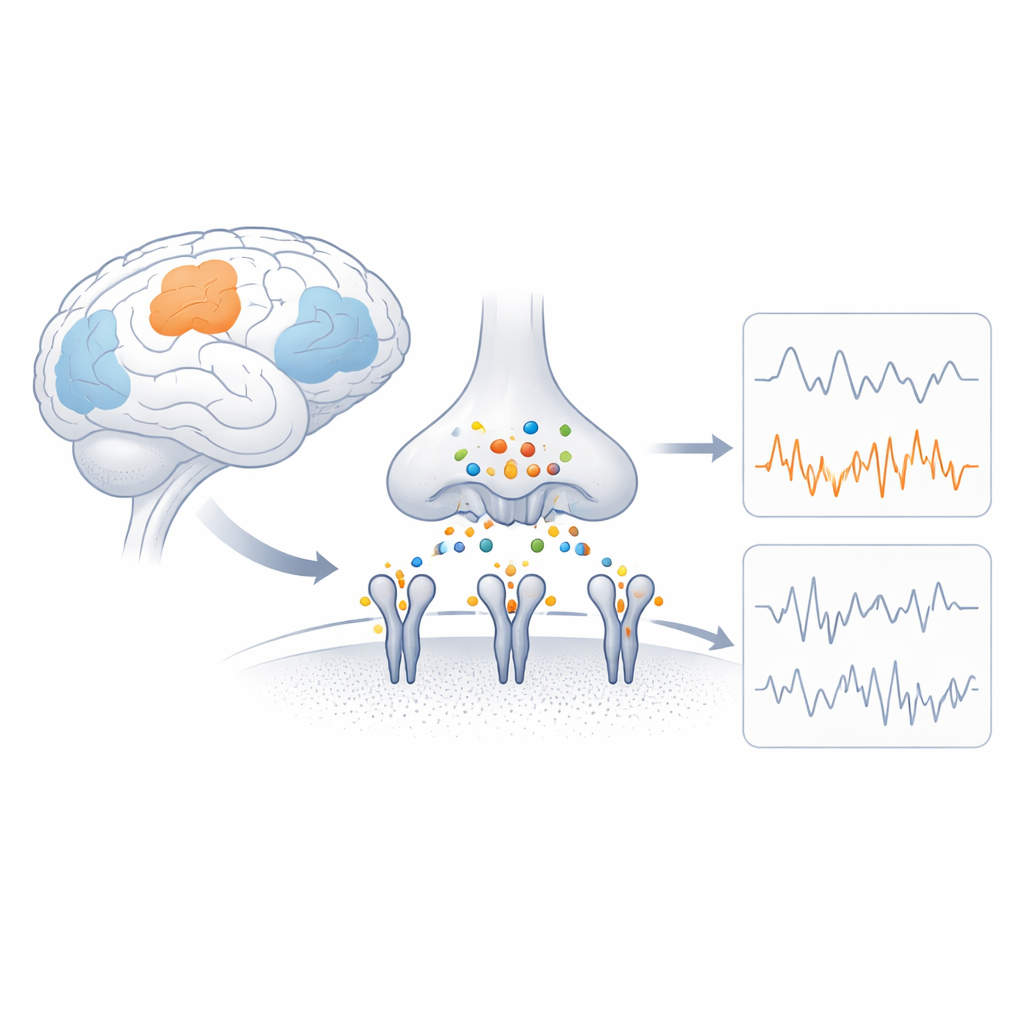
Szybkie przełączniki mózgu
Receptory AMPA to kompleksy białkowe zakotwiczone w błonie komórek nerwowych, które przekształcają sygnał chemiczny w prąd elektryczny, pozwalając na przepływ naładowanych cząstek. Każdy receptor zbudowany jest z czterech spokrewnionych podjednostek, a ich skład determinuje, jak szybko kanał się otwiera, jak duży prąd przewodzi i czy do wnętrza może przedostać się wapń. GluA4 to podjednostka przepuszczalna dla wapnia, występująca niezwykle intensywnie w określonych typach komórek, takich jak neurony hamujące pozytywne dla parwalbuminy oraz niektóre neurony słuchowe i móżdżkowe. Badania genetyczne pokazują, że uszkadzające zmiany w genie GluA4 mogą powodować napady i zaburzenia poznawcze, co sugeruje, że jej specyficzne właściwości są kluczowe dla funkcjonowania mózgu, choć pozostawały dotąd strukturalnie tajemnicze.
Uchwycenie GluA4 w działaniu
Aby ujawnić, jak działa GluA4, badacze zastosowali kriomikroskopię elektronową — technikę obrazowania zamrożonych błyskawicznie cząsteczek z niemal atomową rozdzielczością. Oczyszczono receptory złożone wyłącznie z GluA4 i ściśle powiązane z pomocniczym białkiem TARPγ2, które naturalnie współdziała z GluA4 w mózgu i precyzuje jej właściwości. Zespół zablokował receptory w stanie aktywnym, niezdezesnizowanym, używając glutaminianu wraz z lekiem zapobiegającym zamknięciu kanału. Nagrania elektryczne wykonane na sztucznych błonach potwierdziły, że te oczyszczone kompleksy zachowywały się jak prawdziwe receptory AMPA, wykazując krótkie i długie otwarcia o wielu poziomach prądu.
Elastyczna, a jednak spójna architektura
Mapy strukturalne ujawniły, że receptory GluA4 zachowują klasyczny układ w kształcie litery Y znany z innych receptorów AMPA: górny „głowowy” region poza komórką wyczuwający glutaminian oraz dolne jądro tworzące kanał jonowy przez błonę. Najwyższa warstwa, zwana domeną aminoterminową, okazała się zaskakująco ruchoma — przyjmowała wiele różnych pozycji, zachowując jednocześnie kluczowe kontakty spajające cztery podjednostki. Pokazuje to, że zewnętrzny szkielet GluA4 jest stabilny, lecz wysoce elastyczny, co może umożliwiać mu interakcję z różnorodnymi partnerami białkowymi w różnych regionach mózgu bez rozpadu kompletu.
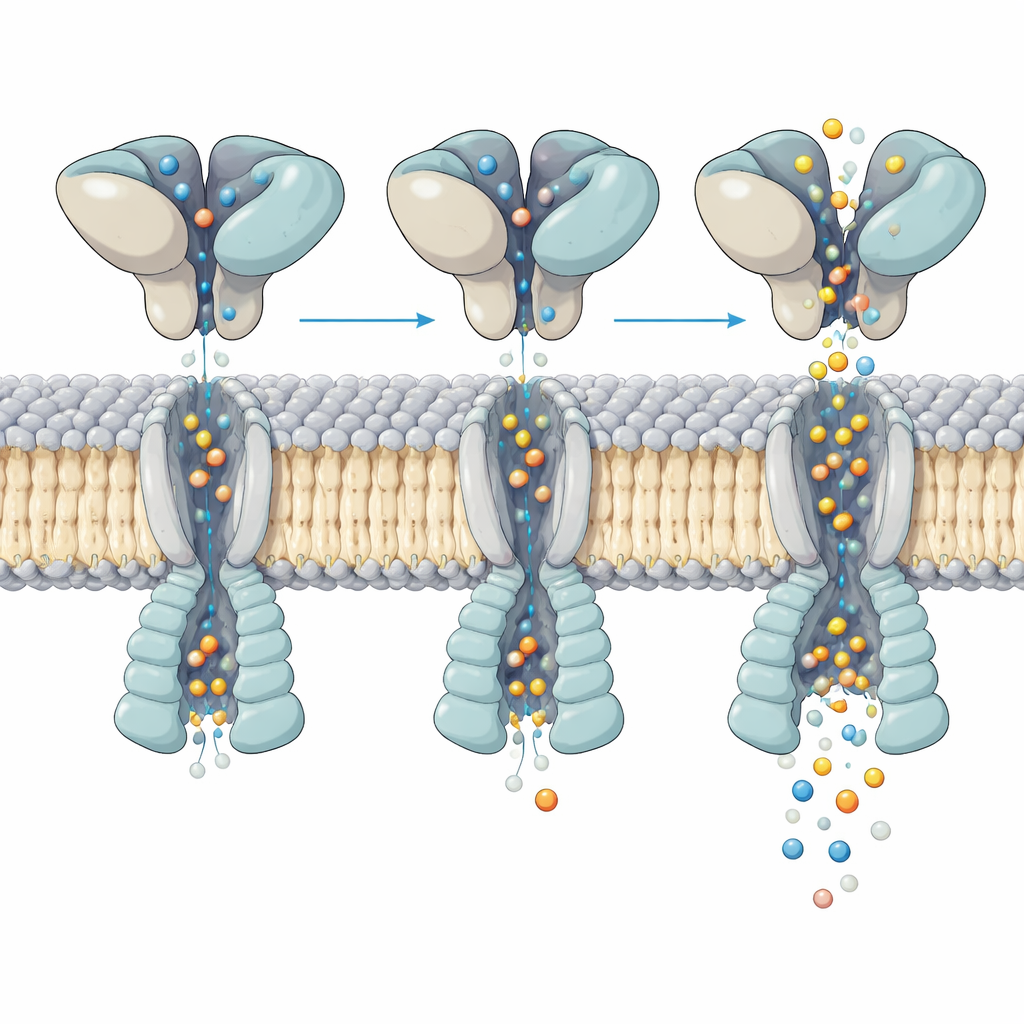
Jak zmiana kształtu kontroluje przepływ jonów
Bardziej szczegółowa analiza aktywnego kanału ujawniła, jak ruch w warstwie wiążącej glutaminian powyżej przekłada się na otwarcie poru poniżej. Wszystkie cztery kieszenie wiążące były wypełnione glutaminianem, jednak helisy tworzące bramkę zginały się w nierównomierny, asymetryczny sposób wśród podjednostek. Analiza setek tysięcy cząstek pozwoliła wydzielić pięć odrębnych „podstanów” tego samego aktywowanego receptora. W każdej z nich górne domeny nieznacznie kołyszą się i skręcają względem rdzenia błonowego, a ta drobna reorganizacja przesuwa miejsce i siłę, z jaką kluczowe helisy załamują się wewnątrz poru. Te subtelne różnice zmieniają szerokość poru w krytycznych punktach, co odpowiada wielopoziomowym wartościom przewodności obserwowanym w pomiarach pojedynczych kanałów, mimo że zajętość miejsc wiążących glutaminian jest taka sama.
Łączenie struktury z wariantami związanymi z chorobami
Badanie identyfikuje niemal każdy aminokwas w krótkim, silnie zachowanym odcinku helisy tworzącej por jako zdolny służyć jako zawias do zginania. Kilka z tych pozycji odpowiada dokładnym miejscom, w których odkryto mutacje wywołujące choroby u ludzi z epilepsją i upośledzeniem intelektualnym. Autorzy sugerują, że te warianty prawdopodobnie zmieniają łatwość, z jaką helisa może się załamywać, przesuwając równowagę między podpoziomami otwarcia kanału lub zmieniając dostęp wapnia do pobliskiego miejsca wiążącego. W praktyce drobne zmiany w tej strefie zawiasowej mogą nadmiernie lub niedostatecznie dostroić sygnał elektryczny przekazywany przez receptory zawierające GluA4, z poważnymi konsekwencjami dla obwodów nerwowych polegających na niezwykle szybkim i precyzyjnym wyładowaniu.
Co to oznacza dla zdrowia mózgu
Pokazując, że GluA4 jest jednocześnie strukturalnie stabilna i wyjątkowo plastyczna konformacyjnie, praca ta przekształca sposób myślenia naukowców o funkcji receptorów AMPA. Zamiast traktować różne poziomy prądu jedynie jako rezultat liczby związanych cząsteczek glutaminianu, wyniki wspierają obraz, w którym w pełni zajęty receptor nadal może próbować wielu konformacji, z których każda ma odrębne otwarcie poru. Ta „plastyczność konformacyjna” dostarcza strukturalnego wytłumaczenia gradacyjnych odpowiedzi kanałów GluA4 i sugeruje nowe sposoby, w jakie leki lub białkowi partnerzy mogą modulować ich aktywność. W dłuższej perspektywie mapowanie tych mikroskopijnych zmian kształtu może ukierunkować terapie dla zaburzeń, w których GluA4 odgrywa kluczową rolę — od niektórych postaci epilepsji po zmiany obwodów w chorobach psychicznych oraz w sygnalizacji mózgowej związanej z rakiem.
Cytowanie: Hale, W.D., Wang, H., Huganir, R.L. et al. Structural basis for activation and conformational plasticity of the GluA4 AMPA receptor. Nat Commun 17, 2932 (2026). https://doi.org/10.1038/s41467-026-68953-9
Słowa kluczowe: receptor AMPA, GluA4, transmisja synaptyczna, kriomikroskopia elektronowa, zamykanie kanału jonowego