Clear Sky Science · es
Base estructural para la activación y la plasticidad conformacional del receptor AMPA GluA4
Por qué importa este canal cerebral
Cada pensamiento, recuerdo y movimiento del cuerpo depende de diminutas señales eléctricas que se transmiten entre las neuronas. Muchas de estas señales son mediadas por receptores AMPA, «puertas» moleculares que se abren al detectar el mensajero químico glutamato. Este estudio se centra en una versión poco común de esa puerta, llamada GluA4, que se concentra en neuronas de disparo rápido y en el cerebelo. Dado que las alteraciones en GluA4 se han asociado con epilepsia, discapacidad intelectual e incluso tumores cerebrales, comprender cómo funciona este receptor a nivel atómico podría revelar por qué es tan potente —y cómo podría ser diana de futuros fármacos.
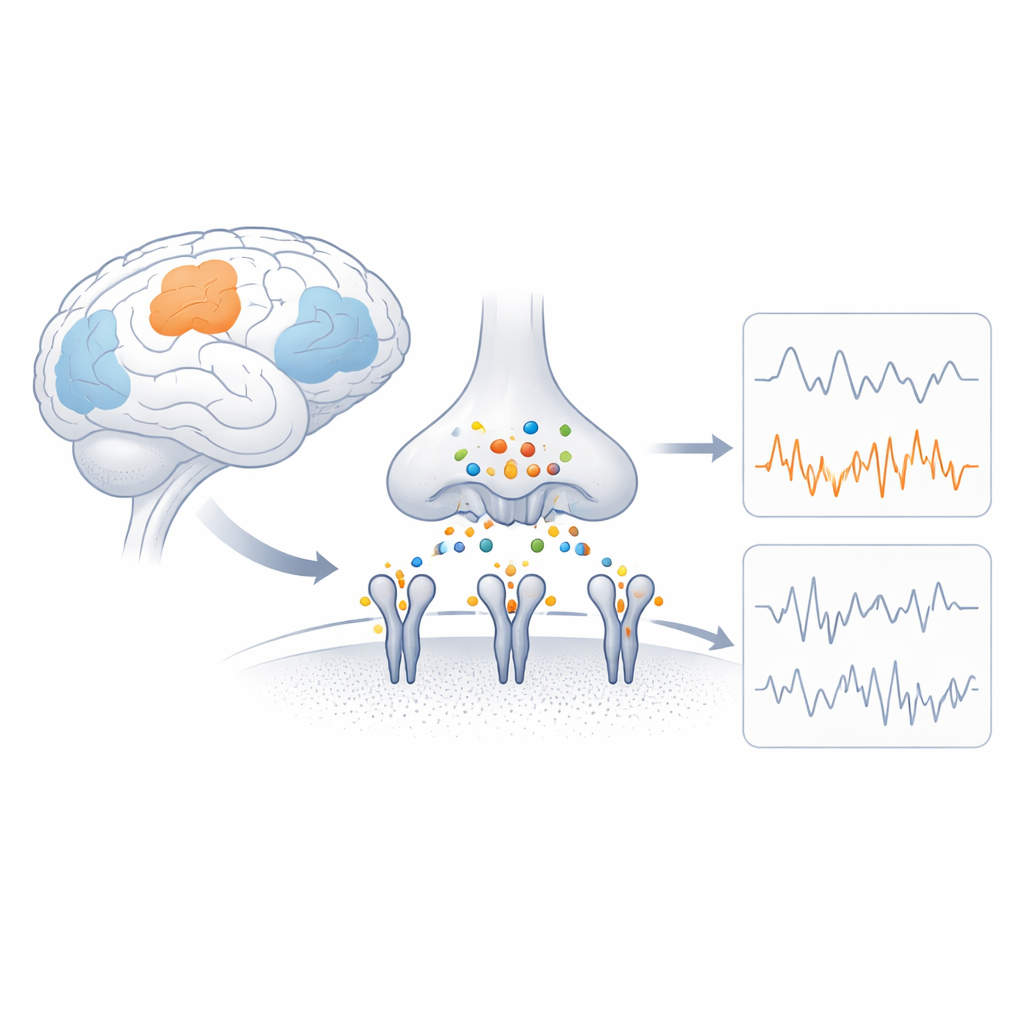
Los conmutadores rápidos del cerebro
Los receptores AMPA son complejos proteicos que se sitúan en la membrana de las neuronas y convierten una señal química en una corriente eléctrica permitiendo el paso de partículas cargadas. Cada receptor se compone de cuatro partes relacionadas (subunidades), y la mezcla de estas subunidades determina la rapidez con la que se abre el canal, la cantidad de corriente que deja pasar y si puede entrar calcio. GluA4 es una subunidad permeable al calcio que abunda de forma inusual en tipos celulares específicos, como las neuronas inhibitorias parvalbumina‑positivas y ciertas neuronas auditivas y cerebelosas. Estudios genéticos muestran que cambios dañinos en el gen de GluA4 pueden causar convulsiones y problemas cognitivos, lo que sugiere que sus propiedades especiales son cruciales para la función cerebral pero hasta ahora habían permanecido estructuralmente enigmáticas.
Capturando a GluA4 en acción
Para revelar cómo opera GluA4, los investigadores utilizaron crio‑microscopía electrónica, una técnica que imagen moléculas vitrificadas a resolución casi atómica. Purificaron receptores compuestos enteramente por GluA4 y estrechamente ligados a una proteína auxiliar llamada TARPγ2, que se asocia de forma natural con GluA4 en el cerebro y ayuda a afinar su comportamiento. El equipo bloqueó los receptores en un estado activo y no desensibilizado usando glutamato junto con un fármaco que impide el cierre del canal. Registros eléctricos en membranas artificiales confirmaron que estos complejos purificados se comportaban como receptores AMPA reales, produciendo aperturas breves y prolongadas con múltiples niveles de corriente.
Una arquitectura flexible pero intacta
Los mapas estructurales revelaron que los receptores GluA4 conservan el diseño clásico en forma de Y observado en otros receptores AMPA: una región superior «cabeza» fuera de la célula que detecta glutamato, y un núcleo inferior que forma el canal iónico a través de la membrana. La capa más externa, denominada dominio aminoterminal, resultó ser sorprendentemente móvil, adoptando muchas posiciones diferentes mientras mantenía contactos clave que sostienen las cuatro subunidades juntas. Esto muestra que el armazón exterior de GluA4 está intacto pero es altamente flexible, lo que potencialmente le permite interactuar con diversos socios proteicos en distintas regiones del cerebro sin desintegrarse.
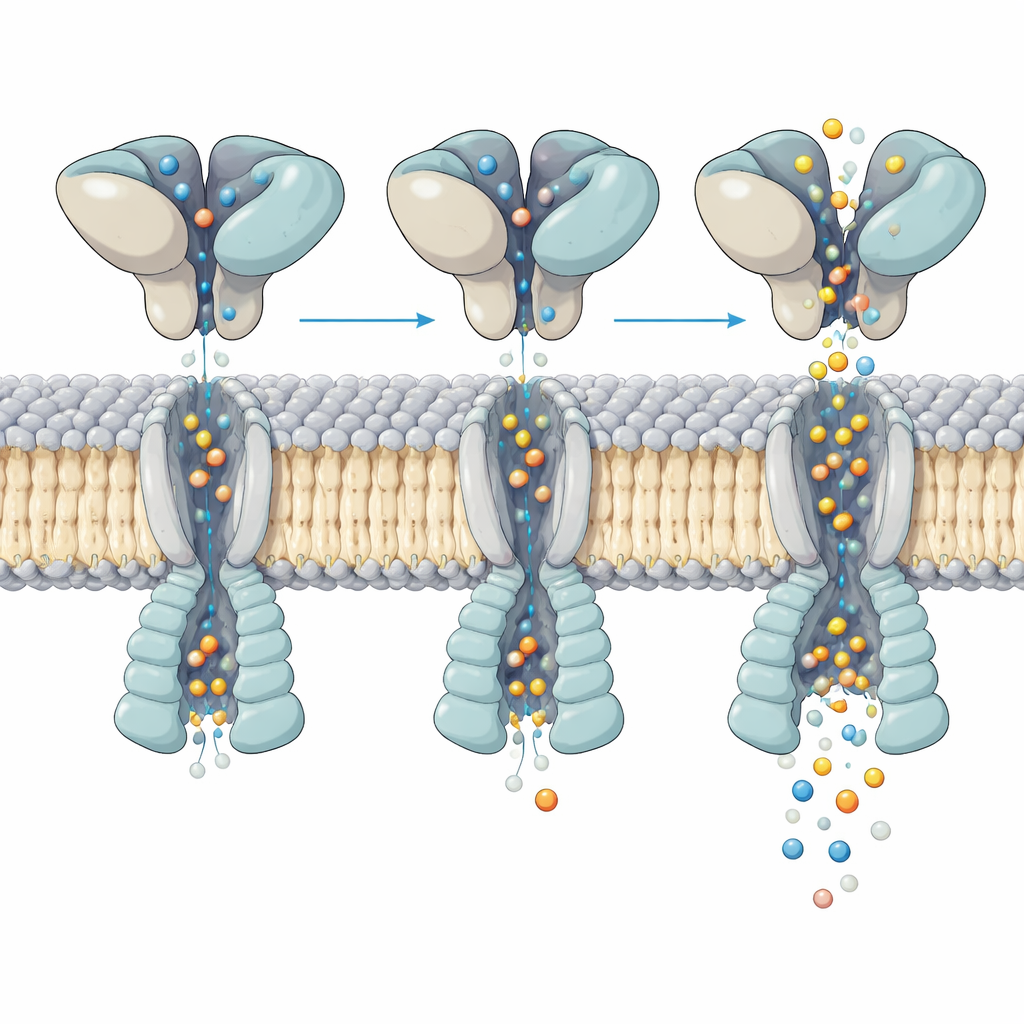
Cómo el cambio de forma controla el flujo de iones
Una inspección más detallada del canal activo mostró cómo el movimiento en la capa de unión al glutamato se traduce en la apertura del poro debajo. Los cuatro huecos de unión estaban ocupados por glutamato, sin embargo, las hélices que forman la compuerta se doblaron de manera desigual y asimétrica entre las cuatro subunidades. Al analizar cientos de miles de partículas, el equipo resolvió cinco «subestados» distintos del mismo receptor activado. En cada subestado, los dominios superiores se balancean y giran ligeramente respecto al núcleo de la membrana, y este pequeño reajuste desplaza dónde y con qué intensidad se producen las flexiones clave de las hélices dentro del poro. Estas diferencias sutiles modifican la anchura del poro en puntos críticos, coincidiendo con los múltiples niveles de conductancia observados en registros de canales individuales, pese a que la ocupación por glutamato es la misma.
Vinculando la estructura con variantes relacionadas con enfermedades
El estudio identifica casi todos los aminoácidos en un tramo corto y altamente conservado de la hélice formadora del poro como capaces de funcionar como bisagra de flexión. Varias de estas posiciones coinciden exactamente con mutaciones causantes de enfermedad en GluA4 humano halladas en pacientes con epilepsia y discapacidad intelectual. Los autores proponen que estas variantes probablemente alteran la facilidad con la que la hélice puede doblarse, desplazando el equilibrio entre los subniveles de apertura del canal o cambiando el acceso del calcio a un sitio de unión cercano. En efecto, pequeños cambios en esta zona bisagra podrían sobreajustar o subajustar la señal eléctrica mediada por receptores que contienen GluA4, con grandes consecuencias para los circuitos neuronales que dependen de disparos extremadamente rápidos y precisos.
Qué significa esto para la salud cerebral
Al mostrar que GluA4 es a la vez estructuralmente estable y extraordinariamente flexible en su forma, este trabajo replantea la forma en que los científicos piensan sobre la función de los receptores AMPA. En lugar de ver los distintos niveles de corriente simplemente como resultado del número de moléculas de glutamato unidas, los hallazgos apoyan una visión en la que un receptor completamente cargado aún puede muestrear múltiples conformaciones, cada una con una apertura de poro distinta. Esta «plasticidad conformacional» ofrece una explicación estructural para las respuestas graduadas de los canales GluA4 y sugiere nuevas vías por las que fármacos o proteínas asociadas podrían modular su actividad. A largo plazo, cartografiar estos cambios microscópicos de forma podría orientar terapias para trastornos en los que GluA4 es un actor clave —desde ciertas epilepsias hasta alteraciones de circuito en enfermedades psiquiátricas y la señalización cerebral relacionada con el cáncer.
Cita: Hale, W.D., Wang, H., Huganir, R.L. et al. Structural basis for activation and conformational plasticity of the GluA4 AMPA receptor. Nat Commun 17, 2932 (2026). https://doi.org/10.1038/s41467-026-68953-9
Palabras clave: receptor AMPA, GluA4, transmisión sináptica, crio‑microscopía electrónica, apertura del canal iónico