Clear Sky Science · tr
GluA4 AMPA reseptörünün aktivasyonu ve konformasyonel plastisitesinin yapısal temeli
Bu beyin kanalı neden önemli
Vücudunuzdaki her düşünce, anı ve hareket, sinir hücreleri arasında geçen küçük elektrik sinyallerine dayanır. Bu sinyallerin birçoğu, kimyasal haberci glutamati algıladıklarında açılan moleküler “kapılar” olan AMPA reseptörleri aracılığıyla iletilir. Bu çalışma, hızlı ateşleyen beyin hücrelerinde ve beyincikte yoğunlaşmış nadir bir kapı çeşidi olan GluA4’e odaklanıyor. GluA4’teki değişikliklerin epilepsi, zihinsel engellilik ve hatta beyin tümörleriyle ilişkilendirilmesi nedeniyle, bu reseptörün atomik düzeyde nasıl çalıştığını anlamak, neden bu kadar etkili olduğunu ve gelecekteki ilaçların nasıl hedefleyebileceğini ortaya koyabilir.
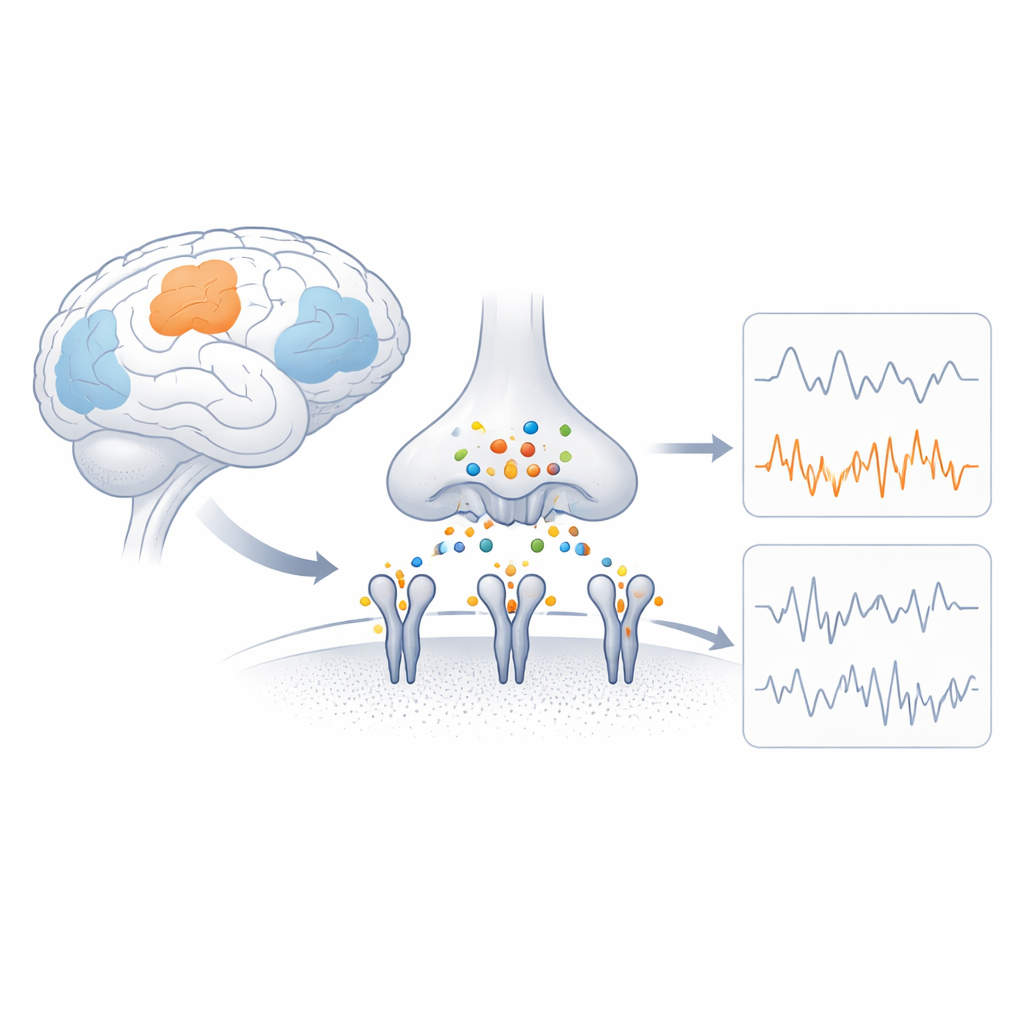
Beynin hızlı anahtarları
AMPA reseptörleri, sinir hücrelerinin zarında bulunan ve kimyasal bir sinyali yüklü parçacıkların akışına izin vererek elektrik akımına dönüştüren protein kompleksleridir. Her reseptör dört ilgili parçadan (altbirim) oluşur ve bu altbirimlerin karışımı, kanalın ne kadar çabuk açıldığını, ne kadar akım geçtiğini ve kalsiyumun girip giremeyeceğini belirler. GluA4, parvalbumin-pozitif inhibitör nöronlar ve belirli işitsel ve beyincik nöronları gibi özgül hücre tiplerinde alışılmadık derecede bol bulunan kalsiyum geçirgen bir altbirimdir. Genetik çalışmalar, GluA4 genindeki zararlı değişikliklerin nöbetlere ve bilişsel sorunlara yol açabileceğini gösteriyor; bu da onun özel özelliklerinin beyin işlevi için kritik olduğunu ancak yapısal olarak gizemini koruduğunu işaret ediyor.
GluA4’ü eylem halinde yakalamak
GluA4’ün nasıl çalıştığını ortaya koymak için araştırmacılar, molekülleri neredeyse atomik çözünürlükte görüntüleyen bir teknik olan kryo-elektron mikroskopisini kullandılar. Araştırmacılar tamamen GluA4’ten oluşan ve beyinde doğal olarak GluA4 ile ilişkili olup davranışını ince ayarlayan yardımcı bir ortak protein olan TARPγ2’ye sıkıca bağlı reseptörleri saflaştırdılar. Ekip, glutamat ile birlikte kanalı kapanmaktan alıkoyan bir ilaç kullanarak reseptörleri aktif, desensitize olmamış bir durumda kilitledi. Yapay membranlardaki elektrik kayıtları, bu saflaştırılmış komplekslerin gerçek AMPA reseptörleri gibi davrandığını, çok seviyeli kısa ve uzun açıklıklar ürettiğini doğruladı.
Esnek ama bütünsel bir mimari
Yapısal haritalar, GluA4 reseptörlerinin diğer AMPA reseptörlerinde görülen klasik Y-şeklindeki düzeni koruduğunu gösterdi: hücre dışındaki glutamati algılayan üst “baş” bölgesi ve zar boyunca iyon kanalını oluşturan alt çekirdek. Amino-terminus adı verilen en üst katman, dört altbirimi bir arada tutan kilit temasları korurken şaşırtıcı derecede hareketli çıktı ve birçok farklı pozisyon benimsedi. Bu, GluA4’ün dış iskelesinin sağlam fakat son derece esnek olduğunu; böylece farklı beyin bölgelerinde çeşitli ortak proteinlerle etkileşim kurmasına izin verebileceğini, parçalanmadan kalabileceğini gösterir.
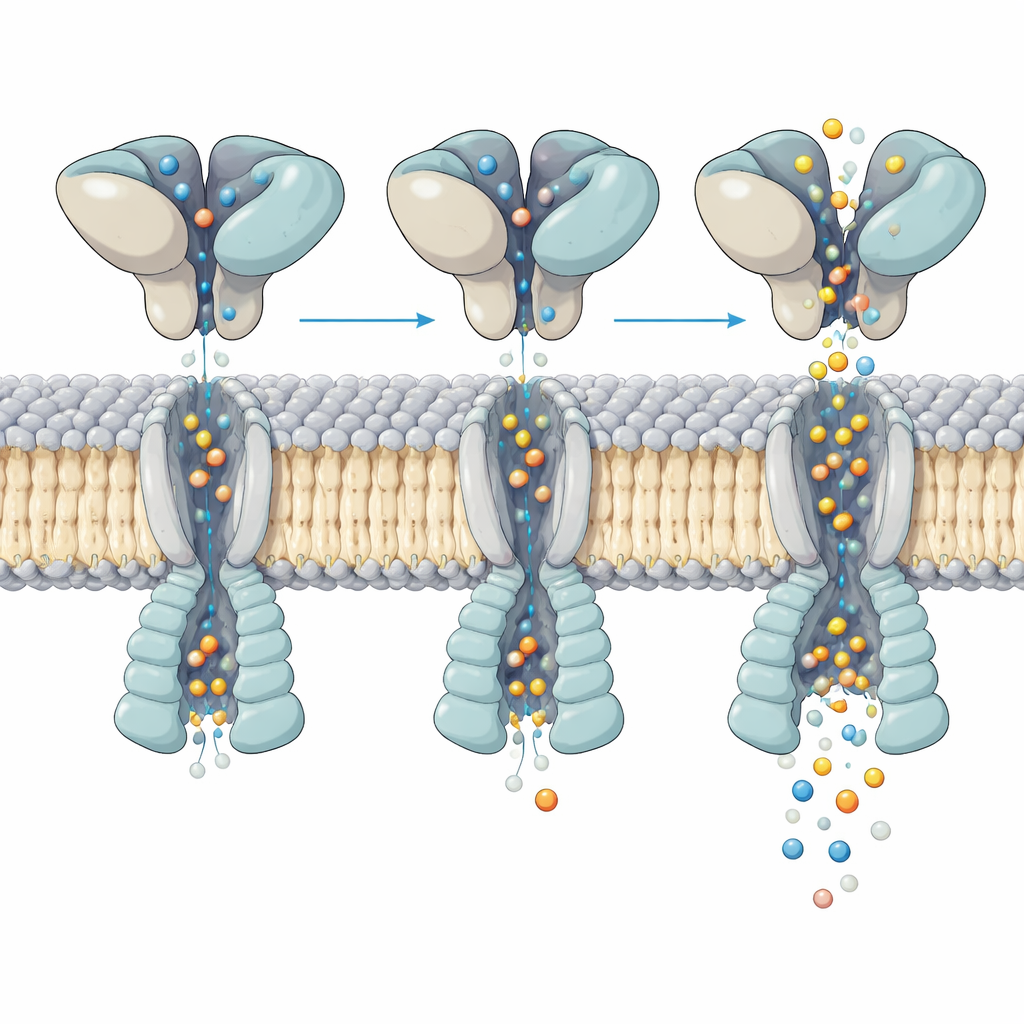
Şekil değiştirme iyon akışını nasıl kontrol eder
Aktif kanalın daha yakından incelenmesi, üstteki glutamat-bağlayıcı katmandaki hareketin alttaki gözenek açılmasına nasıl dönüştüğünü ortaya çıkardı. Dört bağlanma cebi de glutamatla doluydu, ancak kapıyı oluşturan heliksler dört altbirim arasında düzensiz, simetrik olmayan bir şekilde büküldü. Yüzbinlerce parçacığın analiz edilmesiyle ekip, aynı aktive olmuş reseptörün beş farklı “alt-durumunu” ayırt etti. Her alt-durumda üst bölgeler membral çekirdeğe göre hafifçe sallanıp dönüyor ve bu küçük yeniden düzenleme, gözenek içindeki ana helikslerin nerede ve ne kadar güçlü eğildiğini değiştiriyor. Bu ince farklılıklar, gözenek genişliğini kritik noktalarda değiştirerek tek kanal kayıtlarında görülen çoklu iletkenlik seviyeleriyle uyum sağlıyor; oysa glutamat doluluğu aynı kalıyor.
Yapıyı hastalıkla ilişkili varyantlara bağlamak
Çalışma, gözenek oluşturan heliksin kısa, yüksek derecede korunmuş bir bölgesindeki neredeyse her amino asidin bükülme menteşesi olarak görev yapabileceğini belirliyor. Bu pozisyonların birkaçında, insan GluA4’te epilepsi ve zekâ geriliği olan hastalarda bulunan hastalığa neden olan mutasyonlar tam olarak yer alıyor. Yazarlar, bu varyantların heliksin ne kadar kolayça bükülebileceğini muhtemelen değiştirdiğini; kanal açılmasının alt seviyeleri arasındaki dengeyi kaydırdığını veya yakınlardaki bir bağlanma bölgesine kalsiyum erişimini etkilediğini öne sürüyor. Etkide, bu menteşe bölgesindeki küçük değişiklikler, GluA4 içeren reseptörlerin taşıdığı elektrik sinyalini aşırı veya yetersiz ayarlayabilir ve son derece hızlı, hassas ateşlemeye dayanan sinir devreleri için büyük sonuçlar doğurabilir.
Bu bulguların beyin sağlığı için anlamı
GluA4’ün hem yapısal olarak stabil hem de alışılmadık derecede şekil-esnek olduğunu göstererek bu çalışma, bilim insanlarının AMPA reseptör işlevini düşünme biçimini yeniden çerçeveliyor. Farklı akım seviyelerini sadece kaç glutamat molekülünün bağlı olduğunun bir sonucu olarak görmek yerine, bulgular tamamen dolu bir reseptörün yine de her biri farklı bir gözenek açıklığına sahip birden çok konformasyonu deneyimleyebileceği bir resmi destekliyor. Bu “konformasyonel plastisite”, GluA4 kanallarının dereceli yanıtları için yapısal bir açıklama sunuyor ve ilaçların veya ortak proteinlerin aktiviteyi nasıl ayarlayabileceğine dair yeni yollar öneriyor. Uzun vadede, bu mikroskopik şekil değişikliklerinin haritalanması, GluA4’ün önemli bir rol oynadığı bozukluklar—belirli epilepsilerden psikiyatrik hastalıklardaki devre değişikliklerine ve kanserle ilişkili beyin sinyalleşmesine—yönelik tedavilere rehberlik edebilir.
Atıf: Hale, W.D., Wang, H., Huganir, R.L. et al. Structural basis for activation and conformational plasticity of the GluA4 AMPA receptor. Nat Commun 17, 2932 (2026). https://doi.org/10.1038/s41467-026-68953-9
Anahtar kelimeler: AMPA reseptörü, GluA4, sinaptik iletim, kryo elektron mikroskopisi, iyon kanalı kapanması