Clear Sky Science · ja
GluA4 AMPA受容体の活性化とコンフォメーション可塑性の構造基盤
なぜこの脳のチャネルが重要なのか
あなたの思考、記憶、運動のすべては、神経細胞間を通る微小な電気信号に依存しています。これらの信号の多くは、グルタミン酸という化学メッセンジャーを感知すると開く分子「ゲート」であるAMPA受容体によって伝えられます。本研究は、速発火する神経細胞や小脳に多く存在する稀なゲートの一種であるGluA4に焦点を当てています。GluA4の変化はてんかん、知的障害、さらには脳腫瘍と関連づけられているため、この受容体が原子レベルでどのように機能するかを理解することは、その強力さの理由や将来の医薬品による標的化の手がかりを与える可能性があります。
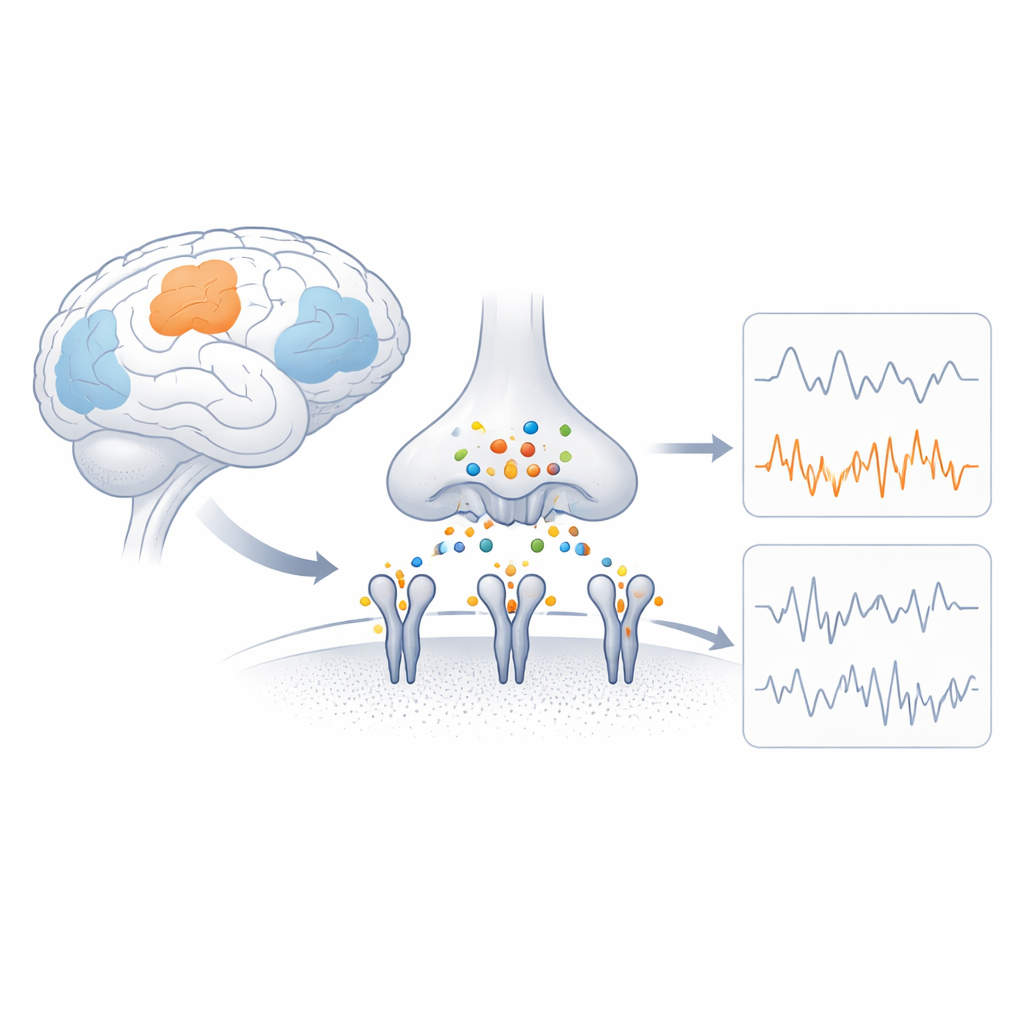
脳の高速スイッチ
AMPA受容体は神経細胞の膜に位置するタンパク質複合体で、化学信号を電流に変換し、帯電粒子の流入を許すことで機能します。各受容体は4つの関連サブユニットから構成され、サブユニットの組み合わせがチャネルの開口速度、通す電流量、カルシウムの透過性を決定します。GluA4はカルシウム透過性を持つサブユニットで、パルブアルブミン陽性の抑制性ニューロンや特定の聴覚・小脳ニューロンなど、特定の細胞型に異常に豊富に存在します。遺伝学的研究は、GluA4遺伝子の損傷性変化が発作や認知障害を引き起こすことを示しており、その特異な性質が脳機能にとって重要である一方で、構造的には不明な点が多いことを示唆しています。
作動中のGluA4を捉える
GluA4の動作を明らかにするため、研究者らはクライオ電子顕微鏡(クライオEM)を用い、ほぼ原子分解能でフラッシュフローズンした分子を撮像しました。彼らはGluA4のみで構成され、脳内で自然にGluA4に結合してその挙動を調節する補助タンパク質TARPγ2と強固に結び付いた受容体を精製しました。チームは、グルタミン酸とチャネルの閉鎖を防ぐ薬剤を併用することで、脱感作していない活性状態に受容体を固定しました。人工膜での電気生理記録は、これらの精製複合体が実際のAMPA受容体と同様に振る舞い、短時間と長時間の開口および複数レベルの電流を生じることを確認しました。
柔軟性を保った一体的な構造
構造マップは、GluA4受容体が他のAMPA受容体で見られる古典的なY字型レイアウトを保持していることを示しました:細胞外に位置する上部の“頭”領域がグルタミン酸を感知し、膜を貫くイオンチャネルを形成する下部コアがあります。最上層のアミノ末端ドメインは驚くほど可動性が高く、四つのサブユニットを結びつける主要な接触を維持しつつ多様な位置をとることが分かりました。これは、GluA4の外側スキャフォールドが一体性を保ちつつ非常に柔軟であり、崩壊することなく異なる脳領域で多様なパートナータンパク質と相互作用できる可能性を示しています。
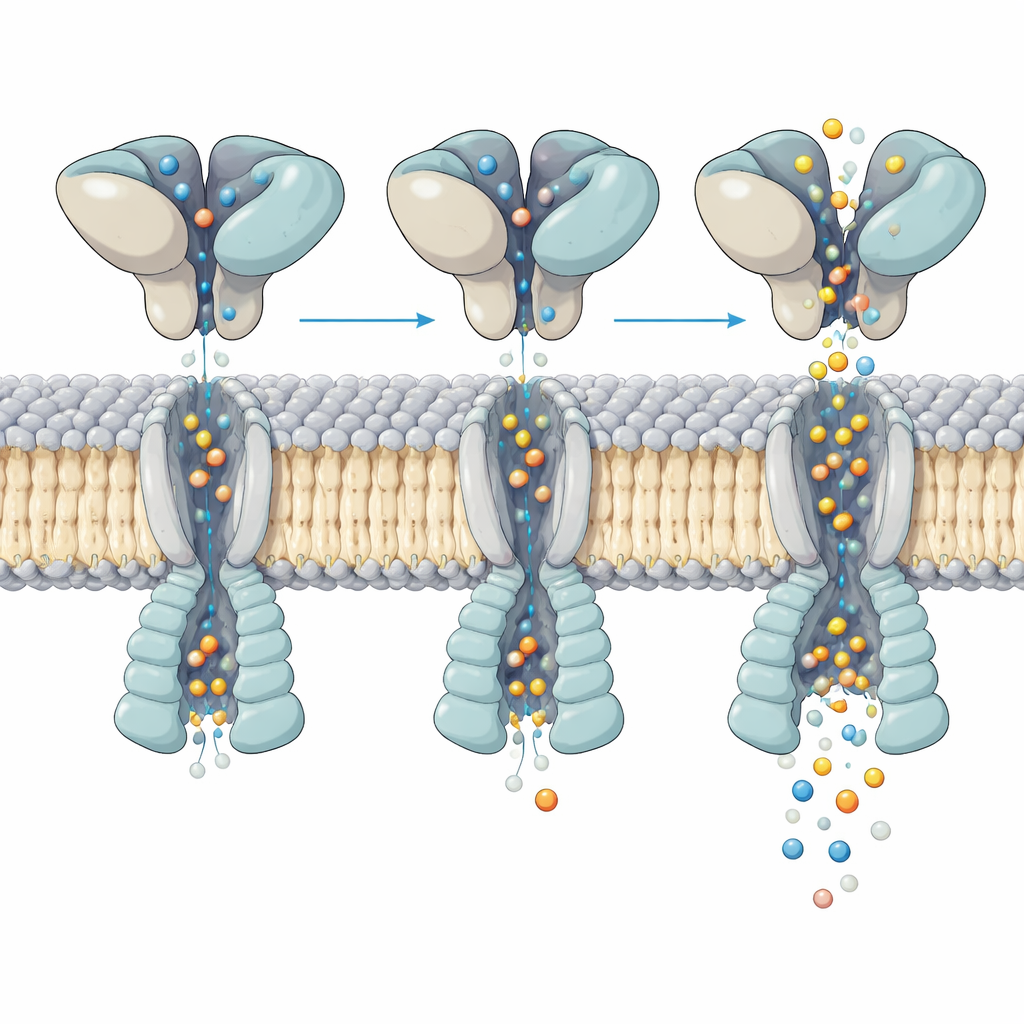
形状変化がイオン流を制御する仕組み
活性化したチャネルを詳しく調べると、上部のグルタミン酸結合層の運動がどのように下方の孔の開口に伝達されるかが明らかになりました。四つの結合ポケットはいずれもグルタミン酸で満たされていましたが、門を形成するヘリックスは四つのサブユニットで不均一かつ非対称に曲がっていました。数十万の粒子を解析することで、チームは同一の活性化受容体における5つの異なる「サブステート」を分離しました。各サブステートでは、上部ドメインが膜コアに対してわずかに揺れたりねじれたりし、その微小な再配列が孔内で重要なヘリックスが曲がる位置や曲がりやすさを変えます。これらの微妙な違いが、重要な箇所での孔の幅を変化させ、グルタミン酸占有が同じであっても単一チャネル記録で観察される複数の導電度レベルに対応します。
構造と疾患変異の結びつき
本研究は、孔を形成するヘリックスの短く高度に保存された領域のほぼすべてのアミノ酸が曲げヒンジとして機能し得ることを特定しました。これらの位置のいくつかは、てんかんや知的障害の患者で見つかっているGluA4の病因性変異と正確に一致します。著者らは、これらの変異がヘリックスの曲がりやすさを変え、チャネル開口のサブレベル間のバランスをシフトさせるか、近接する結合部位へのカルシウムのアクセスを変える可能性が高いと提案しています。結果として、このヒンジ領域のわずかな変化がGluA4含有受容体が担う電気信号を過度にあるいは不足気味に調節し、極めて高速かつ精密な発火を必要とする神経回路に大きな影響を与えることがあり得ます。
脳の健康にとっての意義
GluA4が構造的に安定でありながら異常に形を変えやすいことを示すことで、この研究はAMPA受容体の機能に対する科学者の理解を再構築します。異なる電流レベルを単に結合しているグルタミン酸分子の数の違いとしてだけ捉えるのではなく、完全に荷電した受容体でも複数のコンフォメーションを取り得て、それぞれが異なる孔の開き方を持つという図が支持されます。この「コンフォメーショナル・プラスティシティ」はGluA4チャネルの段階的応答に対する構造的説明を提供し、薬剤やパートナータンパク質がその活性を微調整する新たな手段を示唆します。長期的には、これらの微視的な形状変化を地図化することが、特定のてんかんから精神疾患やがん関連の脳内シグナル伝達にかかわる回路変化まで、GluA4が重要な役割を果たす疾患に対する治療法の指針となるかもしれません。
引用: Hale, W.D., Wang, H., Huganir, R.L. et al. Structural basis for activation and conformational plasticity of the GluA4 AMPA receptor. Nat Commun 17, 2932 (2026). https://doi.org/10.1038/s41467-026-68953-9
キーワード: AMPA受容体, GluA4, シナプス伝達, クライオ電子顕微鏡, イオンチャネルのゲーティング