Clear Sky Science · he
הבסיס המבני להפעלה ולגמישות הקונפורמציה של קולטני AMPA מסוג GluA4
מדוע התעלה הזאת במוח חשובה
כל מחשבה, זיכרון ותנועה בגופך תלויים באותות חשמליים זעירים החולפים בין תאי העצב. רבים מהאותות האלה מועברים על ידי קולטני AMPA, “שערים” מולקולריים הנפתחים כשהם מזהים את המוליך הכימי גלוטמט. המחקר הזה מתמקד בגרסה נדירה של השער, הנקראת GluA4, שנמצאת בריכוז גבוה בתאי מוח המתמצים לירי מהיר ובמוחון. מכיוון ששינויים ב‑GluA4 נקשרו לאפילפסיה, לקויות אינטלקטואליות ואפילו לגידולים מוחיים, הבנת אופן פעולת הקולטן ברזולוציה אטומית עשויה לחשוף מדוע הוא כה רב‑עוצמה — וכיצד ניתן יהיה למקד אותו בתרופות עתידיות.
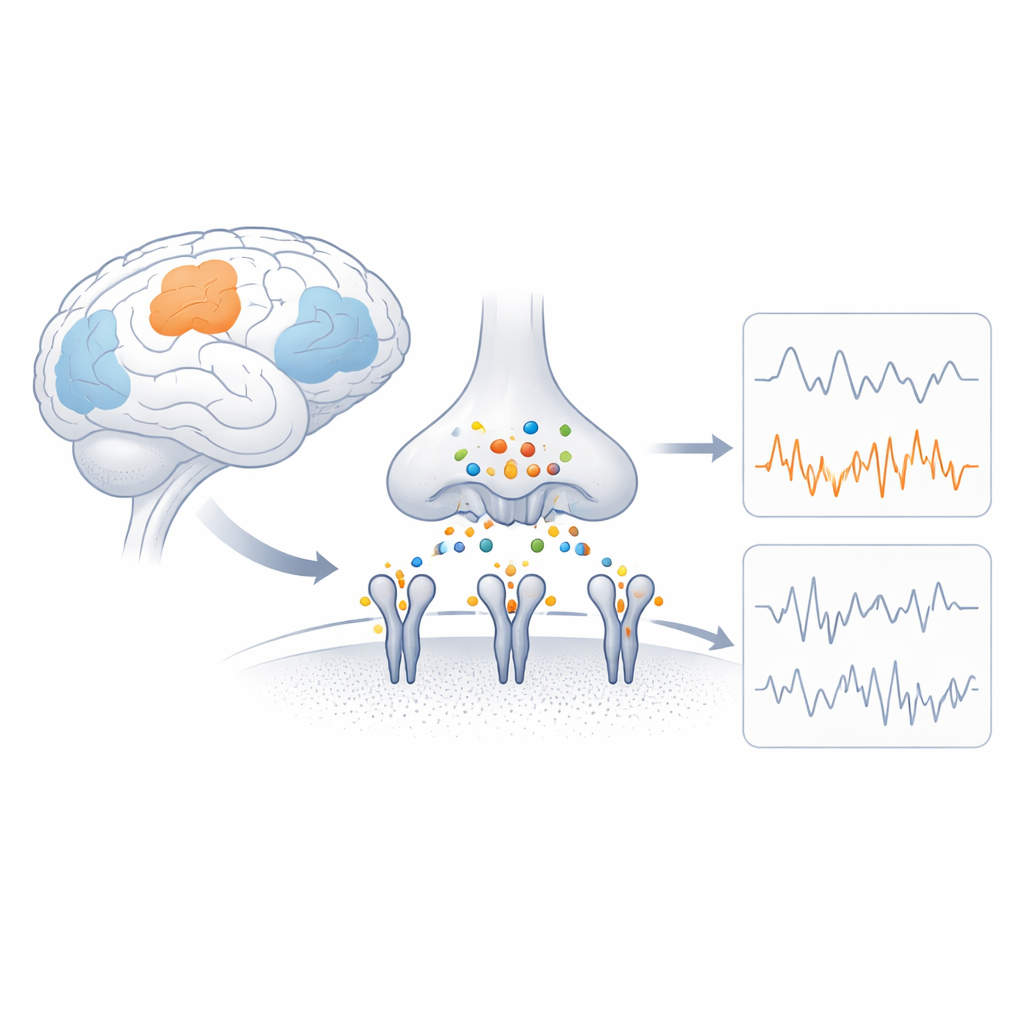
המפסקים המהירים של המוח
קולטני AMPA הם קומפלקסים חלבוניים היושבים בממברנת תאי העצב והופכים אות כימי לזרם חשמלי על‑ידי מתן אפשרות לטעונים לעבור. כל קולטן מורכב מארבע תת‑יחידות קרובות, והתמהיל של תת‑היחידות הללו מעצב עד כמה מהר התעלה נפתחת, כמה זרם היא מעבירה והאם סידן יכול להיכנס. GluA4 היא תת‑יחידה הניתנת לחלחול סידן ושכיחה במיוחד בסוגי תאים מסוימים, כגון נוירונים מעכבים חיוביים לפרוולבומין וכן בניורונים שמיעתיים ומוחוניים מסוימים. מחקרים גנטיים מראים ששינויים מזיקים בגֵן של GluA4 עלולים לגרום לפרכוסים ולבעיות קוגניטיביות, ורמזים אלה מצביעים שתכונותיה המיוחדות קריטיות לתפקוד המוח אך נותרו מסתוריות מבחינה מבנית.
לתפוס את GluA4 בפעולה
כדי לגלות כיצד GluA4 פועל, החוקרים השתמשו במיקרוסקופ אלקטרונים בקריוגנציה (cryo‑EM), טכניקה המצלמת מולקולות מוקפאות באופן מיידי ברזולוציה כמעט אטומית. הם טיהרו קולטנים המורכבים כולם מ‑GluA4 וקושרו בחוזקה לחלבון משלים עזרי בשם TARPγ2, שמקושר באופן טבעי ל‑GluA4 במוח ועוזר לדייק את התנהגותו. הצוות נעץ את הקולטנים במצב פעיל שאינו מדכא באמצעות גלוטמט יחד עם תרופה המונעת את סגירת התעלה. רשומות חשמליות מממברנות מלאכותיות אישרו כי קומפלקסים מטוהרים אלה התנהגו כמו קולטני AMPA אמיתיים, וייצרו פתיחות קצרות וארוכות ברמות זרם מרובות.
ארכיטקטורה גמישה ועדיין שלמה
המפות המבניות הראו שקולטני GluA4 שומרים על פריסת ה‑Y הקלאסית הנראית בקולטני AMPA אחרים: אזור עליון «ראשי» מחוץ לתא החוש את הגלוטמט, וליבה תחתונה שיוצרת את תעלת היונים החוצה את הממברנה. השכבה העליונה ביותר, המכונה תחום האמינו‑טרמינל, התבררה כמגיבה בתנועה מפתיעה, מאמצת מצבים רבים שונים תוך שמירה על מגעים מרכזיים המחזיקים את ארבעת תת‑היחידות יחד. ממצא זה מראה שהשלד החיצוני של GluA4 נשאר שלם אך גמיש באופן חריג, מה שעשוי לאפשר לו אינטראקציה עם חלבוני שותפים מגוונים באזורים שונים במוח מבלי להתפרק.
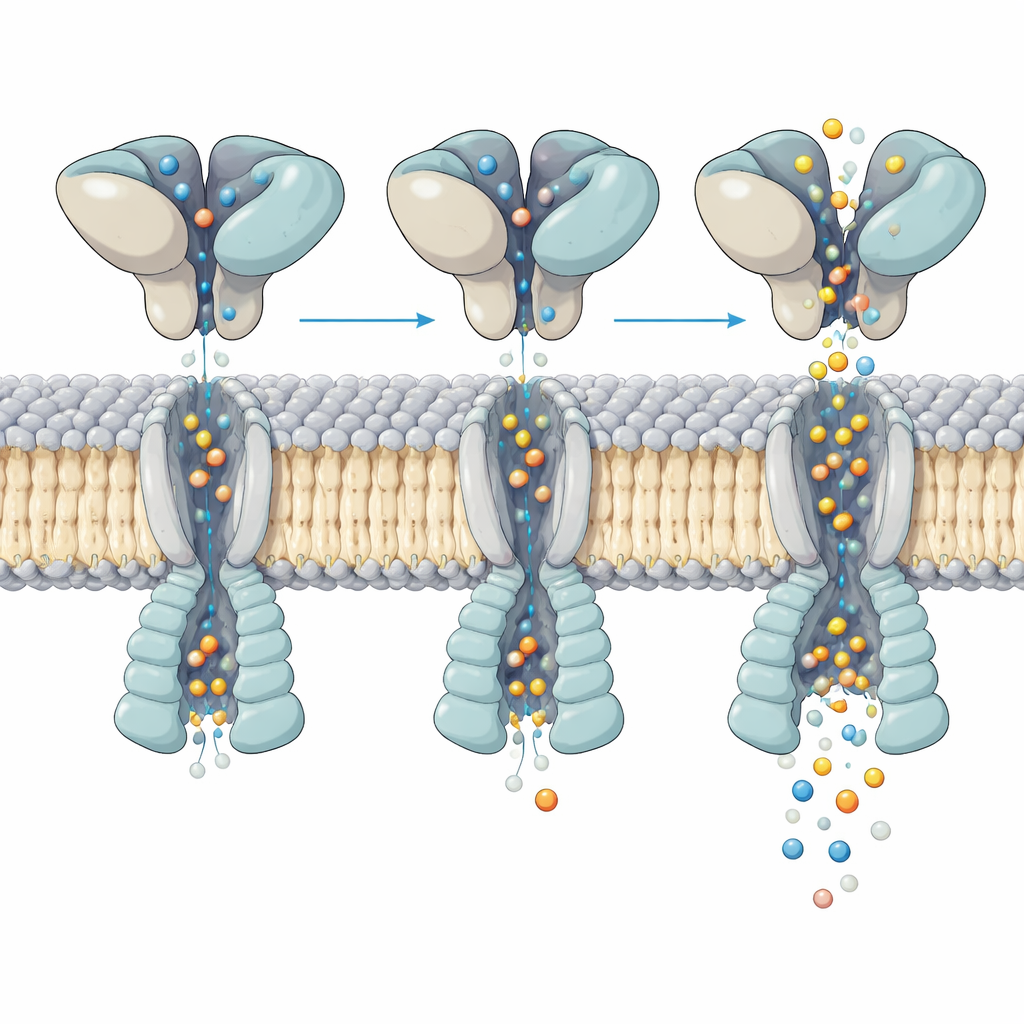
כיצד שינוי צורה שולט בזרימת היונים
בדיקה מעמיקה יותר של התעלה הפעילה חשפה כיצד תנועה בשכבת הקליטה של הגלוטמט שמעל מתורגמת לפתיחת הנקבובית שמתחת. כל ארבע כיסי הקישור היו מלאים בגלוטמט, אך ההליקסים היוצרים את השער כופפו בצורה לא אחידה, אסימטרית, בין ארבעת תת‑היחידות. באמצעות ניתוח של מאות אלפי חלקיקים, הקבוצה הבדילה חמש "מצבי משנה" מובחנים של אותו קולטן מאוקטב. בכל מצב משנה, התחומים העליונים נוטים ומסתובבים במקצת ביחס לליבת הממברנה, וסידור קטן זה מזיז היכן ובאיזה כוח ההליקסים המרכזיים מתעקמים בתוך הנקבובית. הבדלים עדינים אלה משנים את רוחב הנקבובית בנקודות קריטיות, ומתאימים לרמות ההולכה המרובות שנצפו ברישומי תעלה יחידה, אף על פי שעומס הגלוטמט זהה.
קישור מבנה לווריאנטים קשורים למחלות
המחקר מזהה כמעט כל חומצת אמינו במקטע קצר ושמורות מאוד של ההליקס היוצר את הנקבובית כנקודה שיכולה לשמש בציר כיפוף. מספר עמדות אלו הן בדיוק אותן נקודות שבהן נמצאו מוטציות מיטלדות במחלת אדם ב‑GluA4 בחולים עם אפילפסיה וליקויים אינטלקטואליים. החוקרים מציעים שהווריאנטים הללו סביר שישנו את קלות הכיפוף של ההליקס, וישנו את האיזון בין תתי‑הרמות של פתיחת התעלה או ישפיעו על גישת הסידן לאתר קשירה סמוך. למעשה, שינויים זעירים באזור הציר הזה עשויים לכוון יתר או חוסר כיוון של האות החשמלי המועבר על‑ידי קולטנים המכילים GluA4, עם השלכות משמעותיות על מעגלים עצביים התלויים בירי מהיר ומדויק מאוד.
מה המשמעות לבריאות המוח
על‑ידי הראיה ש‑GluA4 יציב מבחינה מבנית ובו‑בעת גמיש בצורה לא שגרתית, עבודה זו משנה את האופן שבו מדענים חושבים על תפקוד קולטני AMPA. במקום לראות רמות זרם שונות כתוצאה פשוטה של כמה מולקולות גלוטמט קשורות, הממצאים תומכים בתמונה שבה קולטן מלא לחלוטין עדיין יכול לדגום מצבים קונפורמציונליים מרובים, שלכל אחד מהם פתיחת נקבובית שונה. "גמישות קונפורמציונלית" זו נותנת הסבר מבני לתגובות המדורגות של תעלות GluA4 ומציעה דרכים חדשות שבהן תרופות או חלבוני שותף עשויים לכוונן את פעילותן. בטווח הארוך, מיפוי שינויים זעירים אלה בצורתם עשוי לכוון טיפולים להפרעות שבהן GluA4 הוא שחקן מרכזי — מאפילפסיות מסוימות ועד שינויים מעגליים בהפרעות פסיכיאטריות ובאותות מוחיים הקשורים בסרטן.
ציטוט: Hale, W.D., Wang, H., Huganir, R.L. et al. Structural basis for activation and conformational plasticity of the GluA4 AMPA receptor. Nat Commun 17, 2932 (2026). https://doi.org/10.1038/s41467-026-68953-9
מילות מפתח: קולטן AMPA, GluA4, העברה סינפטית, מיקרוסקופ אלקטרונים בקפוא, פתיחת תעלת יון