Clear Sky Science · fr
Base structurelle de l’activation et de la plasticité conformationnelle du récepteur AMPA GluA4
Pourquoi ce canal cérébral est important
Chaque pensée, mémoire et mouvement de votre corps dépend de minuscules signaux électriques qui transitent entre les cellules nerveuses. Beaucoup de ces signaux sont portés par les récepteurs AMPA, des « portes » moléculaires qui s’ouvrent lorsqu’elles détectent le messager chimique glutamate. Cette étude se concentre sur une version rare de cette porte, appelée GluA4, qui est concentrée dans les cellules cérébrales à décharge rapide et dans le cervelet. Comme des altérations de GluA4 ont été associées à l’épilepsie, à la déficience intellectuelle et même à des tumeurs cérébrales, comprendre le fonctionnement de ce récepteur au niveau atomique pourrait révéler pourquoi il est si influent — et comment il pourrait être ciblé par de futurs médicaments.
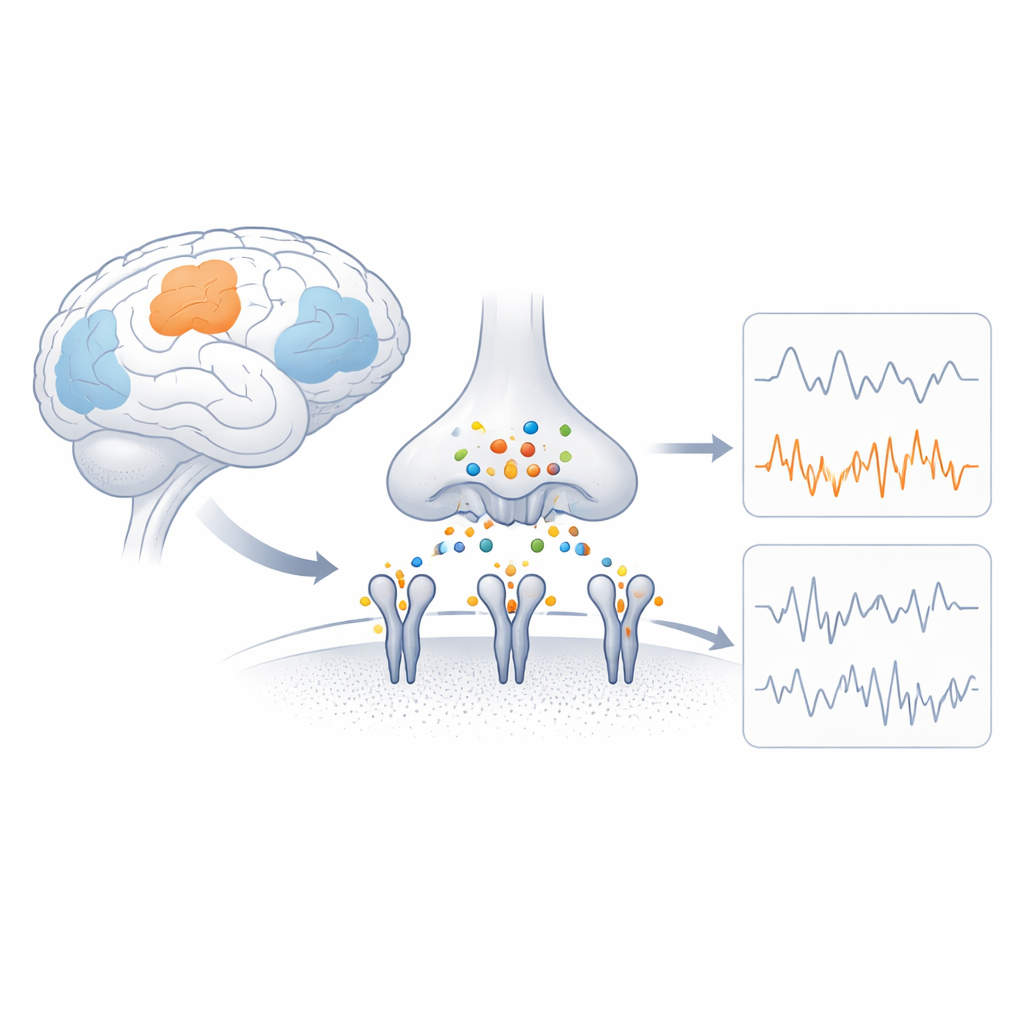
Les commutateurs rapides du cerveau
Les récepteurs AMPA sont des complexes protéiques qui siègent dans la membrane des neurones et convertissent un signal chimique en courant électrique en laissant circuler des particules chargées. Chaque récepteur est construit à partir de quatre parties apparentées (sous‑unités), et la combinaison de ces sous‑unités détermine la rapidité d’ouverture du canal, l’intensité du courant qu’il laisse passer et la perméabilité au calcium. GluA4 est une sous‑unité perméable au calcium, inhabituelle par son abondance dans certains types cellulaires, comme les neurones inhibiteurs parvalbumine‑positifs et certains neurones auditifs et cérébelleux. Des études génétiques montrent que des altérations délétères du gène codant GluA4 peuvent provoquer des crises et des troubles cognitifs, suggérant que ses propriétés particulières sont cruciales pour la fonction cérébrale tout en restant structurellement mystérieuses.
Capturer GluA4 en action
Pour révéler le fonctionnement de GluA4, les chercheurs ont utilisé la cryo‑microscopie électronique, une technique qui image des molécules vitrifiées à une résolution proche de l’atomique. Ils ont purifié des récepteurs composés uniquement de GluA4 et étroitement associés à une protéine auxiliaire nommée TARPγ2, qui s’associe naturellement à GluA4 dans le cerveau et module finement son comportement. L’équipe a verrouillé les récepteurs dans un état actif non désensibilisé en utilisant du glutamate associé à un médicament empêchant la fermeture du canal. Des enregistrements électriques réalisés sur membranes artificielles ont confirmé que ces complexes purifiés se comportaient comme de vrais récepteurs AMPA, présentant des ouvertures brèves et longues avec plusieurs niveaux de courant.
Une architecture flexible mais intacte
Les cartes structurales ont révélé que les récepteurs GluA4 conservent la disposition classique en Y observée chez d’autres récepteurs AMPA : une région supérieure « tête » extracellulaire qui détecte le glutamate, et un noyau inférieur qui forme le canal ionique à travers la membrane. La couche la plus haute, appelée domaine amino‑terminal, s’est avérée étonnamment mobile, adoptant de nombreuses positions différentes tout en maintenant des contacts clés qui maintiennent les quatre sous‑unités ensemble. Cela montre que l’armature externe de GluA4 est intacte mais très flexible, ce qui lui permettrait d’interagir avec divers partenaires protéiques dans différentes régions du cerveau sans se désintégrer.
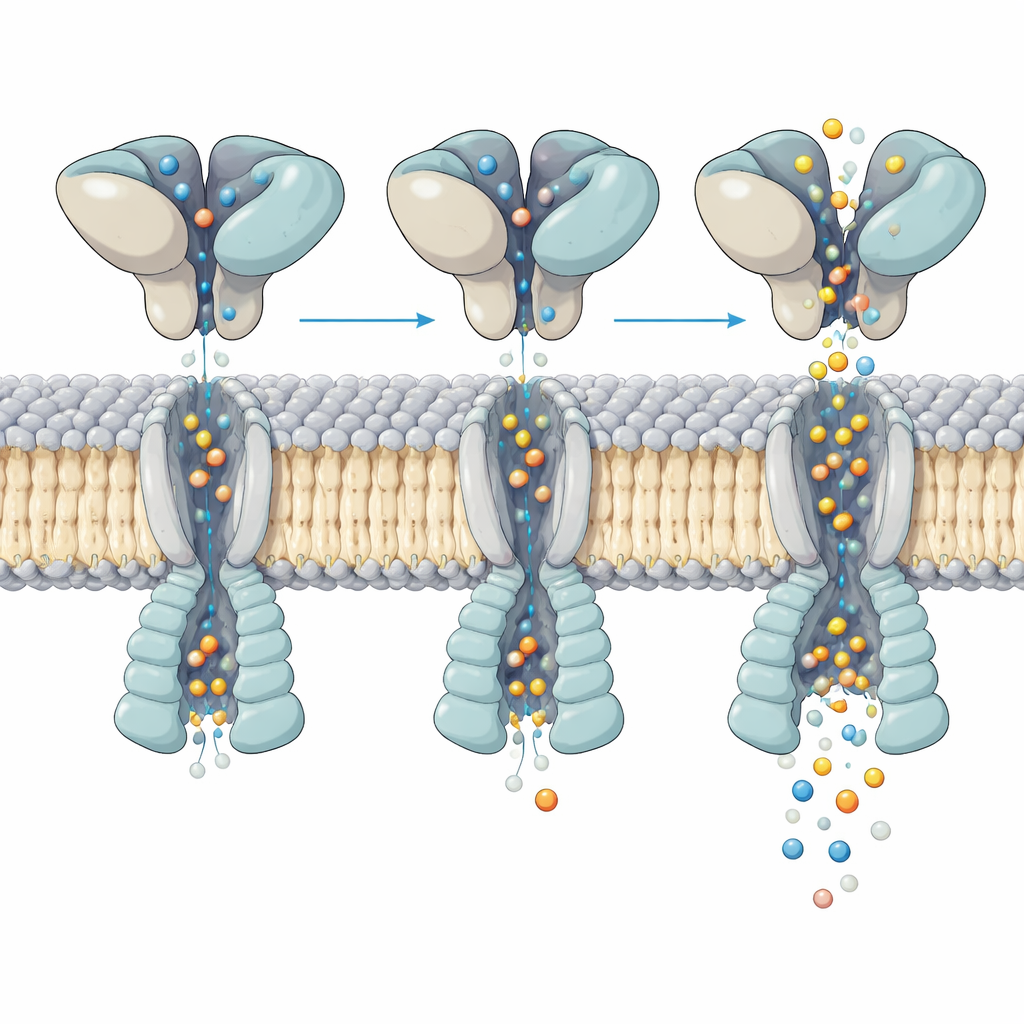
Comment le changement de forme contrôle le flux d’ions
Un examen plus attentif du canal activé a mis au jour la manière dont le mouvement dans la couche de liaison au glutamate au‑dessus se traduit en ouverture du pore en dessous. Les quatre poches de liaison étaient remplies de glutamate, et pourtant les hélices qui forment la porte se sont incurvées de façon inégale et asymétrique entre les quatre sous‑unités. En analysant des centaines de milliers de particules, l’équipe a résolu cinq « sous‑états » distincts du même récepteur activé. Dans chaque sous‑état, les domaines supérieurs basculent et se tordent légèrement par rapport au noyau membranaire, et ce petit réarrangement déplace l’endroit et l’intensité où des hélices clés se plient au sein du pore. Ces différences subtiles modifient la largeur du pore à des points critiques, ce qui correspond aux niveaux de conductance multiples observés dans les enregistrements d’un seul canal, même si l’occupation par le glutamate est identique.
Relier la structure aux variantes liées à la maladie
L’étude identifie presque tous les acides aminés d’un court segment hautement conservé de l’hélice formant le pore comme susceptibles de servir de charnière de flexion. Plusieurs de ces positions correspondent précisément à des mutations pathogènes observées chez des patients porteurs de variants de GluA4 impliqués dans l’épilepsie et la déficience intellectuelle. Les auteurs proposent que ces variantes modifient probablement la facilité avec laquelle l’hélice peut se plier, décalant l’équilibre entre les sous‑niveaux d’ouverture du canal ou changeant l’accès au calcium vers un site de liaison adjacent. En pratique, de petites altérations dans cette zone‑charnière pourraient sur‑ ou sous‑régler le signal électrique porté par les récepteurs contenant GluA4, avec des conséquences majeures pour les circuits neuronaux qui dépendent d’une décharge extrêmement rapide et précise.
Ce que cela signifie pour la santé cérébrale
En montrant que GluA4 est à la fois structurellement stable et exceptionnellement flexible en conformation, ce travail reconfigure la façon dont les scientifiques perçoivent la fonction des récepteurs AMPA. Plutôt que de considérer les différents niveaux de courant comme simplement le résultat du nombre de molécules de glutamate liées, les résultats soutiennent l’idée qu’un récepteur pleinement chargé peut néanmoins explorer plusieurs conformations, chacune avec une ouverture de pore distincte. Cette « plasticité conformationnelle » fournit une explication structurelle aux réponses graduées des canaux GluA4 et suggère de nouvelles façons dont des médicaments ou des protéines partenaires pourraient régler leur activité. À long terme, cartographier ces changements microscopiques de forme pourrait guider des thérapies pour des troubles où GluA4 joue un rôle clé — des épilepsies particulières aux altérations de circuits dans les maladies psychiatriques et la signalisation cérébrale liée au cancer.
Citation: Hale, W.D., Wang, H., Huganir, R.L. et al. Structural basis for activation and conformational plasticity of the GluA4 AMPA receptor. Nat Commun 17, 2932 (2026). https://doi.org/10.1038/s41467-026-68953-9
Mots-clés: Récepteur AMPA, GluA4, transmission synaptique, cryo‑microscopie électronique, ouverture du canal ionique