Clear Sky Science · sv
Strukturell grund för aktivering och konformationsplasticitet hos GluA4 AMPA‑receptorn
Varför denna hjärnkanal spelar roll
Varje tanke, minne och rörelse i din kropp bygger på små elektriska signaler som passerar mellan nervceller. Många av dessa signaler förmedlas av AMPA‑receptorer, molekylära ”grindar” som öppnas när de känner av budbäraren glutamat. Denna studie fokuserar på en ovanlig variant av den grinden, kallad GluA4, som är koncentrerad i snabbutlösande hjärnceller och i lillhjärnan. Eftersom förändringar i GluA4 har kopplats till epilepsi, intellektuell funktionsnedsättning och till och med hjärntumörer, kan förståelse av hur denna receptor fungerar på atomär nivå avslöja varför den är så potent — och hur den kan bli ett mål för framtida läkemedel.
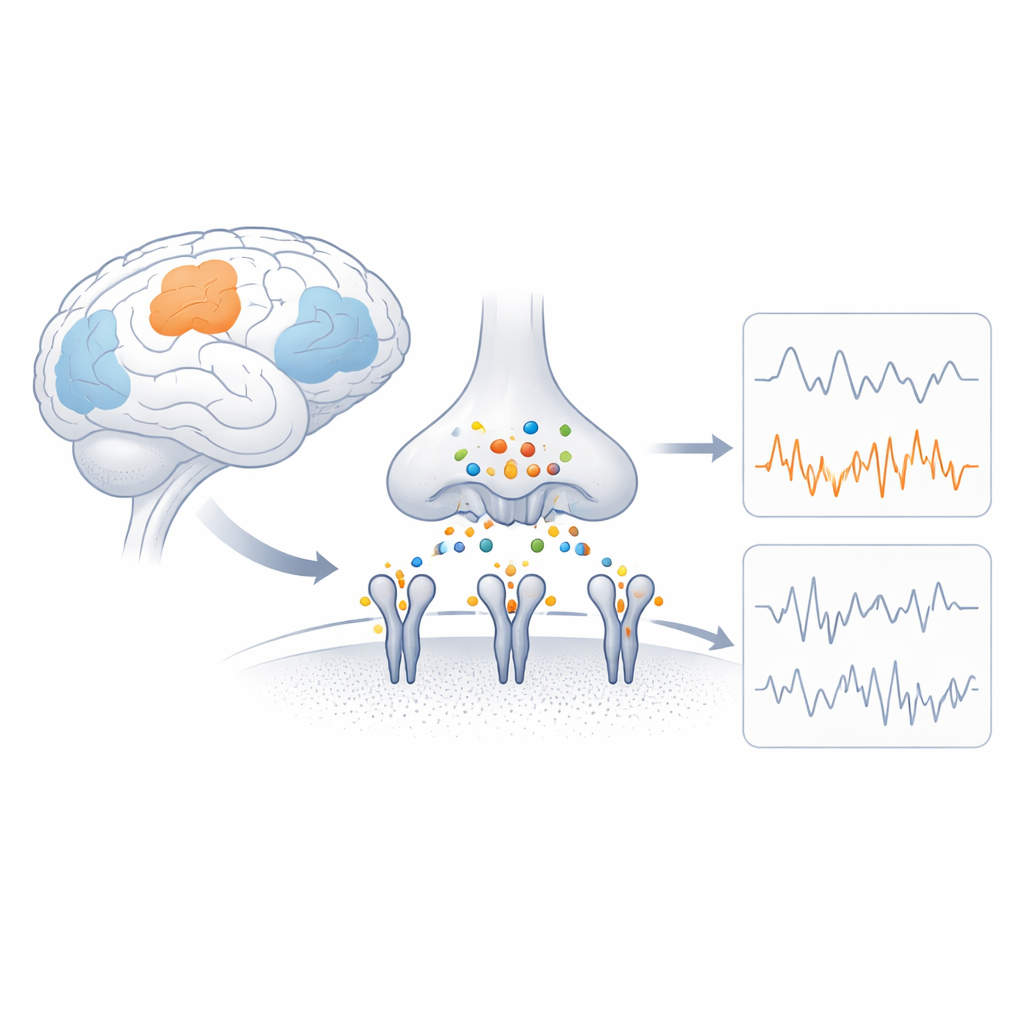
Hjärnans snabba strömbrytare
AMPA‑receptorer är proteinkomplex som sitter i nervcellernas membran och omvandlar en kemisk signal till en elektrisk ström genom att släppa igenom laddade partiklar. Varje receptor byggs av fyra närbesläktade delar (subenheter), och blandningen av dessa subenheter bestämmer hur snabbt kanalen öppnas, hur mycket ström den släpper igenom och om kalcium kan ta sig in. GluA4 är en kalciumpermeabel subenhet som är ovanligt riklig i specifika celltyper, såsom parvalbumin‑positiva inhibitoriska neuroner och vissa auditiva och cerebellära neuroner. Genetiska studier visar att skadliga förändringar i genen för GluA4 kan orsaka anfall och kognitiva problem, vilket antyder att dess särdrag är avgörande för hjärnfunktionen men hittills varit strukturellt oförklarade.
Fånga GluA4 in action
För att avslöja hur GluA4 fungerar använde forskarna kryo‑elektronmikroskopi, en teknik som avbildar blixtfrusna molekyler vid nästan atomär upplösning. De renade receptorer byggda enbart av GluA4 och tätt länkat till en assisterande partnerprotein kallad TARPγ2, som naturligt associerar med GluA4 i hjärnan och finsiktar dess beteende. Gruppen låste receptorerna i ett aktivt, icke‑desensitiserat tillstånd med glutamat tillsammans med ett läkemedel som förhindrar att kanalen stängs av. Elektriska inspelningar från artificiella membran bekräftade att dessa renade komplex beter sig som riktiga AMPA‑receptorer och ger både korta och långa öppningar med flera strömnivåer.
En flexibel men intakt arkitektur
De strukturella kartorna visade att GluA4‑receptorer bibehåller den klassiska Y‑formade layouten som setts hos andra AMPA‑receptorer: en övre ”huvud”region utanför cellen som känner av glutamat, och en nedre kärna som bildar jonkanalen genom membranet. Det översta lagret, kallat aminoterminaldomänen, visade sig vara överraskande rörligt och intog många olika positioner samtidigt som det behöll viktiga kontakter som håller de fyra subenheterna samman. Detta visar att GluA4:s yttre ställning är intakt men mycket flexibel, vilket potentiellt tillåter interaktion med olika partnerproteiner i olika hjärnregioner utan att falla isär.
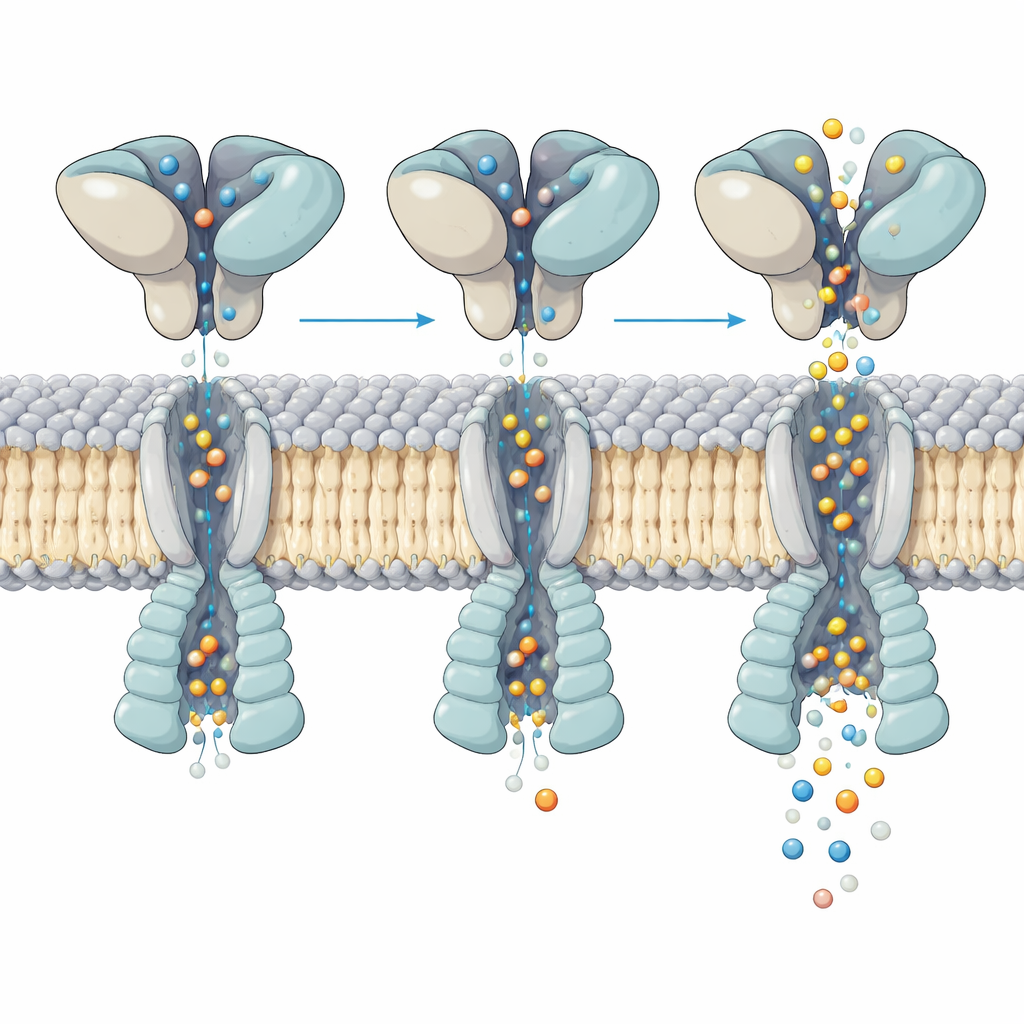
Hur formförändring styr jonflödet
Närmare granskning av den aktiva kanalen visade hur rörelser i glutamatbindande lagret ovanför översätts till öppning av poren nedanför. Alla fyra bindningsfickor var fyllda med glutamat, ändå böjde sig helixarna som bildar grinden på ett ojämnt, asymmetriskt sätt över de fyra subenheterna. Genom att analysera hundratusentals partiklar löste teamet upp fem distinkta ”deltilstånd” av samma aktiverade receptor. I varje deltilstånd gungar och vrider de övre domänerna sig något i förhållande till membrankärnan, och denna lilla omarrangemang förskjuter var och hur kraftigt nyckelhelixar vinklar i poren. Dessa subtila skillnader ändrar porens bredd vid kritiska punkter och motsvarar de flera ledningsnivåerna som ses i enkanalsinspelningar, trots att glutamatupptaget är detsamma.
Koppla struktur till sjukdomsrelaterade varianter
Studien identifierar nästan varje aminosyra i ett kort, högt bevarat avsnitt av pore‑bildande helixen som kapabel att fungera som en böjningsgångjärn. Flera av dessa positioner är exakt där sjukdomsframkallande mutationer i mänskligt GluA4 har upptäckts hos patienter med epilepsi och intellektuell funktionsnedsättning. Författarna föreslår att dessa varianter sannolikt förändrar hur lätt helixen kan vika sig, vilket skiftar balansen mellan delnivåer av kanalöppning eller ändrar kalciumtillgången till en närliggande bindningsplats. I praktiken kan små förändringar i detta gångjärnsområde över‑ eller underjustera den elektriska signalen som förmedlas av GluA4‑innehållande receptorer, med stora konsekvenser för nervkretsar som förlitar sig på extremt snabb och precis avfyrning.
Vad detta betyder för hjärnhälsa
Genom att visa att GluA4 både är strukturellt stabil och ovanligt formflexibel omdefinierar detta arbete hur forskare betraktar AMPA‑receptorernas funktion. Istället för att se olika strömnivåer enbart som ett resultat av hur många glutamatmolekyler som är bundna, stödjer resultaten en bild där en fullastad receptor fortfarande kan prova flera konformationer, var och en med en distinkt poröppning. Denna ”konformationsplasticitet” ger en strukturell förklaring till de graderade responserna hos GluA4‑kanaler och föreslår nya sätt som läkemedel eller partnerproteiner kan finjustera deras aktivitet. På längre sikt kan kartläggning av dessa mikroskopiska formförändringar vägleda terapier för störningar där GluA4 spelar en nyckelroll — från vissa former av epilepsi till kretsförändringar i psykiatriska sjukdomar och cancerrelaterad hjärnsignalering.
Citering: Hale, W.D., Wang, H., Huganir, R.L. et al. Structural basis for activation and conformational plasticity of the GluA4 AMPA receptor. Nat Commun 17, 2932 (2026). https://doi.org/10.1038/s41467-026-68953-9
Nyckelord: AMPA‑receptor, GluA4, synaptisk transmission, kryoelektronmikroskopi, jonkanals‑grindning