Clear Sky Science · ru
Структурная основа активации и конформационной пластичности AMPA‑рецептора GluA4
Почему этот канал мозга важен
Каждая мысль, воспоминание и движение в вашем теле зависят от крошечных электрических сигналов, которые проходят между нервными клетками. Многие из этих сигналов передают AMPA‑рецепторы — молекулярные «ворота», которые открываются при распознавании химического посредника глутамата. В этом исследовании внимание сосредоточено на редкой версии таких ворот, называемой GluA4, которая сосредоточена в быстро‑работающих нейронах и в мозжечке. Поскольку изменения в GluA4 связаны с эпилепсией, умственной отсталостью и даже опухолями мозга, понимание работы этого рецептора на атомном уровне может объяснить, почему он столь силён, — и как на него можно воздействовать будущими лекарствами.
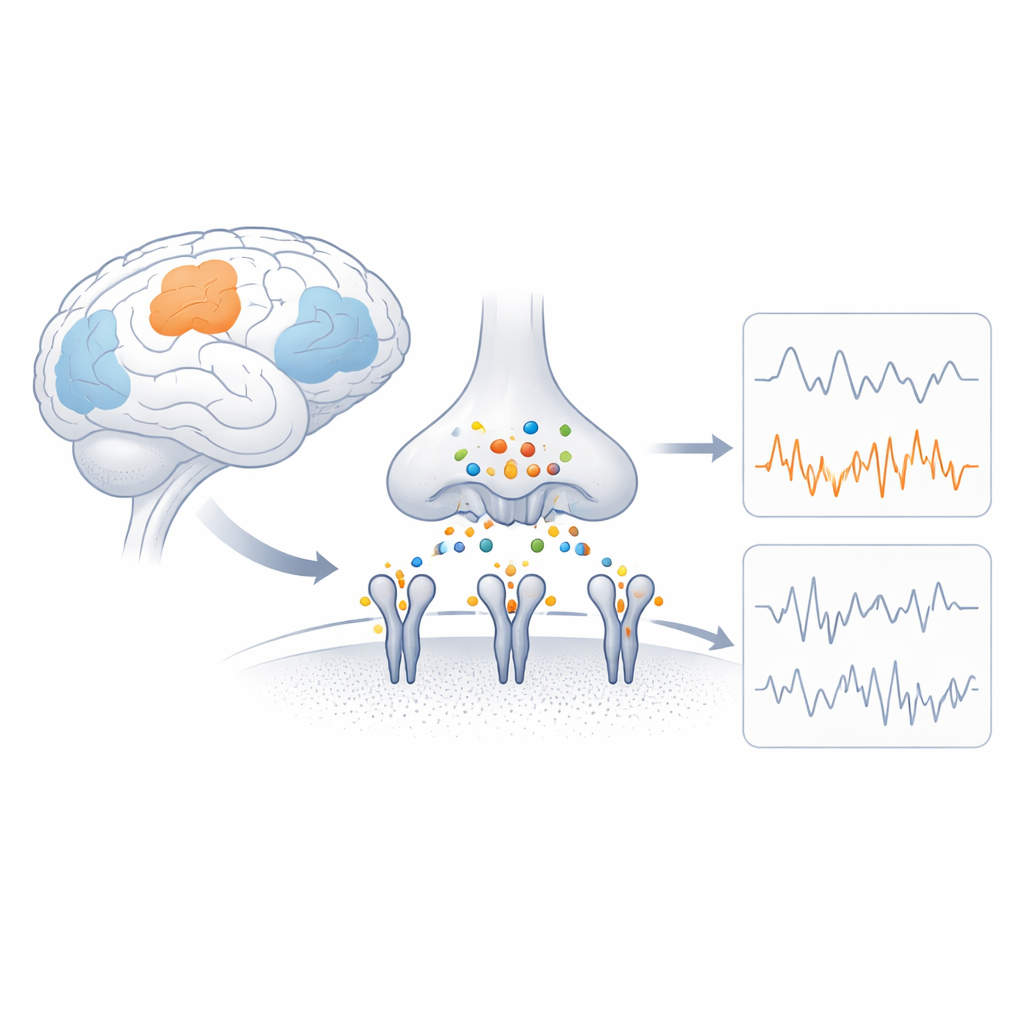
Быстрые переключатели мозга
AMPA‑рецепторы — это белковые комплексы, расположенные в мембране нервных клеток, которые преобразуют химический сигнал в электрический ток, пропуская заряженные частицы. Каждый рецептор состоит из четырёх родственных частей (субъединиц), и сочетание этих субъединиц определяет, как быстро канал открывается, какой ток проходит и может ли проникать кальций. GluA4 — кальций‑проницаемая субъединица, которая необычно богата в определённых типах клеток, таких как парвальбумин‑положительные тормозные нейроны и некоторые слуховые и мозжечковые нейроны. Генетические исследования показывают, что повреждающие изменения в гене GluA4 могут вызывать судороги и когнитивные нарушения, что указывает на то, что её особые свойства критичны для функций мозга, хотя их структурные основы оставались неясными.
Запечатление GluA4 в действии
Чтобы выяснить, как работает GluA4, исследователи использовали крио‑электронную микроскопию — метод, позволяющий получать изображения замороженных молекул с почти атомным разрешением. Они очистили рецепторы, собранные полностью из GluA4 и тесно связанных с вспомогательным партнёром TARPγ2, который естественно ассоциируется с GluA4 в мозге и помогает тонко регулировать её поведение. Команда зафиксировала рецепторы в активном, не десенситизированном состоянии, применив глутамат вместе с препаратом, который препятствует закрытию канала. Электрические записи из искусственных мембран подтвердили, что эти очищенные комплексы ведут себя как реальные AMPA‑рецепторы, демонстрируя короткие и длительные открытия с несколькими уровнями тока.
Гибкая, но цельная архитектура
Структурные карты показали, что рецепторы GluA4 сохраняют классическую Y‑образную схему, наблюдаемую у других AMPA‑рецепторов: верхнюю «головную» область вне клетки, распознающую глутамат, и нижнее ядро, формирующее ионный канал через мембрану. Самый верхний слой, называемый аминно‑терминальным доменом, оказался удивительно подвижным, принимая множество разных положений при сохранении ключевых контактов, удерживающих четыре субъединицы вместе. Это указывает на то, что внешняя опора GluA4 остаётся целой, но сильно гибкой, что, возможно, позволяет ей взаимодействовать с разнообразными партнёрскими белками в разных отделах мозга, не распадаясь.
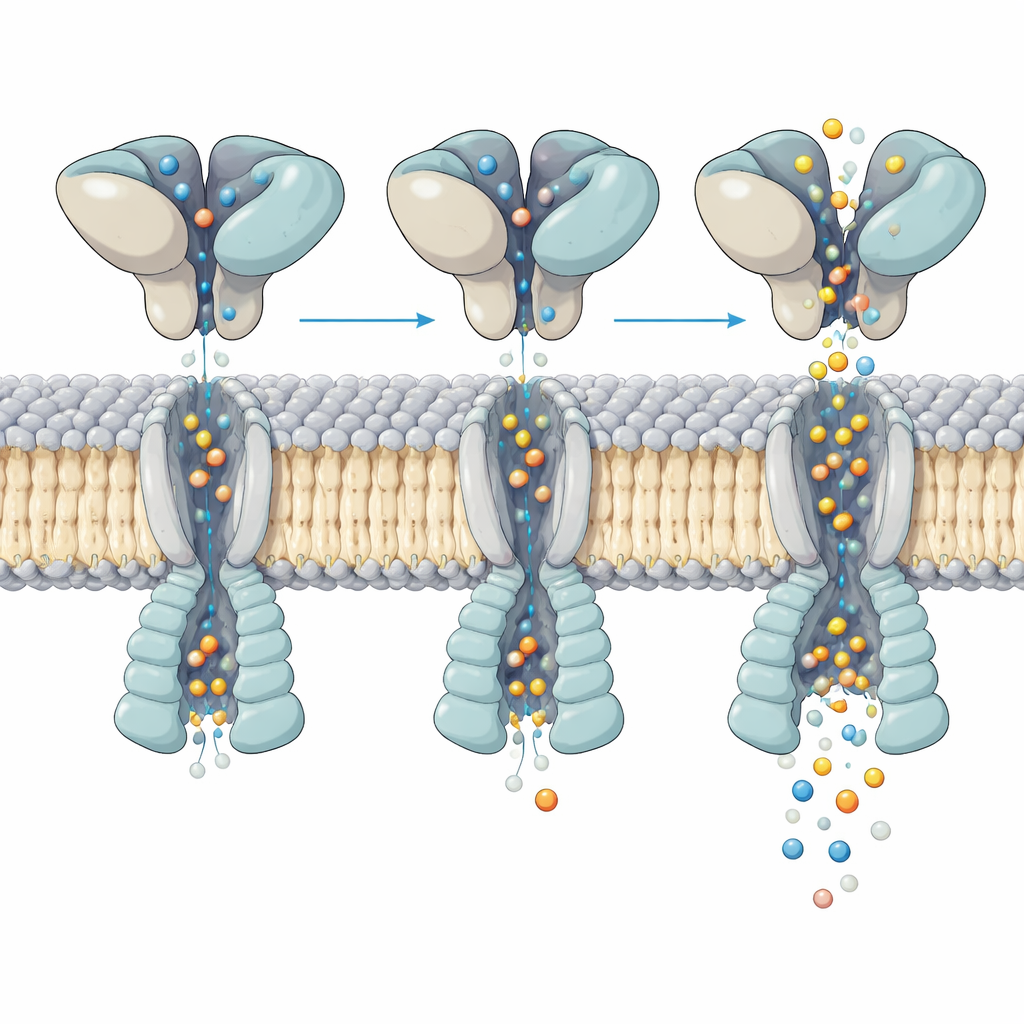
Как изменение формы контролирует поток ионов
Более тщательный осмотр активного канала показал, как движение в слое, связывающем глутамат выше, преобразуется в открытие поры ниже. Все четыре кармана связывания были заполнены глутаматом, однако спирали, формирующие затвор, изгибались неравномерно, асимметрично между субъединицами. Анализ сотен тысяч частиц позволил команде выделить пять различных «подсостояний» одного и того же активированного рецептора. В каждом подсостоянии верхние домены слегка качаются и скручиваются относительно мембранного ядра, и это небольшое перераспределение сдвигает место и силу изгиба ключевых спиралей внутри поры. Эти тонкие различия меняют ширину поры в критических точках, что согласуется с множественными уровнями проводимости в одиночных записях каналов, хотя заполнение глутаматом остаётся одинаковым.
Связывание структуры с вариантами, связанными с болезнями
Исследование выявляет почти каждую аминокислоту в коротком, высококонсервативном участке формирующей пору спирали как потенциальную точку сгиба. Несколько таких позиций совпадают с местами, где у пациентов с эпилепсией и умственной отсталостью обнаружены патогенные варианты человеческого GluA4. Авторы предполагают, что эти варианты, вероятно, изменяют лёгкость, с которой спираль может изгибаться, смещая баланс между подуровнями открытия канала или изменяя доступ кальция к близкому месту связывания. По сути, крошечные изменения в этой зоне‑шарнире могут сверх‑ или недотюнить электрический сигнал, проводимый рецепторами, содержащими GluA4, с серьёзными последствиями для нейронных цепей, зависящих от чрезвычайно быстрой и точной работы.
Что это значит для здоровья мозга
Показав, что GluA4 одновременно структурно стабильна и необычайно гибка по форме, эта работа меняет представление учёных о функционировании AMPA‑рецепторов. Вместо того чтобы рассматривать разные уровни тока просто как следствие числа связанных молекул глутамата, результаты поддерживают картину, в которой полностью загруженный рецептор всё ещё может переходить между несколькими конформациями, каждая из которых соответствует определённому открытию поры. Эта «конформационная пластичность» даёт структурное объяснение градуированных ответов каналов GluA4 и предлагает новые способы, которыми лекарства или партнёрские белки могут регулировать их активность. В перспективе картирование этих микроскопических изменений формы может направлять разработку терапий для расстройств, где GluA4 играет ключевую роль — от некоторых видов эпилепсии до изменений в цепях при психиатрических заболеваниях и сигнальных нарушениях, связанных с раком мозга.
Цитирование: Hale, W.D., Wang, H., Huganir, R.L. et al. Structural basis for activation and conformational plasticity of the GluA4 AMPA receptor. Nat Commun 17, 2932 (2026). https://doi.org/10.1038/s41467-026-68953-9
Ключевые слова: AMPA‑рецептор, GluA4, синаптическая передача, криоэлектронная микроскопия, закрытие и открытие ионного канала