Clear Sky Science · zh
血管周围间充质细胞指示ST2+修复型巨噬细胞促进小鼠血管内皮损伤诱导的新内膜增生
为什么修复受损动脉会适得其反
当医生用微小金属支架打通堵塞的心脏动脉时,通过恢复血流可以挽救生命。但在许多患者中,受治疗的血管会逐渐再次变窄,因为血管壁中的细胞过度增生。本研究在小鼠中探讨了导致这一问题的关键问题:动脉内的哪些细胞决定愈合是平顺进行,还是倾向于有害的过度生长并再次堵塞血管?
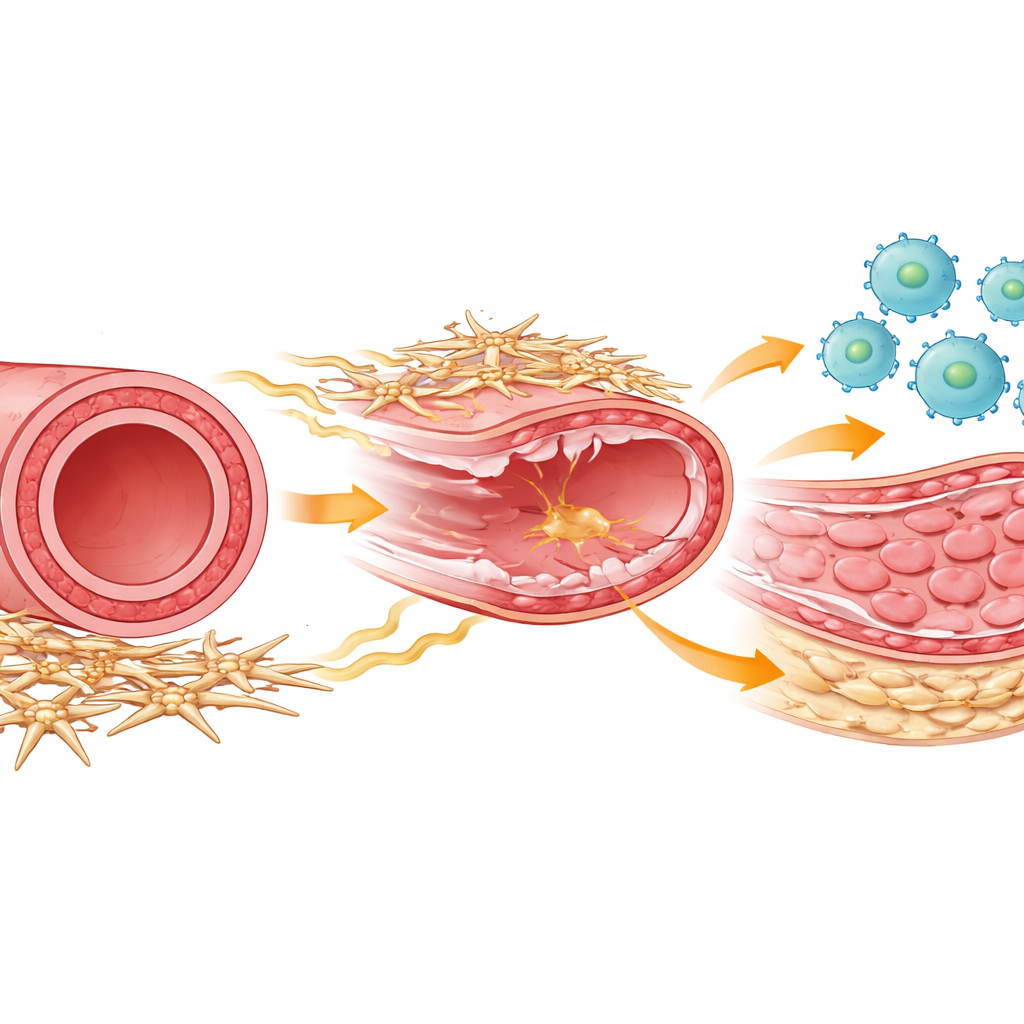
动脉修复中的参与者
在每条动脉内,几种类型的细胞共同工作以修复损伤。被称为巨噬细胞的免疫细胞在损伤后迅速涌入以清除碎屑并协调愈合。平滑肌细胞构成中层肌肉组织,如果开始过度增殖会使血管变厚并变窄。包裹在动脉外侧的是一类不太为人所知的支持细胞,通常称为间充质或基质细胞,它们帮助维持血管结构并通过化学信号与邻近细胞交流。作者使用模拟支架置入时产生刮损损伤的小鼠模型,随后通过强大的单细胞基因测序方法和详尽的细胞谱系分析跟踪这些细胞类型随时间的行为。
从先遣部队到修复队伍
在动脉损伤后不久,免疫细胞大量涌入血管壁,在数天内达到高峰。在这一早期阶段,大多数巨噬细胞表现出经典的“炎症”特征,适合应对危险信号。但到大约一周时,另一类巨噬细胞占主导:一种倾向于重建组织并促进平滑肌生长的修复型。研究人员通过表面标志和时间点区分了这些群体,并显示炎症型和修复型巨噬细胞大多来自于被招募自血液的循环单核细胞。当他们在后期修复阶段实验性清除巨噬细胞时,平滑肌细胞的分裂明显下降,新生的异常内膜未能形成,这证明了这些后期到达的修复导向巨噬细胞对可导致再次堵塞的增厚是必需的。
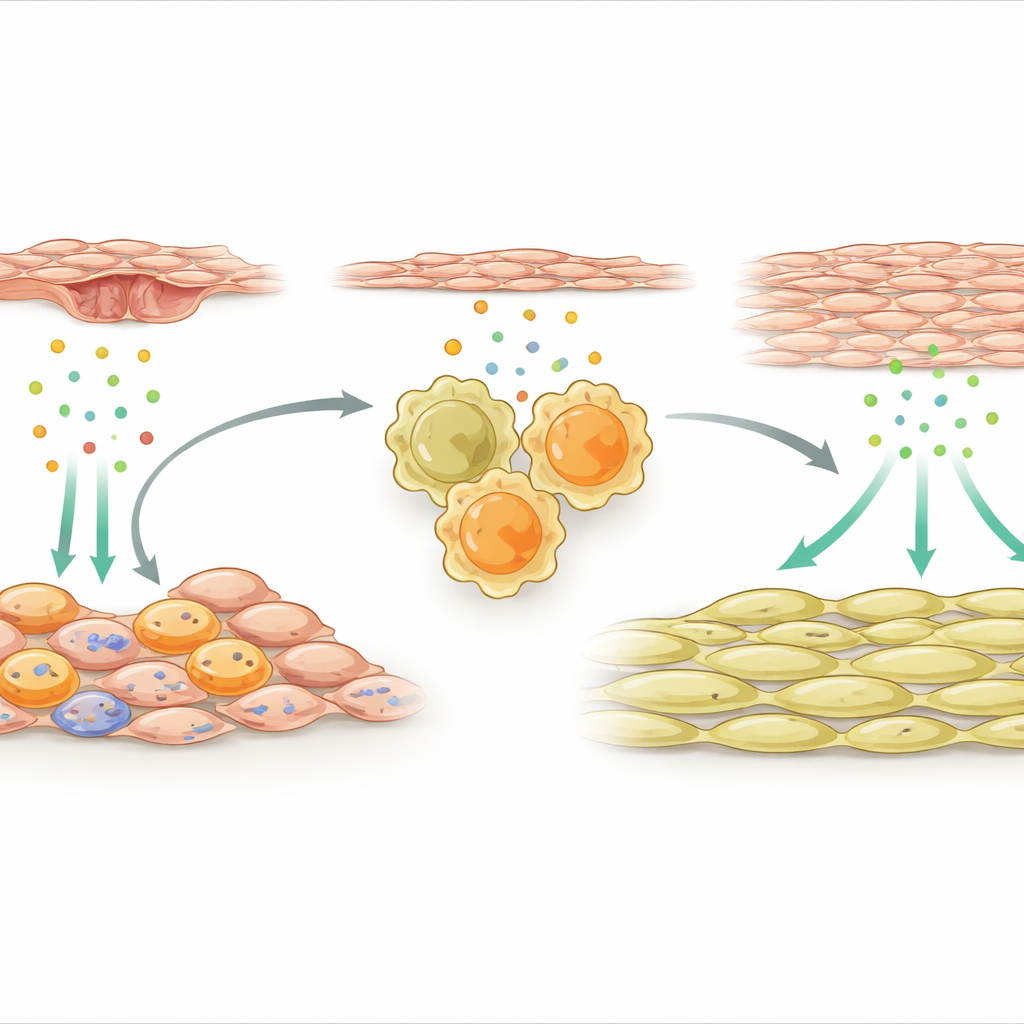
激活修复型巨噬细胞的支持细胞
研究团队随后转向包裹血管的外层支持细胞。损伤后,这类间充质细胞的一个特化亚群变得高度活跃并开始表达许多免疫相关基因。其中一个信号尤为突出:IL-33,一种由损伤或受压组织释放的应激分子。产生IL-33的这些支持细胞在血管壁中与巨噬细胞聚集在一起。研究人员表明,受损的内皮细胞(即动脉内层)释放的因子在间充质细胞中激活了名为NFκB的分子开关,进而促进了IL-33的产生。在小鼠和支架相关再狭窄的人类患者中,IL-33水平均升高,提示该途径具有临床相关性。
导致血管增厚的化学级联反应
IL-33通过与免疫细胞表面的ST2受体结合发挥作用。研究发现,动脉损伤后,血管壁上许多修复型巨噬细胞表达该受体。当来自外层支持细胞的IL-33刺激ST2阳性的巨噬细胞时,会将它们推向强烈的促修复状态,并促使它们释放另一种蛋白质:骨桥蛋白(osteopontin)。骨桥蛋白随后直接作用于平滑肌细胞,驱动其增殖并在动脉内侧堆积,形成收窄血流通道的增厚层。如果研究者特异性地从间充质细胞中去除IL-33,或从巨噬细胞中去除ST2,或用装载在局部水凝胶中的基因沉默分子阻断骨桥蛋白,平滑肌生长均被抑制,动脉保持更通畅。
保持支架通畅的新思路
对非专业读者来说,核心信息是:支架后有害的再狭窄并非仅仅是平滑肌细胞自身失控的问题,而是由外层血管支持细胞与特定亚群“修复型”巨噬细胞之间的对话所主导。损伤触发支持细胞释放IL-33,激活ST2阳性的巨噬细胞,后者再分泌骨桥蛋白过度刺激平滑肌生长。在损伤部位局部中断这条IL-33–ST2–骨桥蛋白通路可以防止小鼠中过度增厚。这提示未来可以将支架与智能凝胶或涂层配对,微调愈合反应而不是粗暴抑制,从而帮助血管自我修复而不再次闭塞。
引用: Ping, Y., Qin, Z., Huang, X. et al. Perivascular mesenchymal cells instruct ST2+ reparative macrophages to promote endovascular injury-induced neointimal hyperplasia in mice. Nat Commun 17, 3635 (2026). https://doi.org/10.1038/s41467-026-68587-x
关键词: 血管修复, 巨噬细胞, IL-33 信号通路, 再狭窄, 平滑肌细胞