Clear Sky Science · fr
Les cellules mésenchymateuses périvasculaires instruisent les macrophages réparateurs ST2+ pour promouvoir l’hyperplasie néointimale induite par une lésion endovasculaire chez la souris
Pourquoi réparer des artères endommagées peut se retourner contre nous
Lorsque les médecins ouvrent des artères coronaires obstruées avec de petits stents métalliques, ils sauvent des vies en restaurant le flux sanguin. Mais chez de nombreux patients, le vaisseau traité se rétrécit progressivement à nouveau parce que les cellules de la paroi vasculaire repoussent de manière excessive. Cette étude chez la souris pose une question centrale derrière ce problème : quelles cellules à l’intérieur de l’artère décident si la cicatrisation reste maîtrisée ou bascule vers une prolifération nuisible qui peut à nouveau obstruer le vaisseau ?
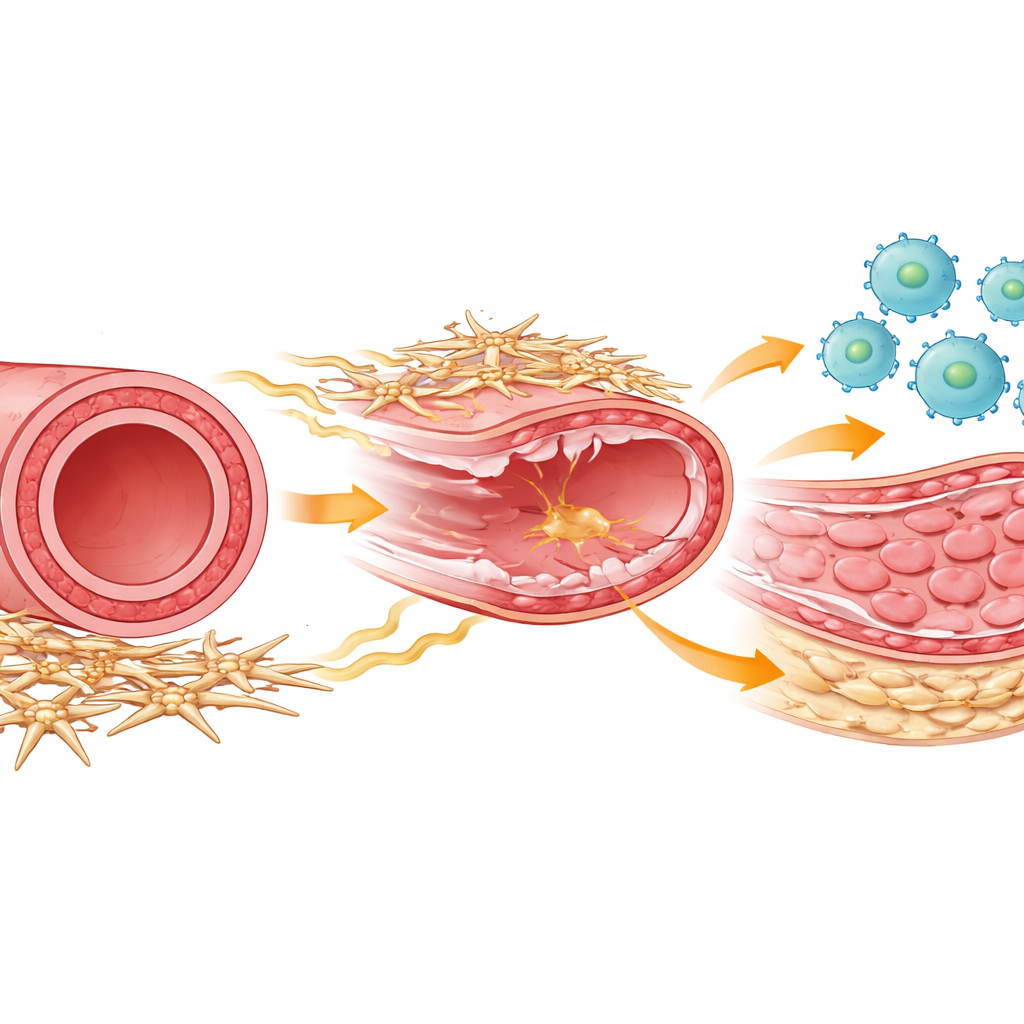
Les acteurs de la réparation artérielle
À l’intérieur de chaque artère, plusieurs types cellulaires coopèrent pour réparer les dégâts. Des cellules immunitaires appelées macrophages affluent après une lésion pour éliminer les débris et coordonner la réparation. Les cellules musculaires lisses forment la couche musculaire intermédiaire qui peut s’épaissir et rétrécir le vaisseau si elles se mettent à proliférer excessivement. Enroulées autour de l’extérieur de l’artère se trouvent des cellules de soutien moins connues, souvent appelées cellules mésenchymateuses ou stromales, qui aident à maintenir la structure du vaisseau et communiquent chimiquement avec les cellules voisines. Les auteurs ont utilisé un modèle murin reproduisant la lésion par raclage causée lors de la pose d’un stent, puis ont suivi le comportement de tous ces types cellulaires au fil du temps en recourant à des méthodes puissantes de lecture génique unicellulaire et à un profilage cellulaire détaillé.
Des premiers intervenants à l’équipe de réparation
Immédiatement après la lésion artérielle, des cellules immunitaires ont envahi la paroi du vaisseau, avec un pic au bout de quelques jours. À ce stade initial, la plupart des macrophages présentaient un profil « inflammatoire » classique, adapté pour combattre les signaux de danger. Mais vers environ une semaine, une autre personnalité de macrophage a dominé : un type réparateur orienté vers la reconstruction tissulaire et l’encouragement de la croissance des cellules musculaires lisses. Les chercheurs ont pu distinguer ces groupes grâce à des marqueurs de surface et au timing, et ont montré que tant les macrophages inflammatoires que réparateurs dérivaient majoritairement de monocytes circulants recrutés depuis le sang. Lorsque les macrophages ont été éliminés expérimentalement pendant la phase réparatrice tardive, la division des cellules musculaires lisses a chuté fortement et la couche interne anormale, ou néointima, n’a pas pu se former, prouvant que ces macrophages orientés réparation, arrivant tardivement, sont nécessaires à l’épaississement susceptible de ré-obstruer les artères.
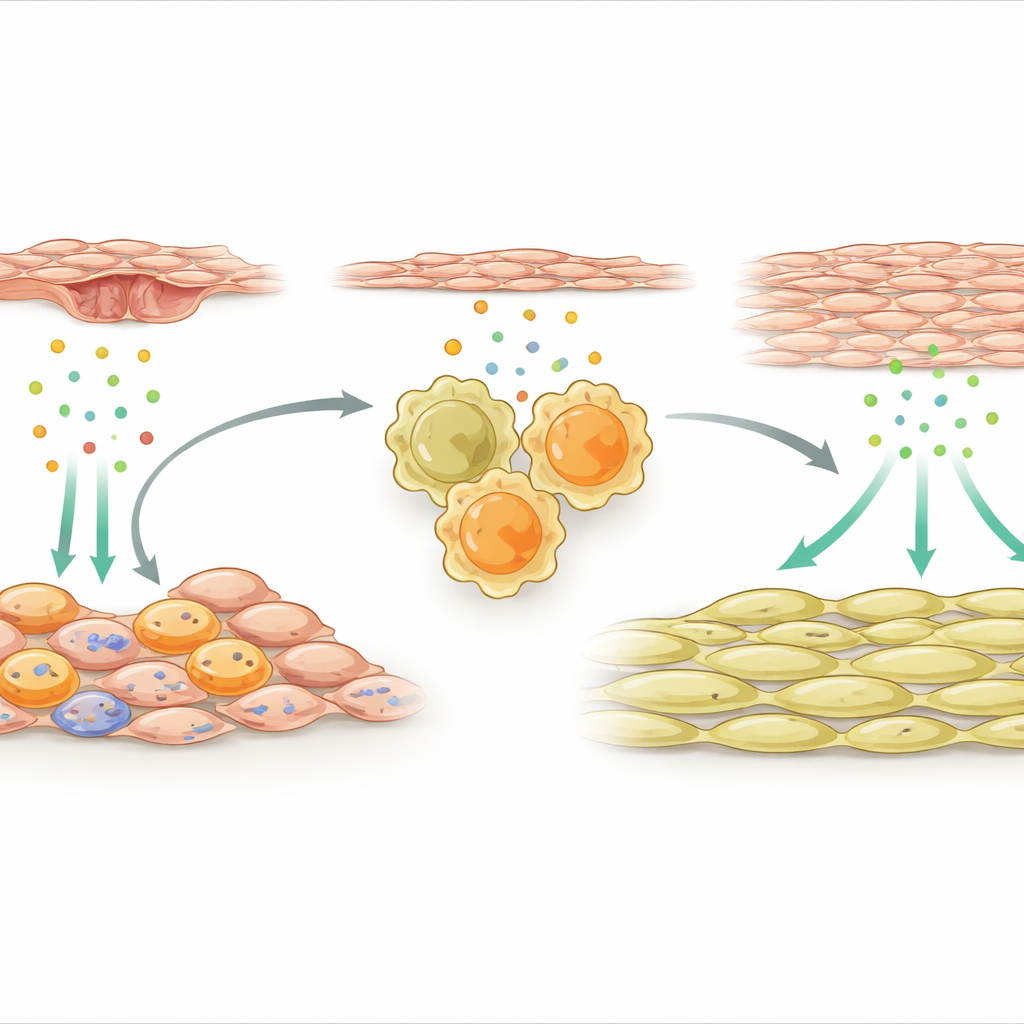
Cellules de soutien qui activent les macrophages de réparation
L’équipe s’est ensuite intéressée aux cellules de soutien externes qui entourent l’artère. Après la lésion, un sous-ensemble spécialisé de ces cellules mésenchymateuses est devenu très actif et a commencé à exprimer de nombreux gènes liés au système immunitaire. Un signal s’est détaché : l’IL-33, une molécule de détresse libérée par des tissus endommagés ou stressés. Ces cellules de soutien productrices d’IL-33 se sont regroupées à proximité des macrophages dans la paroi vasculaire. Les chercheurs ont montré que des facteurs libérés par les cellules endothéliales lésées, la couche interne de l’artère, activaient un interrupteur moléculaire appelé NFκB dans les cellules mésenchymateuses, ce qui augmentait à son tour la production d’IL-33. Tant chez la souris que chez des patients humains présentant une resténose liée aux stents, les niveaux d’IL-33 étaient élevés, suggérant que cette voie est cliniquement pertinente.
Une chaîne chimique menant à l’épaississement du vaisseau
L’IL-33 agit en se liant à un récepteur appelé ST2 sur les cellules immunitaires. L’étude a révélé qu’après une lésion artérielle, de nombreux macrophages réparateurs présents dans la paroi portaient ce récepteur. Lorsque l’IL-33 issue des cellules de soutien externes a stimulé les macrophages ST2-positifs, elle les a poussés vers un état fortement pro-réparateur et les a amenés à libérer une autre protéine, l’ostéopontine. L’ostéopontine a ensuite agi directement sur les cellules musculaires lisses, les incitant à proliférer et à s’accumuler à l’intérieur de l’artère, créant une couche épaissie qui rétrécit le canal de flux sanguin. Si les chercheurs ont supprimé l’IL-33 spécifiquement dans les cellules mésenchymateuses, ou retiré ST2 des macrophages, ou neutralisé l’ostéopontine avec des molécules de silencage génique encapsulées dans un hydrogel local, la croissance des cellules musculaires lisses était limitée et l’artère restait plus ouverte.
Nouvelles pistes pour maintenir les stents perméables
Pour les non-spécialistes, le message central est que la resténose nuisible après pose de stent n’est pas seulement un problème de cellules musculaires lisses qui se comportent mal de façon autonome. Elle est orchestrée par une conversation entre les cellules de soutien externes du vaisseau et un sous-ensemble particulier de macrophages « réparateurs ». La lésion déclenche la libération d’IL-33 par les cellules de soutien, qui active les macrophages ST2-positifs, lesquels sécrètent ensuite de l’ostéopontine pour surexciter la croissance des cellules musculaires lisses. Interrompre localement cette chaîne IL-33–ST2–ostéopontine au niveau de la lésion a empêché l’épaississement excessif chez la souris. Cela suggère un avenir où les stents pourraient être associés à des gels ou des revêtements intelligents qui ajustent finement la réparation plutôt que de la supprimer brutalement, aidant les artères à se réparer sans se refermer à nouveau.
Citation: Ping, Y., Qin, Z., Huang, X. et al. Perivascular mesenchymal cells instruct ST2+ reparative macrophages to promote endovascular injury-induced neointimal hyperplasia in mice. Nat Commun 17, 3635 (2026). https://doi.org/10.1038/s41467-026-68587-x
Mots-clés: réparation vasculaire, macrophages, signalisation IL-33, resténose, cellules musculaires lisses