Clear Sky Science · it
Cellule mesenchimali perivascolari istruiscono macrofagi riparativi ST2+ a promuovere l’ipertrofia neointimale indotta da lesione endovascolare nei topi
Perché riparare arterie danneggiate può avere effetti contrari
Quando i medici aprono arterie coronariche occluse con piccoli stent metallici, salvano vite ripristinando il flusso sanguigno. Ma in molti pazienti il vaso trattato si restringe di nuovo lentamente perché le cellule della parete vascolare ricrescono in modo eccessivo. Questo studio nei topi affronta una domanda fondamentale dietro a questo problema: quali cellule all’interno dell’arteria decidono se la guarigione resta equilibrata oppure scivola verso una crescita dannosa che può occludere di nuovo il vaso?
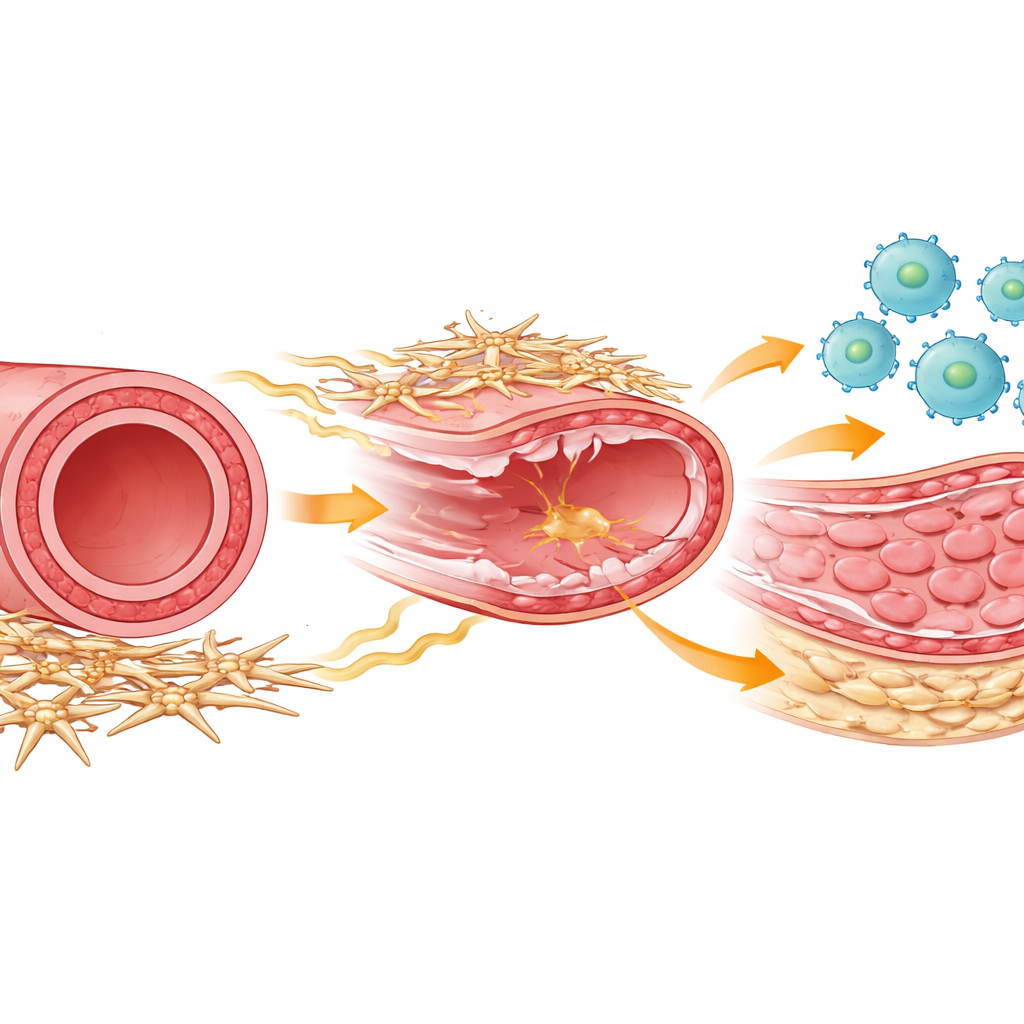
Gli attori della guarigione arteriosa
All’interno di ogni arteria, diversi tipi cellulari collaborano per riparare il danno. Cellule immunitarie chiamate macrofagi accorrono dopo una lesione per rimuovere detriti e coordinare la riparazione. Le cellule muscolari lisce costituiscono lo strato medio muscolare che può ispessirsi e restringere il vaso se comincia a proliferare eccessivamente. Avvolgendo l’esterno dell’arteria si trova un gruppo meno noto di cellule di supporto, spesso chiamate cellule mesenchimali o stromali, che aiutano a mantenere la struttura del vaso e comunicano chimicamente con le cellule vicine. Gli autori hanno usato un modello murino che imita la lesione da raschiamento causata dalla posizionamento di uno stent, quindi hanno seguito il comportamento di tutti questi tipi cellulari nel tempo usando potenti metodi di lettura genica a singola cellula e un profilo dettagliato delle cellule.
Dai primi soccorritori alla squadra di riparazione
Subito dopo la lesione arteriosa, le cellule immunitarie hanno invaso la parete vascolare, raggiungendo un picco in pochi giorni. In questa fase iniziale la maggior parte dei macrofagi mostrava un profilo tipicamente «infiammatorio» adatto a combattere i segnali di pericolo. Ma dopo circa una settimana è emersa una diversa personalità dei macrofagi: un tipo riparativo orientato alla ricostruzione del tessuto e a stimolare la crescita delle cellule muscolari lisce. I ricercatori sono riusciti a separare questi gruppi usando marcatori di superficie e tempistiche, e hanno dimostrato che sia i macrofagi infiammatori sia quelli riparativi derivavano in gran parte da monociti circolanti reclutati dal sangue. Quando hanno rimosso sperimentalmente i macrofagi durante la fase riparativa tardiva, la divisione delle cellule muscolari lisce è diminuita nettamente e lo strato interno anomalo, la neointima, non si è formato, provando che questi macrofagi orientati alla riparazione, arrivati più tardi, sono necessari per l’ispessimento che può ri-ostruire le arterie.
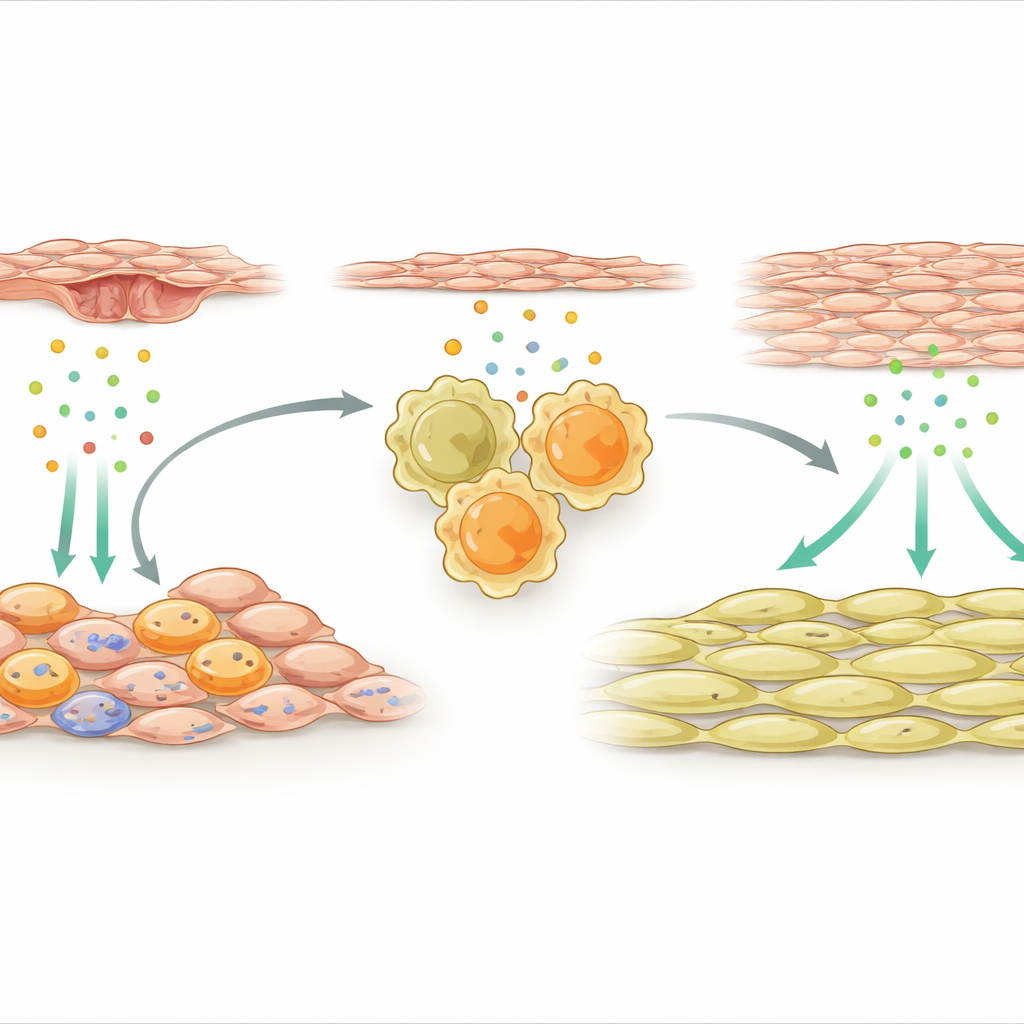
Cellule di supporto che attivano i macrofagi riparativi
Il gruppo si è poi concentrato sulle cellule di supporto esterne che avvolgono l’arteria. Dopo la lesione, un sottogruppo specializzato di queste cellule mesenchimali è diventato altamente attivo ed ha iniziato a esprimere molti geni legati all’immunità. Un segnale è emerso in modo evidente: l’IL-33, una molecola di distress rilasciata da tessuti danneggiati o sotto stress. Queste cellule di supporto produttrici di IL-33 si raggruppavano vicino ai macrofagi nella parete vascolare. I ricercatori hanno dimostrato che fattori rilasciati dalle cellule endoteliali lesionate, il rivestimento interno dell’arteria, attivavano un interruttore molecolare chiamato NFκB nelle cellule mesenchimali, il quale a sua volta aumentava la produzione di IL-33. Sia nei topi sia in pazienti umani con ristrettimento correlato a stent, i livelli di IL-33 risultavano elevati, suggerendo che questa via ha rilevanza clinica.
Una catena chimica verso l’ispessimento del vaso
L’IL-33 agisce legandosi a un recettore noto come ST2 sulle cellule immunitarie. Lo studio ha rilevato che dopo la lesione arteriosa molti dei macrofagi riparativi nella parete esprimevano questo recettore. Quando l’IL-33 prodotto dalle cellule di supporto esterne stimolava i macrofagi ST2-positivi, li spingeva verso uno stato fortemente pro-riparativo e li induceva a rilasciare un’altra proteina, l’osteopontina. L’osteopontina poi agiva direttamente sulle cellule muscolari lisce, inducendole a proliferare e accumularsi all’interno dell’arteria, formando uno strato ispessito che restringe il canale del flusso sanguigno. Se i ricercatori hanno rimosso l’IL-33 specificamente dalle cellule mesenchimali, o eliminato ST2 dai macrofagi, o bloccato l’osteopontina con molecole silenzianti del gene incapsulate in un idrogel locale, la crescita delle cellule muscolari lisce è stata ridotta e l’arteria è rimasta più aperta.
Nuove idee per mantenere gli stent pervi
Per i non specialisti, il messaggio centrale è che il dannoso nuovo restringimento delle arterie dopo lo stenting non è solo un problema di cellule muscolari lisce che si comportano male da sole. Piuttosto, è orchestrato da una conversazione tra le cellule di supporto esterne del vaso e un sottogruppo particolare di macrofagi «riparativi». La lesione induce le cellule di supporto a rilasciare IL-33, che attiva macrofagi ST2-positivi, i quali poi secernono osteopontina per sovrastimolare la crescita delle cellule muscolari lisce. Interrompere localmente questa catena IL-33–ST2–osteopontina nel sito della lesione ha prevenuto l’ispessimento eccessivo nei topi. Ciò suggerisce un futuro in cui gli stent potrebbero essere abbinati a gel o rivestimenti intelligenti che modulano finemente la guarigione invece di sopprimerla in modo indiscriminato, aiutando le arterie a ripararsi senza richiudersi.
Citazione: Ping, Y., Qin, Z., Huang, X. et al. Perivascular mesenchymal cells instruct ST2+ reparative macrophages to promote endovascular injury-induced neointimal hyperplasia in mice. Nat Commun 17, 3635 (2026). https://doi.org/10.1038/s41467-026-68587-x
Parole chiave: riparazione vascolare, macrofagi, segnalazione IL-33, restenosi, cellule muscolari lisce