Clear Sky Science · pt
As células mesenquimais perivasculares instruem macrófagos reparadores ST2+ a promover hiperplasia neointimal induzida por lesão endovascular em camundongos
Por que reparar artérias danificadas pode sair pela culatra
Quando médicos desobstruem artérias coronárias com pequenos stents metálicos, salvam vidas ao restaurar o fluxo sanguíneo. Mas em muitos pacientes, o vaso tratado vai lentamente se estreitando de novo à medida que células da parede vascular crescem de forma excessiva. Este estudo em camundongos investiga uma questão central por trás desse problema: quais células dentro da artéria decidem se a cicatrização permanece controlada ou se desliza para um crescimento prejudicial que pode obstruir o vaso novamente?
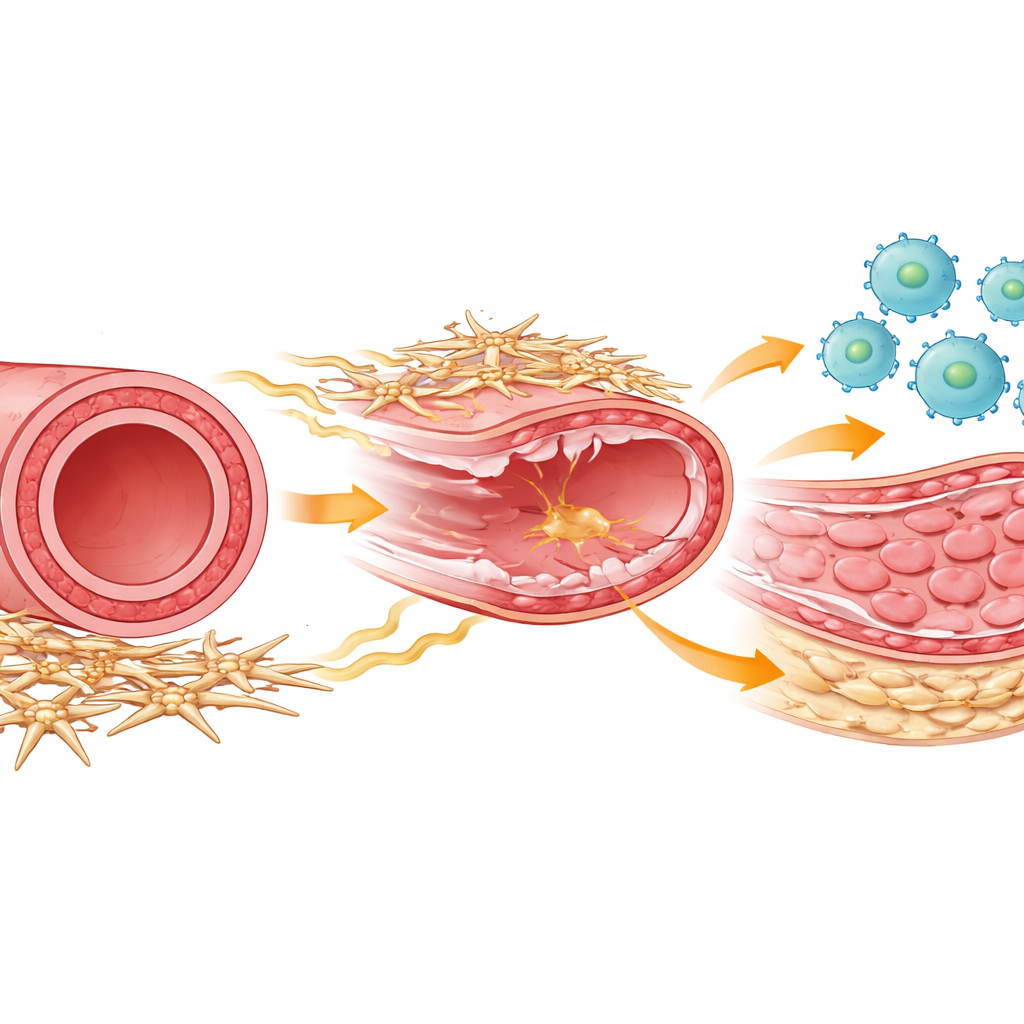
Os protagonistas da cicatrização arterial
No interior de cada artéria, vários tipos celulares trabalham juntos para reparar danos. Células imunes chamadas macrófagos invadem a parede vascular após a lesão para remover detritos e coordenar a reparação. As células musculares lisas formam a camada média muscular que pode se espessar e estreitar o vaso se começarem a proliferar demais. Envolvendo o exterior da artéria há um grupo menos conhecido de células de suporte, frequentemente chamadas de células mesenquimais ou do estroma, que ajudam a manter a estrutura do vaso e se comunicam quimicamente com células vizinhas. Os autores usaram um modelo de camundongo que imita a lesão por raspagem causada pela colocação de um stent e acompanharam como esses tipos celulares se comportaram ao longo do tempo usando métodos poderosos de leitura gênica em célula única e perfis celulares detalhados.
Dos socorristas iniciais à equipe de reparo
Logo após a lesão arterial, células imunes inundaram a parede do vaso, com pico em alguns dias. Nessa fase inicial, a maioria dos macrófagos exibiu um perfil clássico “inflamatório”, adequado para combater sinais de perigo. Mas por volta de uma semana, uma personalidade diferente de macrófago predominou: um tipo reparador voltado para reconstruir tecido e encorajar o crescimento das células musculares lisas. Os pesquisadores conseguiram separar esses grupos usando marcadores de superfície e tempo, e mostraram que tanto os macrófagos inflamatórios quanto os reparadores se originaram majoritariamente de monócitos circulantes recrutados do sangue. Quando eles removeram experimentalmente os macrófagos durante a fase reparadora tardia, a divisão das células musculares lisas caiu drasticamente e a camada interna anormal, ou neointima, deixou de se formar, provando que esses macrófagos orientados ao reparo que chegam mais tarde são necessários para o espessamento que pode reobstruir as artérias.
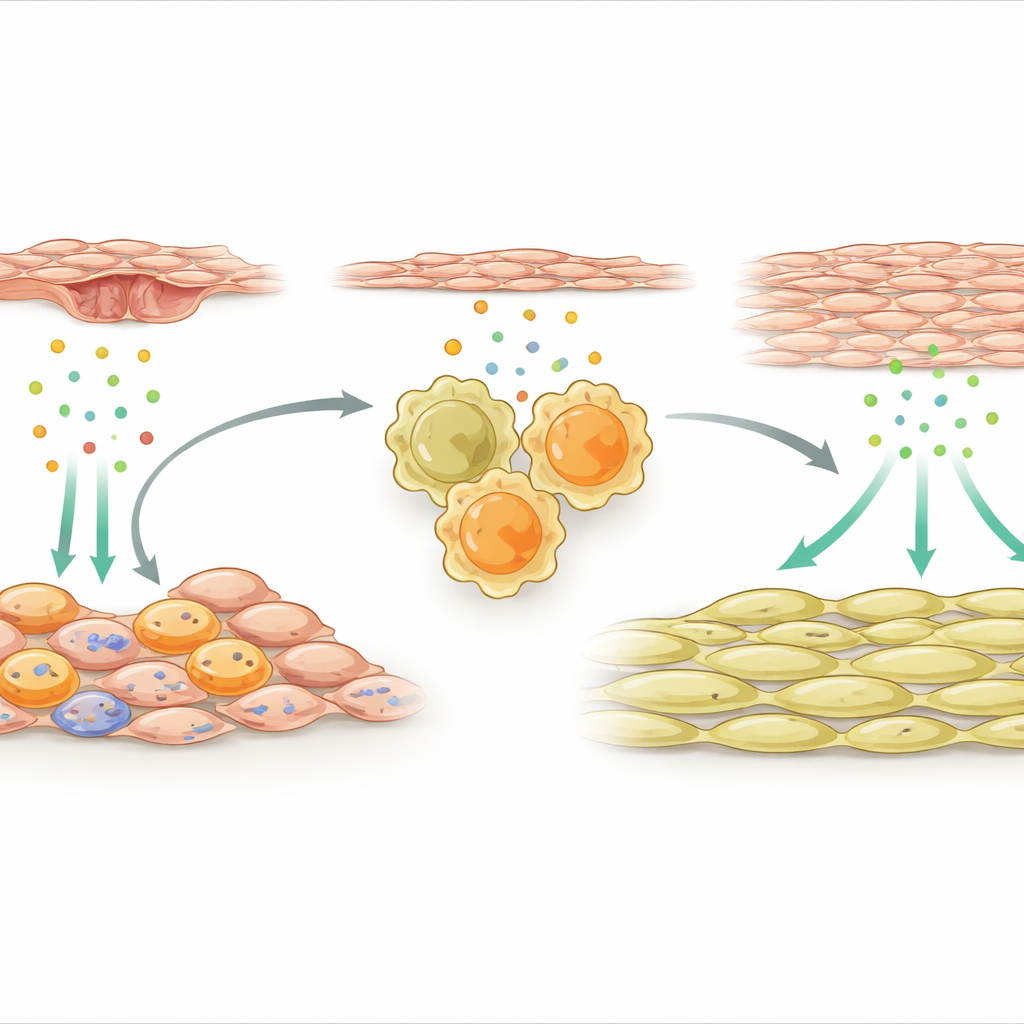
Células de suporte que ativam macrófagos reparadores
A equipe então voltou sua atenção às células de suporte externas que envolvem a artéria. Após a lesão, um subconjunto especializado dessas células mesenquimais tornou-se altamente ativo e começou a expressar muitos genes relacionados ao sistema imune. Um sinal se destacou: IL-33, uma molécula de alarme liberada por tecidos danificados ou estressados. Essas células de suporte produtoras de IL-33 se agruparam próximas aos macrófagos na parede vascular. Os pesquisadores demonstraram que fatores liberados por células endoteliais lesionadas, o revestimento interno da artéria, ativaram um interruptor molecular chamado NFκB nas células mesenquimais, o que por sua vez aumentou a produção de IL-33. Tanto em camundongos quanto em pacientes humanos com reestenose associada a stent, os níveis de IL-33 estavam elevados, sugerindo que essa via tem relevância clínica.
Uma reação em cadeia química rumo ao espessamento vascular
IL-33 atua ao se ligar a um receptor conhecido como ST2 em células imunes. O estudo descobriu que, após a lesão arterial, muitos dos macrófagos reparadores na parede exprimiam esse receptor. Quando IL-33 das células de suporte externas estimulou macrófagos ST2-positivos, isso os empurrou para um modo fortemente pró-reparo e os fez liberar outra proteína, osteopontina. A osteopontina então agiu diretamente sobre as células musculares lisas, induzindo sua proliferação e acúmulo na face interna da artéria, formando uma camada espessada que estreita o canal de fluxo sanguíneo. Se os pesquisadores removeram IL-33 especificamente das células mesenquimais, ou eliminaram ST2 dos macrófagos, ou bloquearam a osteopontina com moléculas de silenciamento gênico entregues em um hidrogel local, o crescimento das células musculares lisas foi contido e a artéria permaneceu mais aberta.
Novas ideias para manter stents permeáveis
Para leigos, a mensagem central é que a reestenose prejudicial após a colocação de stents não é apenas um problema de células musculares lisas se comportando mal por conta própria. Em vez disso, é orquestrada por uma conversa entre as células de suporte externas do vaso e um subconjunto particular de macrófagos “reparadores”. A lesão faz com que as células de suporte liberem IL-33, que ativa macrófagos ST2-positivos, que então secretam osteopontina para superestimular o crescimento das células musculares lisas. Interromper localmente essa cadeia IL-33–ST2–osteopontina no sítio da lesão preveniu o espessamento excessivo em camundongos. Isso sugere um futuro em que stents possam ser associados a géis ou revestimentos inteligentes que ajustem finamente a cicatrização em vez de suprimi-la de forma grosseira, ajudando as artérias a se reparar sem fechar novamente.
Citação: Ping, Y., Qin, Z., Huang, X. et al. Perivascular mesenchymal cells instruct ST2+ reparative macrophages to promote endovascular injury-induced neointimal hyperplasia in mice. Nat Commun 17, 3635 (2026). https://doi.org/10.1038/s41467-026-68587-x
Palavras-chave: reparo vascular, macrófagos, sinalização IL-33, reestenose, células musculares lisas