Clear Sky Science · es
Las células mesenquimales perivasculares instruyen a macrófagos reparadores ST2+ para promover la hiperplasia neointimal inducida por lesión endovascular en ratones
Por qué reparar arterias dañadas puede salir mal
Cuando los médicos abren arterias coronarias obstruidas con pequeños stents metálicos, salvan vidas al restaurar el flujo sanguíneo. Pero en muchos pacientes, el vaso tratado se estrecha de nuevo lentamente porque las células de la pared vascular proliferan de forma excesiva. Este estudio en ratones plantea una cuestión clave detrás de ese problema: ¿qué células dentro de la arteria deciden si la reparación permanece controlada o deriva en un crecimiento dañino que puede volver a obstruir el vaso?
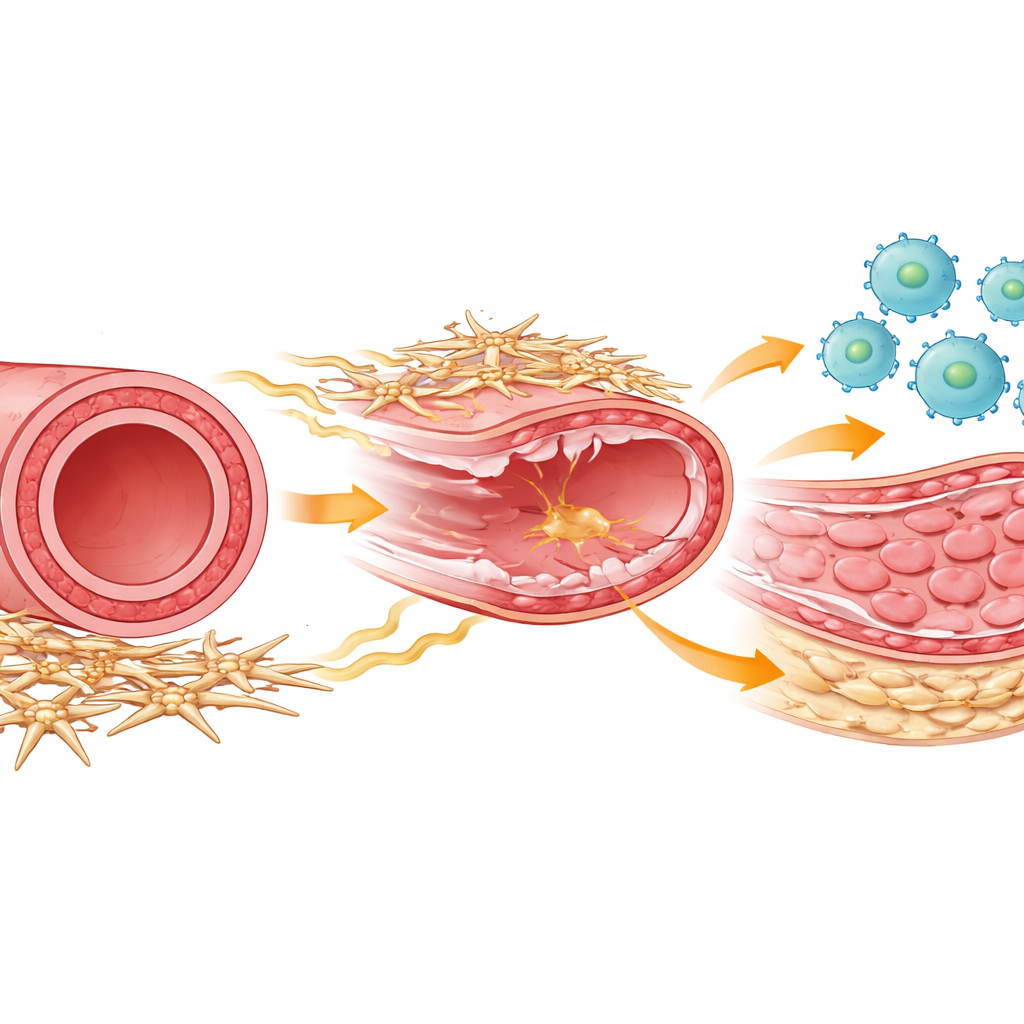
Los actores de la reparación arterial
Dentro de cada arteria, varios tipos celulares colaboran para reparar el daño. Células inmunitarias llamadas macrófagos acuden tras una lesión para limpiar restos y coordinar la reparación. Las células del músculo liso forman la capa media muscular que puede engrosarse y estrechar el vaso si comienzan a multiplicarse en exceso. Alrededor del exterior de la arteria hay un grupo menos conocido de células de soporte, a menudo llamadas células mesenquimales o estromales, que ayudan a mantener la estructura del vaso y se comunican químicamente con las células cercanas. Los autores usaron un modelo de ratón que reproduce la lesión por raspado que causa la colocación de un stent y rastrearon cómo se comportaron estos tipos celulares a lo largo del tiempo mediante potentes métodos de lectura génica unicelular y perfiles celulares detallados.
De los primeros intervinientes al equipo de reparación
Poco después de la lesión arterial, células inmunitarias invadieron la pared vascular, alcanzando un pico en un par de días. En esta etapa temprana, la mayoría de los macrófagos mostraron un perfil clásico «inflamatorio» adecuado para combatir señales de peligro. Pero alrededor de la primera semana predominó otra personalidad macrófaga: un tipo reparador orientado a reconstruir tejido y promover el crecimiento del músculo liso. Los investigadores pudieron separar estos grupos usando marcadores de superficie y el momento temporal, y demostraron que tanto los macrófagos inflamatorios como los reparadores procedían en gran medida de monocitos circulantes reclutados desde la sangre. Cuando eliminaron experimentalmente los macrófagos durante la fase tardía reparadora, la división de las células del músculo liso disminuyó drásticamente y la capa interna anómala, o neointima, no se formó, lo que prueba que estos macrófagos orientados a la reparación son necesarios para el engrosamiento que puede volver a obstruir las arterias.
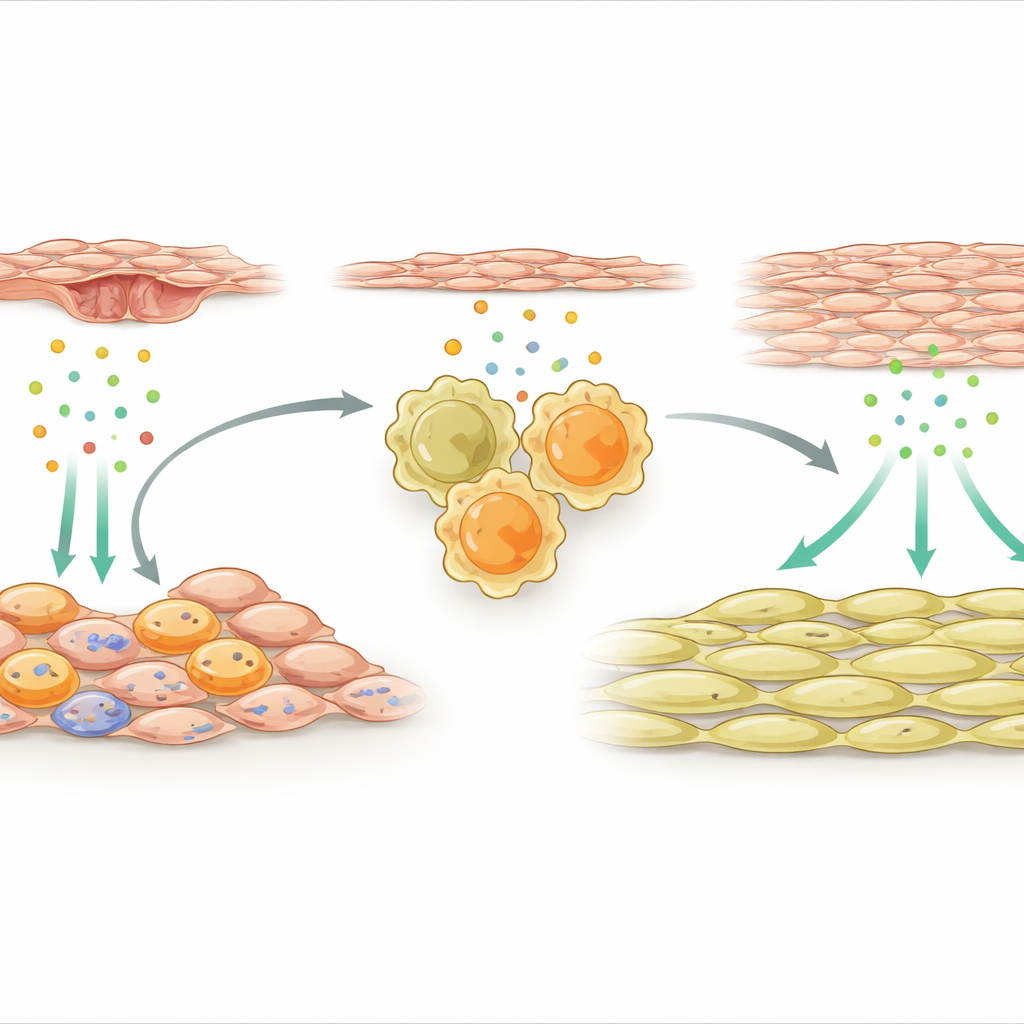
Células de soporte que activan a los macrófagos reparadores
El equipo se centró entonces en las células de soporte externas que envuelven la arteria. Tras la lesión, un subconjunto especializado de estas células mesenquimales se activó intensamente y comenzó a expresar numerosos genes relacionados con la inmunidad. Una señal destacó: IL-33, una molécula de alarma liberada por tejidos dañados o estresados. Estas células de soporte productoras de IL-33 se agruparon cerca de macrófagos en la pared vascular. Los investigadores demostraron que factores liberados por las células endoteliales lesionadas, el revestimiento interior de la arteria, activaron un interruptor molecular llamado NFκB en las células mesenquimales, lo que a su vez aumentó la producción de IL-33. Tanto en ratones como en pacientes humanos con reestrechamiento relacionado con stents, los niveles de IL-33 eran elevados, lo que sugiere que esta vía tiene relevancia clínica.
Una reacción en cadena química hacia el engrosamiento vascular
IL-33 actúa uniéndose a un receptor conocido como ST2 en las células inmunitarias. El estudio encontró que tras la lesión arterial, muchos de los macrófagos reparadores en la pared expresaban este receptor. Cuando el IL-33 procedente de las células de soporte externas estimuló a los macrófagos ST2 positivos, los empujó hacia un modo fuertemente pro-reparador y los indujo a liberar otra proteína, la osteopontina. La osteopontina actuó luego directamente sobre las células del músculo liso, impulsando su proliferación y acumulación en la cara interna de la arteria, creando una capa engrosada que estrecha el canal de flujo sanguíneo. Si los investigadores eliminaron IL-33 específicamente de las células mesenquimales, o eliminaron ST2 en los macrófagos, o bloquearon la osteopontina con moléculas de silenciamiento génico incorporadas en un hidrogel local, el crecimiento del músculo liso se redujo y la arteria permaneció más abierta.
Nuevas ideas para mantener los stents permeables
Para quienes no son especialistas, el mensaje central es que el reestrechamiento perjudicial de las arterias tras la colocación de un stent no es solo un problema de las células del músculo liso portándose mal por sí solas. Más bien, está orquestado por una conversación entre las células de soporte externas del vaso y un subconjunto particular de macrófagos «reparadores». La lesión induce a las células de soporte a liberar IL-33, que activa a los macrófagos ST2 positivos, que a su vez secretan osteopontina para sobreestimular el crecimiento del músculo liso. Interrumpir localmente esta cadena IL-33–ST2–osteopontina en el lugar de la lesión previno el engrosamiento excesivo en ratones. Eso sugiere un futuro en el que los stents podrían combinarse con geles o recubrimientos inteligentes que afinen la reparación en lugar de suprimirla de forma brusca, ayudando a que las arterias se reparen sin volverse a cerrar.
Cita: Ping, Y., Qin, Z., Huang, X. et al. Perivascular mesenchymal cells instruct ST2+ reparative macrophages to promote endovascular injury-induced neointimal hyperplasia in mice. Nat Commun 17, 3635 (2026). https://doi.org/10.1038/s41467-026-68587-x
Palabras clave: rehabilitación vascular, macrófagos, señalización IL-33, reestenosis, células del músculo liso