Clear Sky Science · pl
Komórki mezenchymalne okołonaczyniowe instruują naprawcze makrofagi ST2+ do promowania neointimalnej hiperplazji indukowanej uszkodzeniem endowaskularnym u myszy
Dlaczego naprawa uszkodzonych tętnic może się zemścić
Kiedy lekarze udrażniają zatkane naczynia wieńcowe za pomocą małych metalowych stentów, ratują życie przywracając przepływ krwi. Jednak u wielu pacjentów leczone naczynie stopniowo ulega ponownemu zwężeniu, gdy komórki w ścianie naczynia nadmiernie się odnawiają. Badanie na myszach stawia kluczowe pytanie stojące za tym problemem: które komórki wewnątrz tętnicy decydują, czy gojenie przebiega gładko, czy przechyla się w szkodliwy przerost, który ponownie może zatkać naczynie?
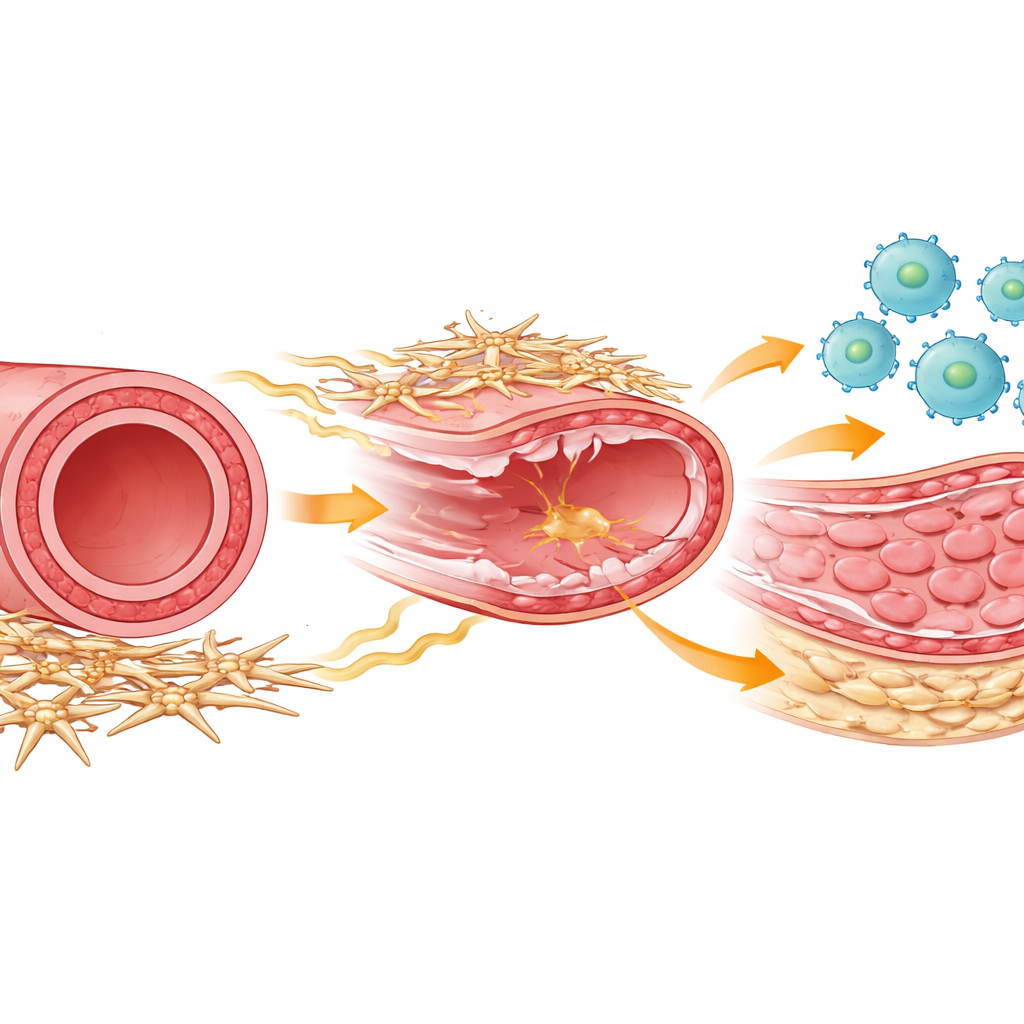
Gracze w procesie gojenia tętnicy
W każdej tętnicy kilka typów komórek współpracuje przy naprawie uszkodzeń. Komórki odpornościowe zwane makrofagami napływają po urazie, aby usuwać szczątki i koordynować gojenie. Komórki mięśni gładkich tworzą warstwę środkową naczynia, która może się pogrubiać i zwężać światło naczynia, jeśli zacznie nadmiernie się dzielić. Otaczająca zewnętrzną stronę tętnicy grupa komórek pomocniczych, często określanych jako komórki mezenchymalne lub stromalne, utrzymuje strukturę naczynia i prowadzi chemiczną komunikację z pobliskimi komórkami. Autorzy użyli modelu mysiego odzwierciedlającego zadrapanie powodowane przez umieszczenie stentu, a następnie śledzili zachowanie tych typów komórek w czasie, wykorzystując zaawansowane metody jednocelowego odczytu genów i szczegółowe profilowanie komórkowe.
Od pierwszych ratowników do załogi naprawczej
Bezpośrednio po uszkodzeniu tętnicy komórki odpornościowe zalewały ścianę naczynia, osiągając szczyt w ciągu kilku dni. Na tym wczesnym etapie większość makrofagów wykazywała klasyczny „zapalny” profil odpowiedni do zwalczania sygnałów zagrożenia. Jednak po około tygodniu dominował inny typ makrofagów: naprawczy, nastawiony na odbudowę tkanek i pobudzanie wzrostu komórek mięśni gładkich. Badacze rozdzielili te grupy na podstawie markerów powierzchniowych i czasu, wykazując, że zarówno zapalne, jak i naprawcze makrofagi w dużej mierze pochodziły z krążących monocytów rekrutowanych z krwi. Gdy eksperymentalnie usunięto makrofagi w późniejszej, naprawczej fazie, podziały komórek mięśni gładkich gwałtownie spadły, a nieprawidłowa wewnętrzna warstwa, czyli neointima, nie utworzyła się, dowodząc, że te późno napływające makrofagi ukierunkowane na naprawę są niezbędne do pogrubienia, które może ponownie zablokować tętnice.
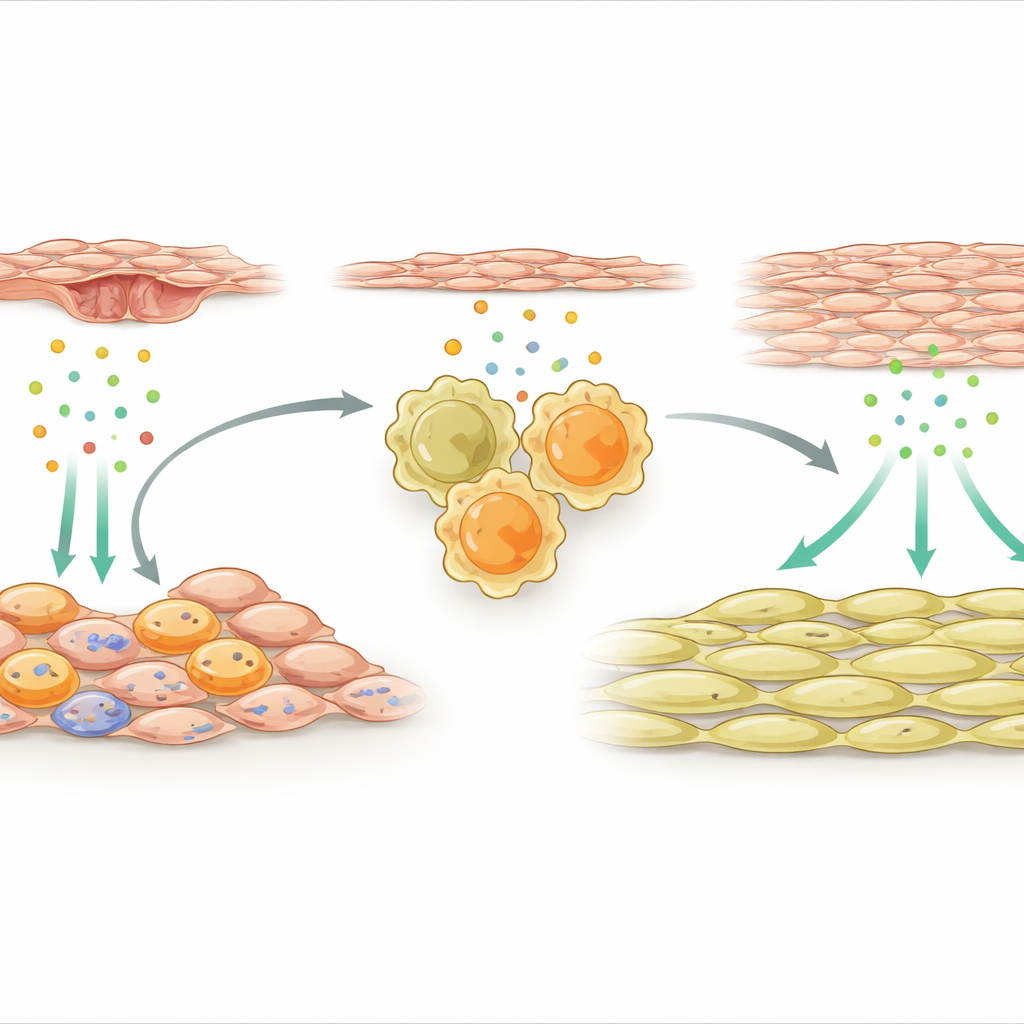
Komórki podporowe, które włączają makrofagi naprawcze
Zespół zwrócił następnie uwagę na zewnętrzne komórki podporowe otaczające tętnicę. Po urazie wyspecjalizowana podgrupa tych komórek mezenchymalnych stała się wysoce aktywna i zaczęła włączać wiele genów związanych z układem odpornościowym. Jeden sygnał wyróżniał się szczególnie: IL-33, cząsteczka alarmowa uwalniana przez uszkodzone lub zestresowane tkanki. Komórki podporowe produkujące IL-33 skupiały się w pobliżu makrofagów w ścianie naczynia. Badacze pokazali, że czynniki uwalniane z uszkodzonych komórek śródbłonka, wewnętrznej wyściółki tętnicy, aktywują w komórkach mezenchymalnych przełącznik molekularny zwany NFκB, co z kolei zwiększa produkcję IL-33. Zarówno u myszy, jak i u pacjentów z ponownym zwężeniem po stencie, poziomy IL-33 były podwyższone, co sugeruje, że ta ścieżka ma znaczenie kliniczne.
Chemiczny łańcuch reakcji prowadzący do pogrubienia naczynia
IL-33 działa poprzez wiązanie z receptorem znanym jako ST2 na komórkach odpornościowych. Badanie wykazało, że po uszkodzeniu tętnicy wiele naprawczych makrofagów w ścianie wyrażało ten receptor. Kiedy IL-33 pochodzący z zewnętrznych komórek podporowych stymulował makrofagi ST2-dodatnie, popychał je w silnie pro-naprawczy tryb i powodował uwalnianie kolejnego białka, osteopontyny. Osteopontyna następnie działała bezpośrednio na komórki mięśni gładkich, pobudzając je do proliferacji i nakładania się po wewnętrznej stronie tętnicy, tworząc pogrubioną warstwę, która zwęża światło naczynia. Gdy badacze usunęli IL-33 specyficznie z komórek mezenchymalnych, albo usunęli ST2 z makrofagów, albo zablokowali osteopontynę za pomocą cząsteczek wyciszających geny umieszczonych w lokalnym hydrożelu, wzrost komórek mięśni gładkich został ograniczony, a tętnica pozostała bardziej przepustowa.
Nowe pomysły na utrzymanie stentów drożnych
Dla osób niebędących specjalistami kluczowy przekaz jest taki, że szkodliwe ponowne zwężenie tętnic po stentowaniu nie jest tylko problemem wynikającym z samodzielnego niewłaściwego zachowania komórek mięśni gładkich. Zamiast tego jest to wynik rozmowy między zewnętrznymi komórkami podporowymi naczynia a szczególną podgrupą „naprawczych” makrofagów. Uszkodzenie powoduje, że komórki podporowe uwalniają IL-33, która aktywuje makrofagi ST2-dodatnie, a te następnie wydzielają osteopontynę, nadmiernie pobudzając wzrost komórek mięśni gładkich. Przerwanie tego łańcucha IL-33–ST2–osteopontyna lokalnie w miejscu urazu zapobiegało nadmiernemu pogrubieniu u myszy. To sugeruje przyszłość, w której stenty mogą być połączone z inteligentnymi żelami lub powłokami, które precyzyjnie modulują gojenie zamiast je brutalnie tłumić, pomagając tętnicom naprawiać się bez ponownego zatykania.
Cytowanie: Ping, Y., Qin, Z., Huang, X. et al. Perivascular mesenchymal cells instruct ST2+ reparative macrophages to promote endovascular injury-induced neointimal hyperplasia in mice. Nat Commun 17, 3635 (2026). https://doi.org/10.1038/s41467-026-68587-x
Słowa kluczowe: naprawa naczyń, makrofagi, sygnalizacja IL-33, restenoza, komórki mięśni gładkich