Clear Sky Science · he
תאי מזנכימה פרי-ווסקולריים מכוונים מקרופגים ST2+ תיקוניים לקידום היפרפלזיה ניו-אינטימלית מוּנעת-פציעה באנדו-וסקולה בעכברים
מדוע תיקון של עורקים פגועים עלול לחזור ולפגוע
כאשר רופאים פותחים עורקי לב סתומים באמצעות תומכנים (סטנטים) מתכתיים זעירים, הם מצילים חיים על ידי שיקום זרימת הדם. עם זאת, אצל מטופלים רבים, כלי הדם המטופל מתעקל בהדרגה שוב כשהתאים בדפנות כלי הדם צומחים בחזרה ביתר שאת. מחקר זה בעכברים שואל שאלה מרכזית מאחורי הבעיה: אילו תאים בתוך העורק מחליטים האם ההחלמה תישאר חלקה או תסטה לצמיחה מזיקה שעלולה לחסום את כלי הדם שנית?
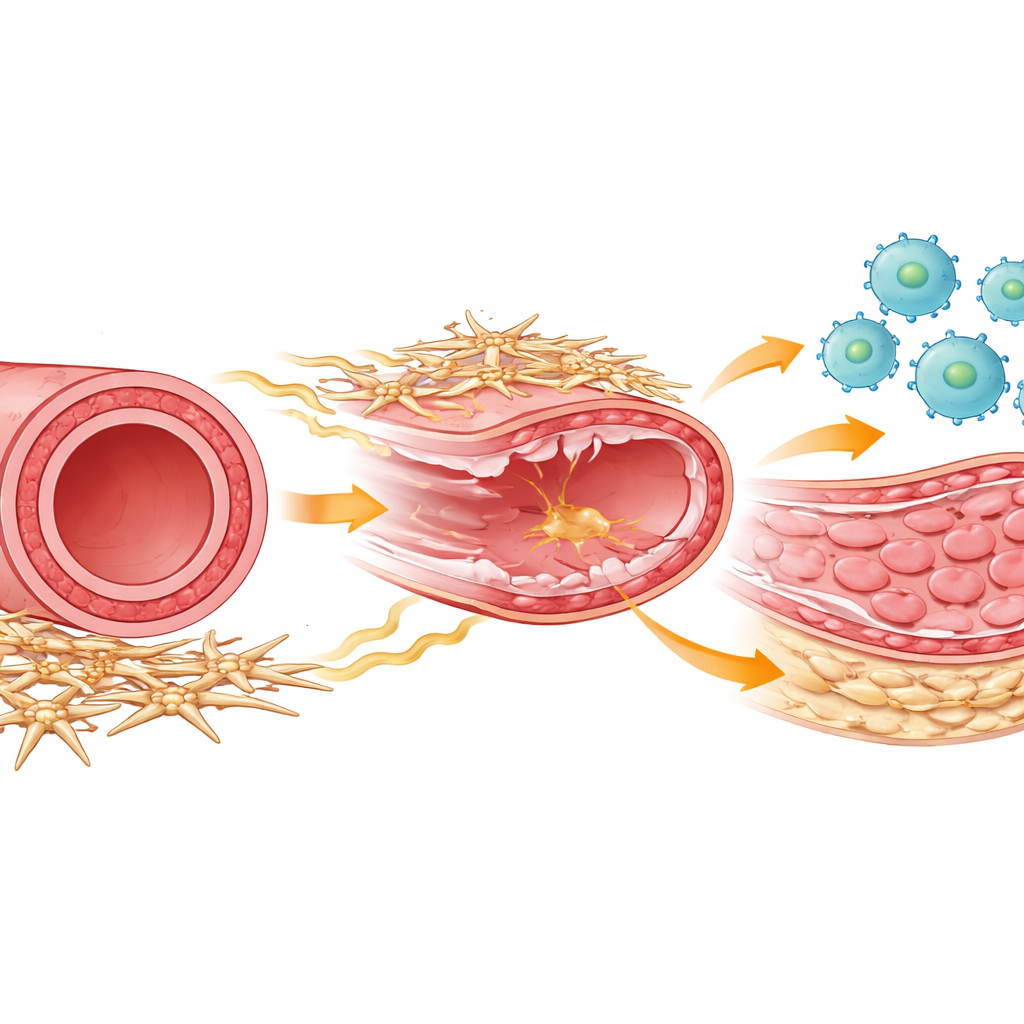
שחקני התיקון בעורק
בתוך כל עורק פועלים יחד מספר סוגי תאים לתיקון נזק. תאי מערכת החיסון הנקראים מקרופגים מגיעים במהרה אחרי הפציעה לנקות שברי תאים ולתאם את ההחלמה. תאי השריר החלק יוצרים את השכבה השרירית האמצעית שיכולה לעבות ולצר את הכלי אם הם מתחילים להתחלק ביתר. עטופים סביב החלק החיצוני של העורק נמצא קבוצה פחות מוכרת של תאי תמיכה, שבדרך כלל מכונים תאי מזנכימה או תאי סטרומה, המסייעים לשמור על מבנה הכלי ומתקשרים כימית עם תאים סמוכים. החוקרים השתמשו במודל עכבר החוקה פציעה בגירוד המדמה את הפציעה הנגרמת בעת הצבת סטנט, ומעקב אחר התנהגות כל סוגי התאים הללו לאורך זמן באמצעות שיטות קריאה של גנים ברמת התא הבודד ותיאורי פרופילינג תאיים מפורטים.
מהמגיבים הראשונים לצוותי התיקון
מיד לאחר הפציעה בעורק, תאי חיסון זלגו לקיר כלי הדם, ושיאם הגיע בתוך יום-יומיים. בשלב המוקדם הזה, מרבית המקרופגים הראו פרופיל קלאסי "דלקתי" המתאים למאבק באיתותי סכנה. אך כעבור כשבוע, דמות אחרת של מקרופגים הפכה לדומיננטית: סוג תיקוני המכוון לבנייה מחדש של רקמה ולעידוד צמיחת תאי שריר חלק. החוקרים הצליחו להבדיל בין הקבוצות הללו באמצעות סימני פני שטח ותזמון, והראו ששני סוגי המקרופגים — גם הדלקתיים וגם התיקוניים — נגזרו ברובם ממונוציטים ממחזור הדם המגוייסים מהדם. כאשר הם הסירו באופן ניסויי מקרופגים בשלב המאוחר של התיקון, חל ירידה חדה בחלוקת תאי השריר החלק והשכבה הפנימית החורגת, הנאו-אינטימה, לא נוצרה כרגיל, מה שמוכיח שמקרופגים אלו שמגיעים בשלב המאוחר נחוצים לעיבוי שעלול לחסום את העורקים מחדש.
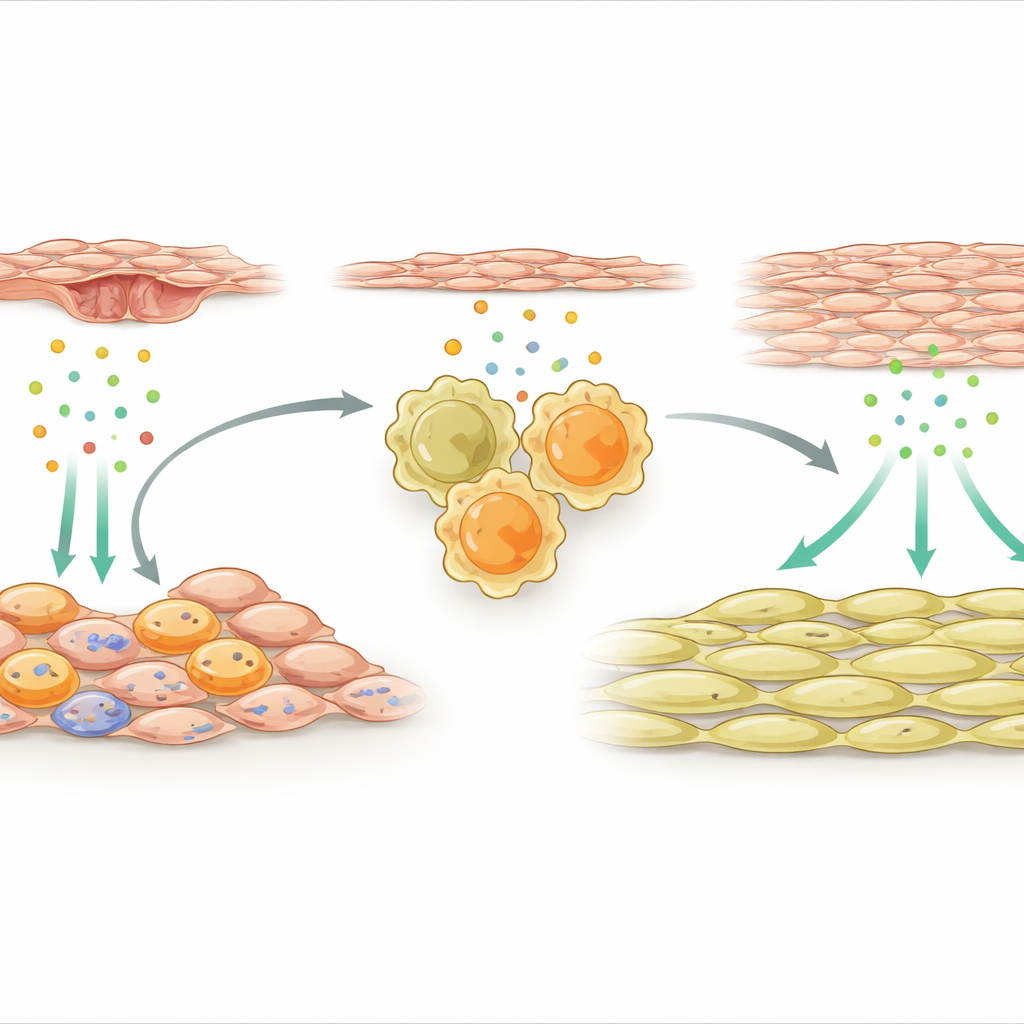
תאי תמיכה שמדליקים מקרופגים תיקוניים
הקבוצה הפנתה אז את תשומת הלב לתאי התמיכה החיצוניים העוטפים את העורק. אחרי הפציעה, תת-אוכלוסייה מיוחדת של תאי מזנכימה אלה הפכה לפעילה מאוד והחלה לבטא גנים רבים הקשורים למערכת החיסון. אות אחד בלט במיוחד: IL-33, מולקולת מצוקה המשוחררת על ידי רקמות פגועות או מנוצלות בלחץ. תאי התמיכה המייצרים IL-33 צברו עצמם קרוב למקרופגים בדפנות כלי הדם. החוקרים הראו כי גורמים שמשתחררים מתאים אנדותל פגועים, השכבה הפנימית של העורק, מפעילים מתג מולקולרי בשם NFκB בתאי מזנכימה, וזה בתורו מגביר את ייצור ה-IL-33. גם בעכברים וגם בחולים אנושיים שסבלו מהיצרות חוזרת בעקבות סטנט, רמות ה-IL-33 נמצאו מוגברות, מה שמרמז כי הנתיב הזה רלוונטי קלינית.
שרשרת כימית שמובילה לעיבוי הכלי
IL-33 פועלת על ידי קשירה לקולטן הידוע בשם ST2 על תאי חיסון. המחקר מצא כי לאחר פציעת העורק, רבים מהמקרופגים התיקוניים בדופן נשאו את הקולטן הזה. כאשר IL-33 מתאי התמיכה החיצוניים עורר מקרופגים הנושאים ST2, הדבר דחף אותם למצב חזק של קידום תיקון וגרם להם לשחרר חלבון נוסף, אוסטאופונטין. אוסטאופונטין פעל אז ישירות על תאי השריר החלק, דוחף אותם להתחלק ולהצטבר בחלק הפנימי של העורק, ויוצר שכבה מעובה שמצמצמת את מעבר הדם. אם החוקרים הסירו ספציפית IL-33 מתאי מזנכימה, או הסירו את ST2 מהמקרופגים, או חסמו את אוסטאופונטין בעזרת מולקולות השתקת גנים ארוזות בהידרוג’ל מקומי, צמיחת תאי השריר החלק הועכבה והעורק נשמר פתוח יותר.
רעיונות חדשים לשמירה על פתיחות הסטנטים
ללא מומחיות מעמיקה, המסר המרכזי הוא שההיצרות המזיקה של העורקים אחרי הצבת סטנט איננה רק בעיה של תאי שריר חלק שמתנהגים לא כשורה לבדם. במקום זאת, היא מאורגנת על ידי שיחה בין תאי התמיכה החיצוניים של הכלי ותת-קבוצה מסוימת של מקרופגים "תיקוניים". הפציעה גוררת תאי תמיכה לשחרר IL-33, שמפעיל מקרופגים בעלי ST2, ואז אלה מופרשים אוסטאופונטין שמעודד באופן מוגזם את צמיחת תאי השריר החלק. הפרעה מקומית בשרשרת IL-33–ST2–אוסטאופונטין באתר הפציעה מנעה עיבוי מופרז בעכברים. זה מציע עתיד שבו סטנטים עשויים להיות משולבים עם ג׳לים חכמים או ציפויים שמדייקים את ההחלמה במקום לדכא אותה בצורה גורפת, ועוזרים לעורקים לתקן את עצמם מבלי להיסתם שוב.
ציטוט: Ping, Y., Qin, Z., Huang, X. et al. Perivascular mesenchymal cells instruct ST2+ reparative macrophages to promote endovascular injury-induced neointimal hyperplasia in mice. Nat Commun 17, 3635 (2026). https://doi.org/10.1038/s41467-026-68587-x
מילות מפתח: תיקון כלי דם, מקרופגים, אותות IL-33, היצרות חוזרת, תאי שריר חלק