Clear Sky Science · de
Perivaskuläre mesenchymale Zellen instruieren ST2+ reparative Makrophagen, um bei endovaskulären Verletzungen eine neointimale Hyperplasie in Mäusen zu fördern
Warum das Reparieren geschädigter Arterien nach hinten losgehen kann
Wenn Ärzte verstopfte Herzkranzgefäße mit winzigen Metallstents öffnen, retten sie Leben, indem sie den Blutfluss wiederherstellen. Bei vielen Patientinnen und Patienten verengt sich das behandelte Gefäß jedoch mit der Zeit erneut, weil Zellen in der Gefäßwand zu stark nachwachsen. Diese Studie an Mäusen stellt eine zentrale Frage hinter diesem Problem: Welche Zellen innerhalb der Arterie entscheiden, ob die Heilung glatt verläuft oder in ein schädliches Überwachsen umschlägt, das das Gefäß erneut verengen kann?
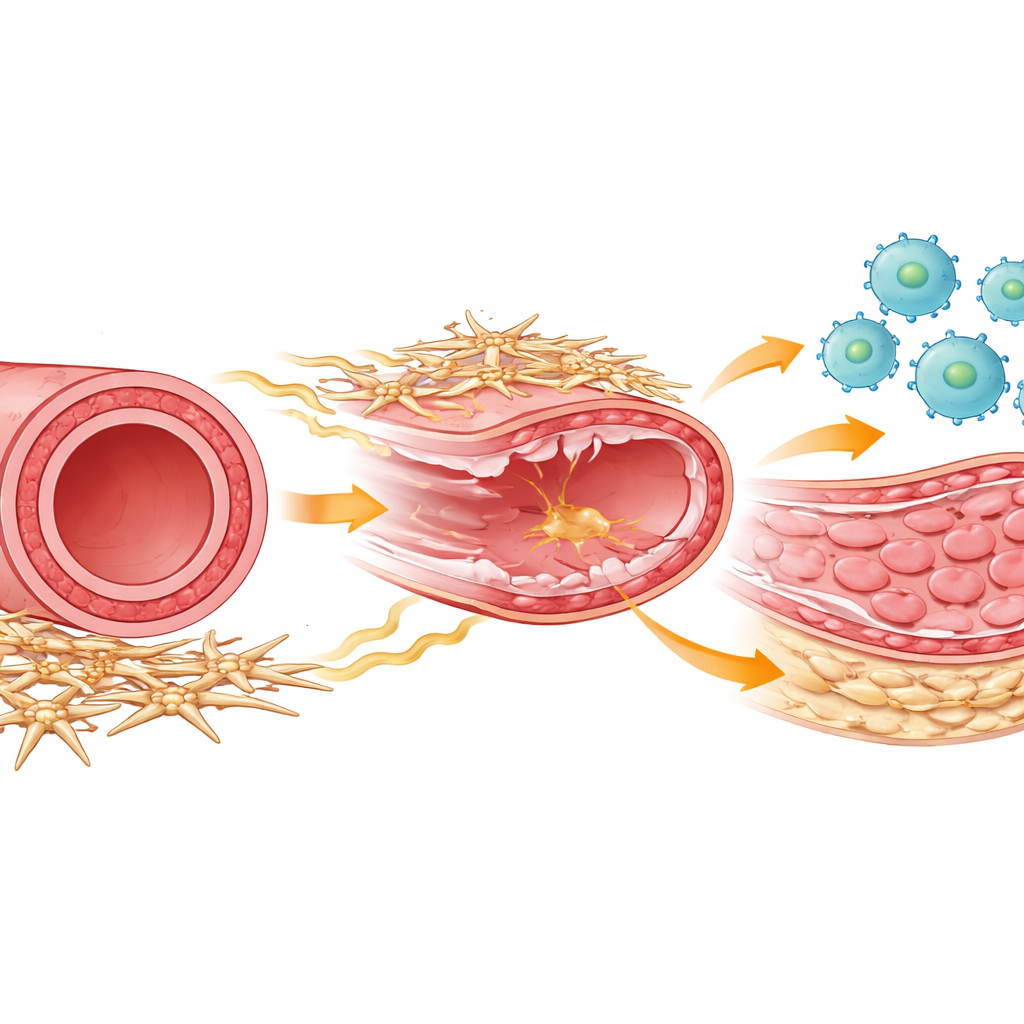
Die Beteiligten der Gefäßheilung
Innerhalb jeder Arterie arbeiten mehrere Zelltypen zusammen, um Schäden zu reparieren. Immunzellen, sogenannte Makrophagen, strömen nach einer Verletzung herbei, um Trümmer zu beseitigen und die Heilung zu koordinieren. Glatte Muskelzellen bilden die muskuläre Mittelschicht, die sich verdicken und das Gefäß verengen kann, wenn sie zu stark proliferiert. Außenseitlich die Arterie umhüllend befindet sich eine weniger bekannte Gruppe von Stütz- oder stromalen Zellen, die die Gefäßstruktur erhalten und chemisch mit benachbarten Zellen kommunizieren. Die Autoren verwendeten ein Mausmodell, das die Abkratzverletzung nach Stenteinlage nachahmt, und verfolgten dann mithilfe leistungsfähiger Einzelzell-Genexpressionsmethoden und detaillierter Zellprofile, wie sich diese Zelltypen über die Zeit verhielten.
Von Ersthelfern zur Reparaturmannschaft
Unmittelbar nach der Arterienverletzung strömten Immunzellen in die Gefäßwand und erreichten innerhalb weniger Tage ihren Höhepunkt. In dieser frühen Phase zeigten die meisten Makrophagen ein klassisches „inflammatorisches“ Profil, geeignet zur Bekämpfung von Gefahrensignalen. Nach etwa einer Woche dominierte jedoch ein anderes Makrophagenprofil: ein reparativer Typ, ausgerichtet auf Gewebewiederaufbau und die Förderung des Wachstums glatter Muskelzellen. Die Forschenden konnten diese Gruppen anhand von Oberflächenmarkern und Zeitverlauf unterscheiden und zeigten, dass sowohl inflammatorische als auch reparative Makrophagen größtenteils aus zirkulierenden Monozyten stammen, die aus dem Blut rekrutiert werden. Entfernten sie experimentell die Makrophagen während der späteren, reparativen Phase, ging die Teilung glatter Muskelzellen stark zurück und die abnorme innere Schicht, die Neointima, bildete sich nicht, was beweist, dass diese spät eintreffenden reparaturorientierten Makrophagen für die Verdickung, die Arterien wieder verengen kann, notwendig sind.
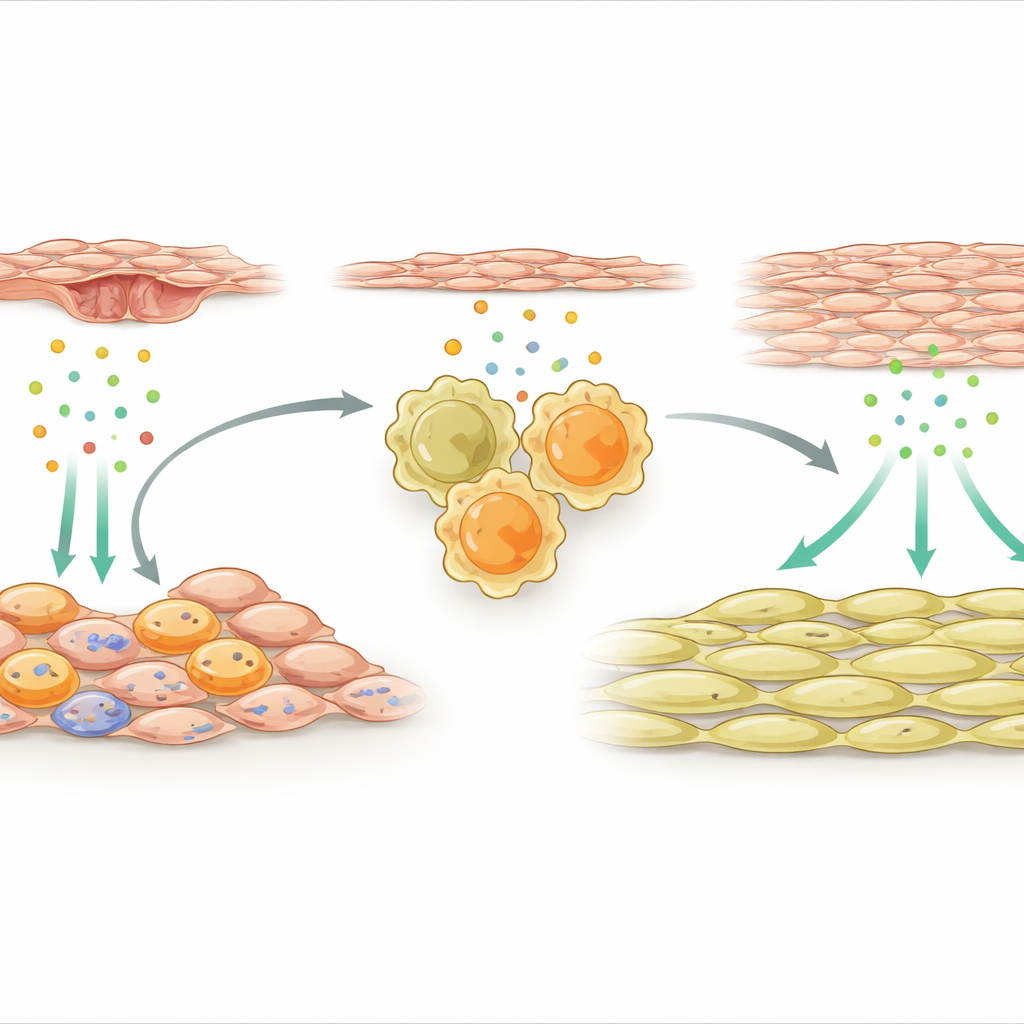
Stütz-Zellen, die Reparaturmakrophagen aktivieren
Das Team wandte sich dann den äußeren Stütz-Zellen zu, die die Arterie umhüllen. Nach der Verletzung wurden eine spezialisierte Untergruppe dieser mesenchymalen Zellen hochaktiv und begann, viele immunbezogene Gene zu exprimieren. Ein Signal stach hervor: IL-33, ein Stress- oder Alarmsignal, das von geschädigten oder belasteten Geweben freigesetzt wird. Diese IL-33-produzierenden Stütz-Zellen gruppierten sich in der Gefäßwand in der Nähe von Makrophagen. Die Forschenden zeigten, dass Faktoren, die von verletzten Endothelzellen — der inneren Auskleidung der Arterie — freigesetzt werden, einen molekularen Schalter namens NFκB in mesenchymalen Zellen aktivieren, was wiederum die IL-33-Produktion steigerte. Sowohl bei Mäusen als auch bei menschlichen Patientinnen und Patienten mit stentbedingter Wiederverengung waren die IL-33-Spiegel erhöht, was darauf hindeutet, dass dieser Weg klinische Relevanz besitzt.
Eine chemische Kettenreaktion zur Gefäßverdickung
IL-33 wirkt, indem es an einen Rezeptor namens ST2 auf Immunzellen bindet. Die Studie fand heraus, dass nach der Arterienverletzung viele der reparativen Makrophagen in der Gefäßwand diesen Rezeptor trugen. Wenn IL-33 aus den äußeren Stützzellen ST2-positive Makrophagen stimulierte, trieben sie diese in einen stark pro-reparativen Zustand und veranlassten sie, ein weiteres Protein freizusetzen: Osteopontin. Osteopontin wirkte dann direkt auf glatte Muskelzellen und trieb deren Proliferation an, sodass sie sich an der Innenseite der Arterie aufschichteten und eine verdickte Schicht bildeten, die den Blutleitkanal verengte. Entfernten die Forschenden IL-33 spezifisch aus mesenchymalen Zellen, oder ST2 aus Makrophagen, beziehungsweise blockierten Osteopontin mit genetisch wirkenden Silencing-Molekülen, die in ein lokales Hydrogel eingebettet wurden, so wurde das Wachstum glatter Muskelzellen gedämpft und das Gefäß blieb weiter offen.
Neue Ansätze, um Stents offen zu halten
Für Nichtfachleute lautet die zentrale Botschaft: Die schädliche Wiederverengung von Arterien nach Stentimplantation ist nicht einfach ein Problem fehlgesteuerter glatter Muskelzellen. Vielmehr wird sie orchestriert durch ein Gespräch zwischen äußeren Gefäßstützzellen und einer bestimmten Untergruppe von „Reparatur“-Makrophagen. Verletzung veranlasst Stützzellen zur Freisetzung von IL-33, das ST2-positive Makrophagen aktiviert, welche dann Osteopontin ausschütten und damit das Wachstum glatter Muskelzellen übermäßig stimulieren. Eine lokale Unterbrechung dieser IL-33–ST2–Osteopontin-Kette an der Verletzungsstelle verhinderte in Mäusen eine übermäßige Verdickung. Das deutet auf eine Zukunft hin, in der Stents mit intelligenten Gelen oder Beschichtungen kombiniert werden könnten, die die Heilung feiner steuern statt sie grob zu unterdrücken, sodass Arterien sich reparieren, ohne sich wieder zu verschließen.
Zitation: Ping, Y., Qin, Z., Huang, X. et al. Perivascular mesenchymal cells instruct ST2+ reparative macrophages to promote endovascular injury-induced neointimal hyperplasia in mice. Nat Commun 17, 3635 (2026). https://doi.org/10.1038/s41467-026-68587-x
Schlüsselwörter: Gefäßreparatur, Makrophagen, IL-33-Signalgebung, Restenose, glatte Muskelzellen