Clear Sky Science · nl
Perivasculaire mesenchymale cellen instrueren ST2+ reparerende macrofagen om endovasculaire letsel-geïnduceerde neointimale hyperplasie bij muizen te bevorderen
Waarom het repareren van beschadigde slagaders averechts kan werken
Wanneer artsen verstopte kransslagaders openen met kleine metalen stents, redden ze levens door de bloedstroom te herstellen. Maar bij veel patiënten vernauwt het behandelde vat na verloop van tijd opnieuw doordat cellen in de vaatwand te enthousiast teruggroeien. Deze muizenstudie onderzoekt een sleutelvraag achter dat probleem: welke cellen binnen de arterie bepalen of genezing soepel verloopt of omslaat in schadelijke overgroei die het vat opnieuw kan verstoppen?
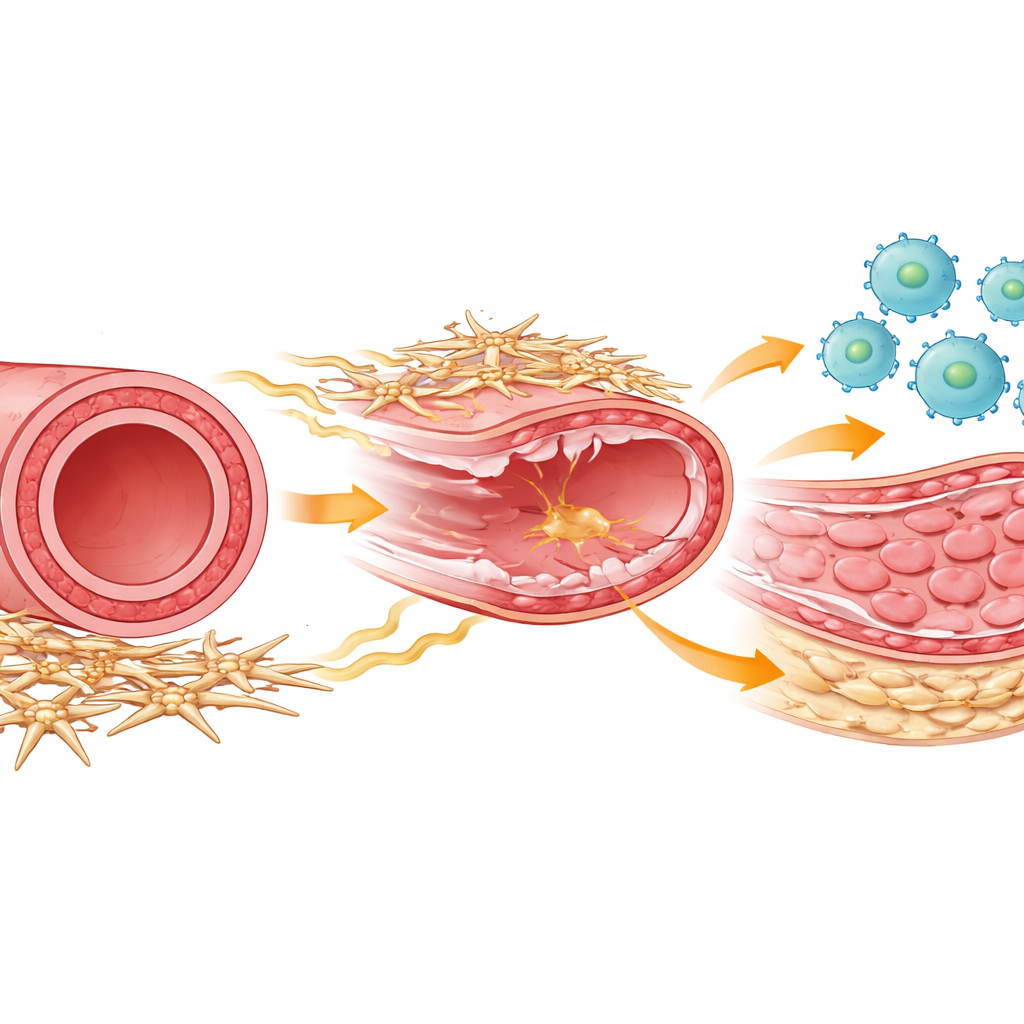
De spelers bij vaatgenezing
In elke arterie werken verschillende celtypen samen om schade te herstellen. Immuuncellen genaamd macrofagen haasten zich na een verwonding naar binnen om puin op te ruimen en genezing te coördineren. Gladde spiercellen vormen de spierlaag in het midden die kan verdikken en het vat vernauwen als ze te veel gaan delen. Rond de buitenkant van de arterie bevindt zich een minder bekend gezelschap ondersteunende cellen, vaak mesenchymale of stromale cellen genoemd, die de structuur van het vat helpen bewaren en chemisch communiceren met naburige cellen. De auteurs gebruikten een muismodel dat het krabben van de vaatwand bij stentplaatsing nabootst en volgden hoe al deze celtypen zich in de tijd gedroegen met krachtige single-cell genleestechnieken en gedetailleerde celprofilering.
Van eerste hulpverleners tot reparatieteam
Direct na het arteriële letsel stroomden immuuncellen de vaatwand binnen en bereikten hun piek binnen een paar dagen. In dit vroege stadium vertoonden de meeste macrofagen een klassiek “inflammatoir” profiel geschikt om gevaarsignalen te bestrijden. Maar na ongeveer een week domineerde een ander macrofaagprofiel: een reparerend type gericht op weefselherstel en het aanmoedigen van gladde spiercelgroei. De onderzoekers konden deze groepen scheiden met oppervlaktemarkers en timing, en toonden aan dat zowel inflammatoire als reparerende macrofagen grotendeels afkomstig waren van circulerende monocyten uit het bloed. Wanneer ze experimenteel macrofagen verwijderden tijdens de latere, reparerende fase, daalde de deling van gladde spiercellen sterk en vormde de abnormale binnenlaag, of neointima, zich niet, wat bewijst dat deze laat binnenkomende, op herstel gerichte macrofagen noodzakelijk zijn voor de verdikking die slagaders opnieuw kan doen dichtslibben.
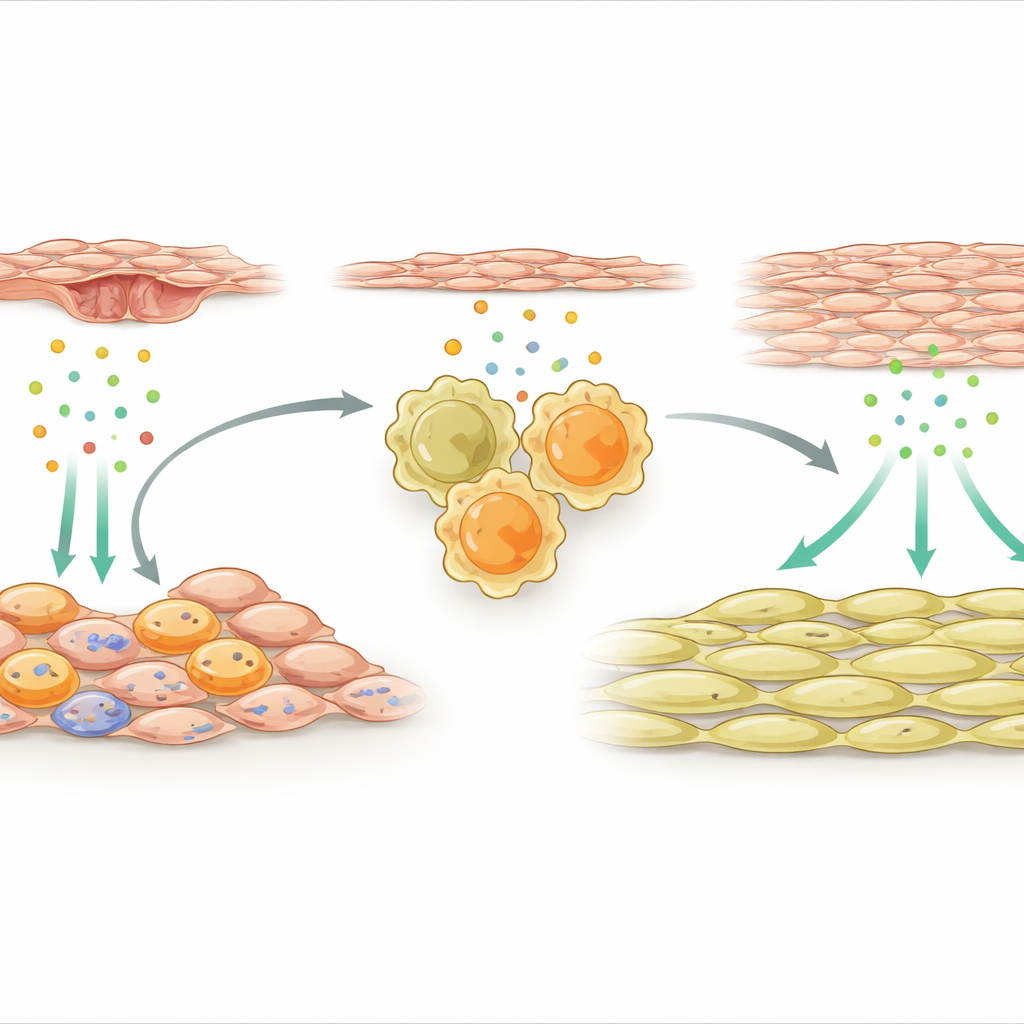
Ondersteunende cellen die reparatiemacrofagen inschakelen
Het team richtte zich vervolgens op de buitenste ondersteunende cellen die de arterie omhullen. Na letsel werd een gespecialiseerde subset van deze mesenchymale cellen zeer actief en begon ze veel immuun-gerelateerde genen tot expressie te brengen. Eén signaal stak er met kop en schouders bovenuit: IL-33, een alarmeringsmolecuul dat wordt vrijgegeven door beschadigd of gestrest weefsel. Deze IL-33–producerende ondersteunende cellen clusteren nabij macrofagen in de vaatwand. De onderzoekers toonden aan dat factoren die vrijkomen uit beschadigde endotheelcellen, de binnenbekleding van de arterie, een moleculaire schakelaar genaamd NFκB in mesenchymale cellen activeerden, wat op zijn beurt de IL-33-productie verhoogde. Zowel bij muizen als bij menselijke patiënten met stent-geassocieerde hervernauwing waren de IL-33-niveaus verhoogd, wat suggereert dat deze route klinisch relevant is.
Een chemische kettingreactie naar vaatverdikking
IL-33 werkt door te binden aan een receptor die bekendstaat als ST2 op immuuncellen. De studie vond dat na arterieel letsel veel van de reparerende macrofagen in de wand deze receptor droegen. Wanneer IL-33 van buitenste ondersteunende cellen ST2-positieve macrofagen stimuleerde, duwde dat hen in een sterk pro-reparatiemode en deed hen een ander eiwit afscheiden, osteopontine. Osteopontine werkte vervolgens direct op gladde spiercellen en dreef deze tot proliferatie en ophoping aan de binnenzijde van de arterie, waardoor een verdikte laag ontstond die het bloedvat vernauwde. Als de onderzoekers IL-33 specifiek uit mesenchymale cellen verwijderden, of ST2 uit macrofagen haalden, of osteopontine blokkeerden met genstilende moleculen verpakt in een lokaal hydrogel, werd de groei van gladde spiercellen afgeremd en bleef de arterie beter open.
Nieuwe ideeën om stents open te houden
Voor niet-specialisten is de kernboodschap dat schadelijke hervernauwing van slagaders na stenting niet alleen een probleem is van slecht functionerende gladde spiercellen op zichzelf. In plaats daarvan wordt het geregisseerd door een gesprek tussen buitenste vaatondersteunende cellen en een specifieke subset van “reparatie” macrofagen. Letsel activeert ondersteunende cellen om IL-33 vrij te geven, dat ST2-positieve macrofagen activeert, die vervolgens osteopontine afscheiden om de groei van gladde spiercellen te overstimuleren. Het onderbreken van deze IL-33–ST2–osteopontine-keten lokaal op de letselplaats voorkwam in muizen overmatige verdikking. Dat suggereert een toekomst waarin stents mogelijk worden gecombineerd met slimme gels of coatings die genezing bijsturen in plaats van deze botweg te onderdrukken, zodat slagaders zichzelf kunnen herstellen zonder opnieuw dicht te lopen.
Bronvermelding: Ping, Y., Qin, Z., Huang, X. et al. Perivascular mesenchymal cells instruct ST2+ reparative macrophages to promote endovascular injury-induced neointimal hyperplasia in mice. Nat Commun 17, 3635 (2026). https://doi.org/10.1038/s41467-026-68587-x
Trefwoorden: vasculair herstel, macrofagen, IL-33 signalering, restenose, gladde spiercellen