Clear Sky Science · sv
Perivaskulära mesenkymala celler instruerar ST2+ reparativa makrofager att främja endovaskulär skada‑inducerad neointimal hyperplasi hos möss
Varför lagning av skadade artärer kan slå tillbaka
När läkare öppnar igentäppta kranskärl med små metallstentar räddar de liv genom att återställa blodflödet. Men hos många patienter smalnar det behandlade kärlet långsamt igen när celler i kärlväggen återväxer för kraftigt. Denna studie i möss ställer en central fråga bakom det problemet: vilka celler inne i artären avgör om läkningsprocessen förblir ordnad eller tippar över i skadlig överväxt som kan täppa till kärlet igen?
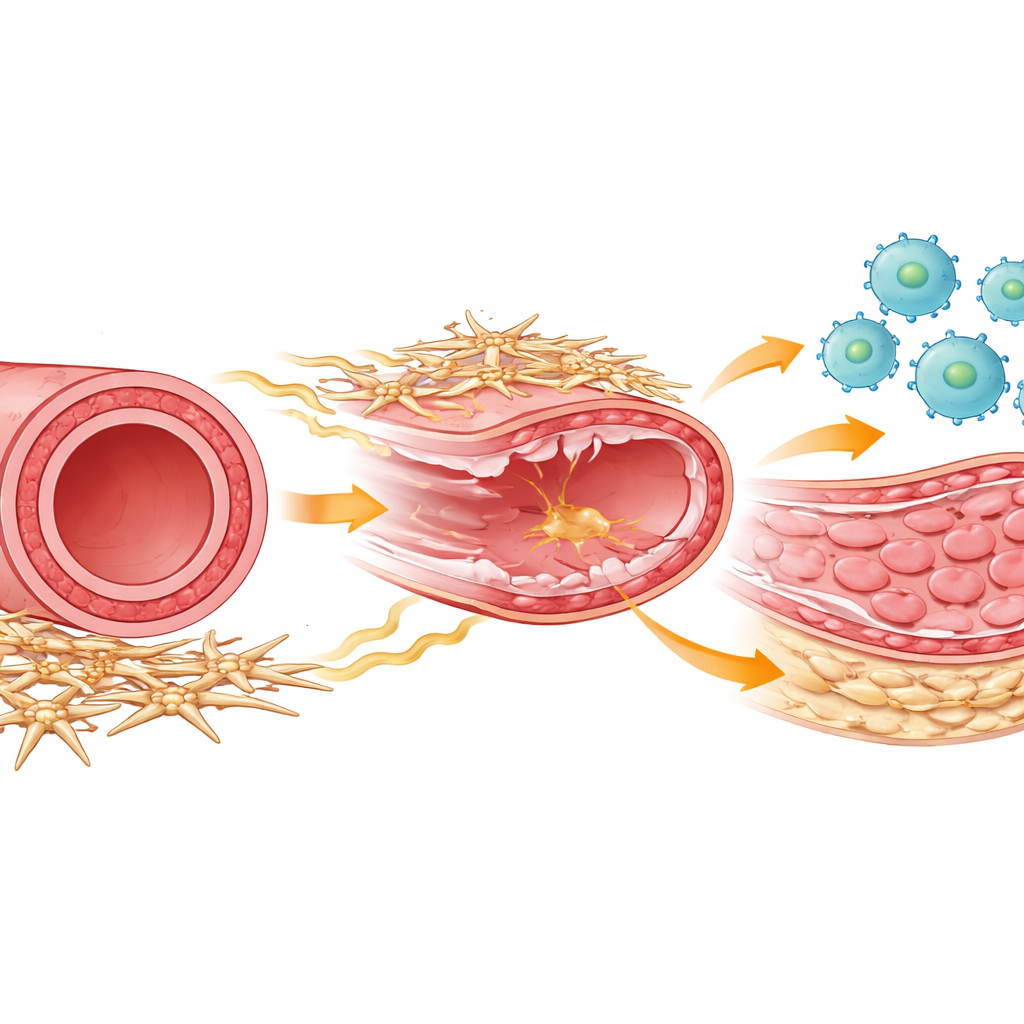
Aktörerna i artärens läkning
Inne i varje artär samarbetar flera celltyper för att reparera skador. Immunceller kallade makrofager strömmar till efter en skada för att rensa upp skräp och samordna läkning. Glatta muskelceller bildar det muskulära mittenlagret som kan förtjockas och förtränga kärlet om de börjar dela sig för mycket. Runt utsidan av artären finns en mindre känd grupp stödjeceller, ofta kallade mesenkymala eller stromaceller, som hjälper till att upprätthålla kärlets struktur och kommunicerar kemiskt med närliggande celler. Författarna använde en musemodell som efterliknar det skrapsår som uppstår när en stent placeras, och följde hur alla dessa celltyper uppträdde över tid med kraftfulla single‑cell‑genläsningsmetoder och detaljerad cellprofilering.
Från förstärkare till reparationsbesättning
Omedelbart efter artärskadan strömmade immunceller in i kärlväggen och nådde sin topp inom ett par dagar. I detta tidiga skede visade de flesta makrofager en klassisk ”inflammatorisk” profil lämpad för att bekämpa farosignaler. Men efter ungefär en vecka dominerade en annan makrofag‑personlighet: en reparativ typ inriktad på vävnadsåteruppbyggnad och som uppmuntrar glatt muskelväxt. Forskarna kunde separera dessa grupper med hjälp av ytmärken och tidpunkt, och visade att både inflammatoriska och reparativa makrofager till stor del härstammade från cirkulerande monocyter rekryterade från blodet. När de experimentellt avlägsnade makrofager under det senare, reparativa stadiet, föll glattmuskelcellernas delning kraftigt och det onormala innerlagret, neointiman, bildades inte — vilket bevisar att dessa sent ankommande, reparationsinriktade makrofager är nödvändiga för den förtjockning som kan täppa till artärer.
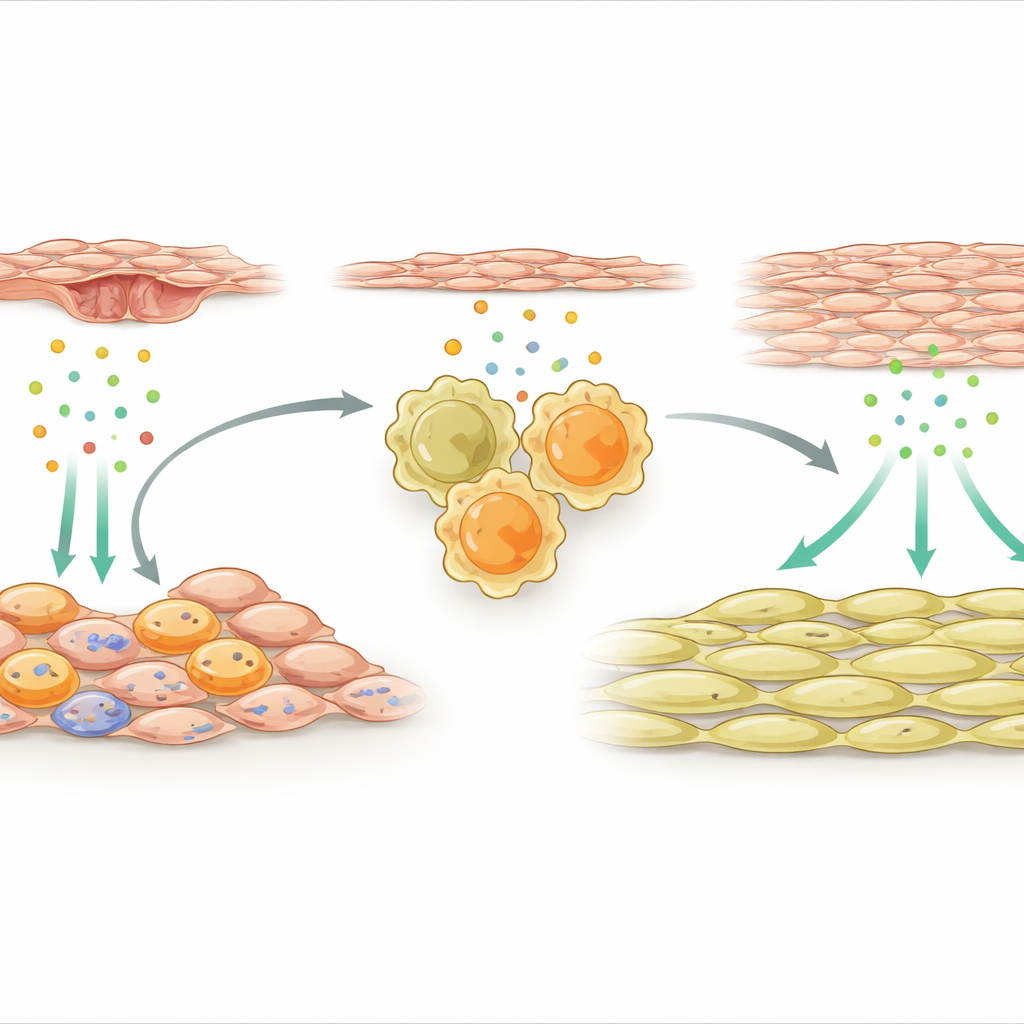
Stödceller som aktiverar reparationsmakrofager
Teamet vände sig sedan till de yttre stödcellerna som omsluter artären. Efter skada blev en specialiserad undergrupp av dessa mesenkymala celler mycket aktiva och började uttrycka många immunkopplade gener. En signal stack ut: IL‑33, ett nödsignalsmolekyl som frisätts av skadad eller stressad vävnad. Dessa IL‑33–producerande stödceller klustrade sig nära makrofager i kärlväggen. Forskarna visade att faktorer som frisätts från skadade endotelceller, artärens inre beklädnad, aktiverade en molekylär strömbrytare kallad NFκB i mesenkymala celler, vilket i sin tur ökade IL‑33‑produktionen. I både möss och mänskliga patienter med stentrelaterad återförträngning var nivåerna av IL‑33 förhöjda, vilket tyder på att denna väg är kliniskt relevant.
En kemisk kedjereaktion till kärlförtjockning
IL‑33 verkar genom att binda till en receptor känd som ST2 på immunceller. Studien fann att efter artärskada bar många av de reparativa makrofagerna i väggen denna receptor. När IL‑33 från yttre stödceller stimulerade ST2‑positiva makrofager drev det dem in i ett starkt pro‑reparativt läge och fick dem att frisätta ett annat protein, osteopontin. Osteopontin verkade sedan direkt på glatta muskelceller och drev dem att proliferera och staplas upp på insidan av artären, vilket skapade ett förtjockat lager som förtränger blodflödeskanalen. Om forskarna tog bort IL‑33 specifikt från mesenkymala celler, eller avlägsnade ST2 från makrofager, eller blockerade osteopontin med gen‑tystande molekyler inpackade i en lokal hydrogel, begränsades glattmuskelväxten och artären förblev mer öppen.
Nya idéer för att hålla stentar öppna
För icke‑specialister är huvudbudskapet att skadlig återförträngning av artärer efter stentning inte bara är ett problem med glatta muskelceller som beter sig fel på egen hand. Istället orkestreras den av en konversation mellan yttre kärlstödjeceller och en särskild undergrupp av ”reparations”‑makrofager. Skada utlöser att stödceller släpper ut IL‑33, vilket aktiverar ST2‑positiva makrofager, som sedan utsöndrar osteopontin för att överstimulera glatt muskelväxt. Att avbryta denna IL‑33–ST2–osteopontin‑kedja lokalt vid skadestället förhindrade överdriven förtjockning hos möss. Det antyder en framtid där stentar kan kombineras med smarta geler eller beläggningar som finjusterar läkning snarare än att trubbigt undertrycka den, så att artärerna kan reparera sig utan att stängas igen.
Citering: Ping, Y., Qin, Z., Huang, X. et al. Perivascular mesenchymal cells instruct ST2+ reparative macrophages to promote endovascular injury-induced neointimal hyperplasia in mice. Nat Commun 17, 3635 (2026). https://doi.org/10.1038/s41467-026-68587-x
Nyckelord: kärlreparation, makrofager, IL-33‑signalering, restenos, glatta muskelceller