Clear Sky Science · ar
الخلايا المتوسطية المحيطة بالأوعية توجهالبالماكروفاجات الإصلاحية الحاملة ST2 لتعزيز فرط النسيج الداخلي الناجم عن إصابة بطانة الأوعية في الفئران
لماذا قد يعود إصلاح الشرايين التالف إلى الإضرار
عندما يفتح الأطباء شرايين القلب المسدودة بواسطة دعامات معدنية صغيرة، فإنهم ينقذون الأرواح باستعادة تدفق الدم. لكن في العديد من المرضى، يتضيّق الوعاء المعالج تدريجيًا مرة أخرى مع نمو الخلايا في جدار الوعاء بشكل مفرط. تطرح هذه الدراسة على الفئران سؤالًا رئيسيًا خلف هذه المشكلة: أي الخلايا داخل الشريان تقرر ما إذا كان الشفاء سيبقى سلسًا أم سيلتهي بنمو ضار يمكن أن يسد الوعاء من جديد؟
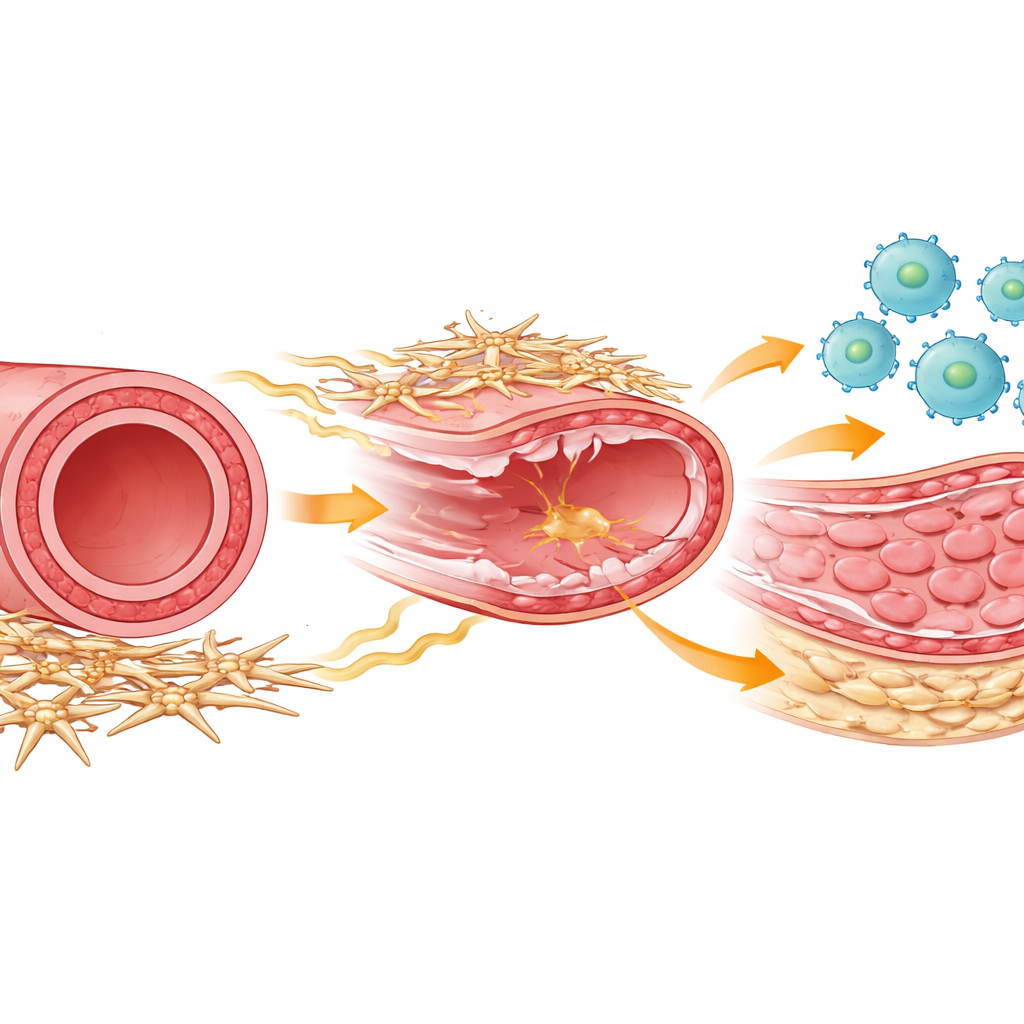
الأطراف الفاعلة في شفاء الشرايين
داخل كل شريان تعمل عدة أنواع من الخلايا معًا لإصلاح الضرر. تتدفق خلايا مناعية تسمى البالماكروفاجات بعد الإصابة لإزالة الحطام وتنسيق الشفاء. تشكل خلايا العضلات الملساء الطبقة العضلية الوسطى التي قد تزداد سماكتها وتضيّق الوعاء إذا بدأت بالتكاثر المفرط. تحيط بالجزء الخارجي من الشريان مجموعة أقل شهرة من خلايا الدعم، غالبيتها خلايا متوسطة أو نسيجية، تساعد على الحفاظ على بنية الوعاء وتتواصل كيميائيًا مع الخلايا المجاورة. استخدم الباحثون نموذج فئران يحاكي إصابة الخدش التي تحدث عند وضع الدعامة، ثم تتبعوا سلوك هذه الأنواع الخلوية على مر الزمن باستخدام طرق قراءة الجينات خلوية واحدة متقدمة وتوصيف خلوي مفصل.
من المستجيبين الأوائل إلى طاقم الإصلاح
بعد إصابة الشريان مباشرة، تسربت الخلايا المناعية إلى جدار الوعاء، وبلغت ذروتها خلال يومين تقريبًا. في هذه المرحلة المبكرة، أظهرت معظم البالماكروفاجات نمطًا «التهابيًا» كلاسيكيًا مناسبًا لمواجهة إشارات الخطر. ولكن بحلول نحو أسبوع، ساد نوع آخر من البالماكروفاجات: نمط إصلاحي مهيأ لإعادة بناء النسيج وتشجيع نمو الخلايا العضلية الملساء. تمكن الباحثون من فصل هذه المجموعات باستخدام علامات سطحية والتوقيت، وأظهروا أن كلًا من البالماكروفاجات الالتهابية والإصلاحية نشأت في معظمها من وحيدات النوى المتداولة التي جُذبت من الدم. عندما أزالوا تجريبيًا البالماكروفاجات خلال المرحلة اللاحقة الإصلاحية، انخفض انقسام خلايا العضلات الملساء بشدة وفشلت الطبقة الداخلية غير الطبيعية، أو النسيج الداخلي الجديد، في التكوّن، مما يثبت أن هذه البالماكروفاجات الإصلاحية اللاحقة ضرورية للسماكة التي يمكن أن تعيد سد الشرايين.
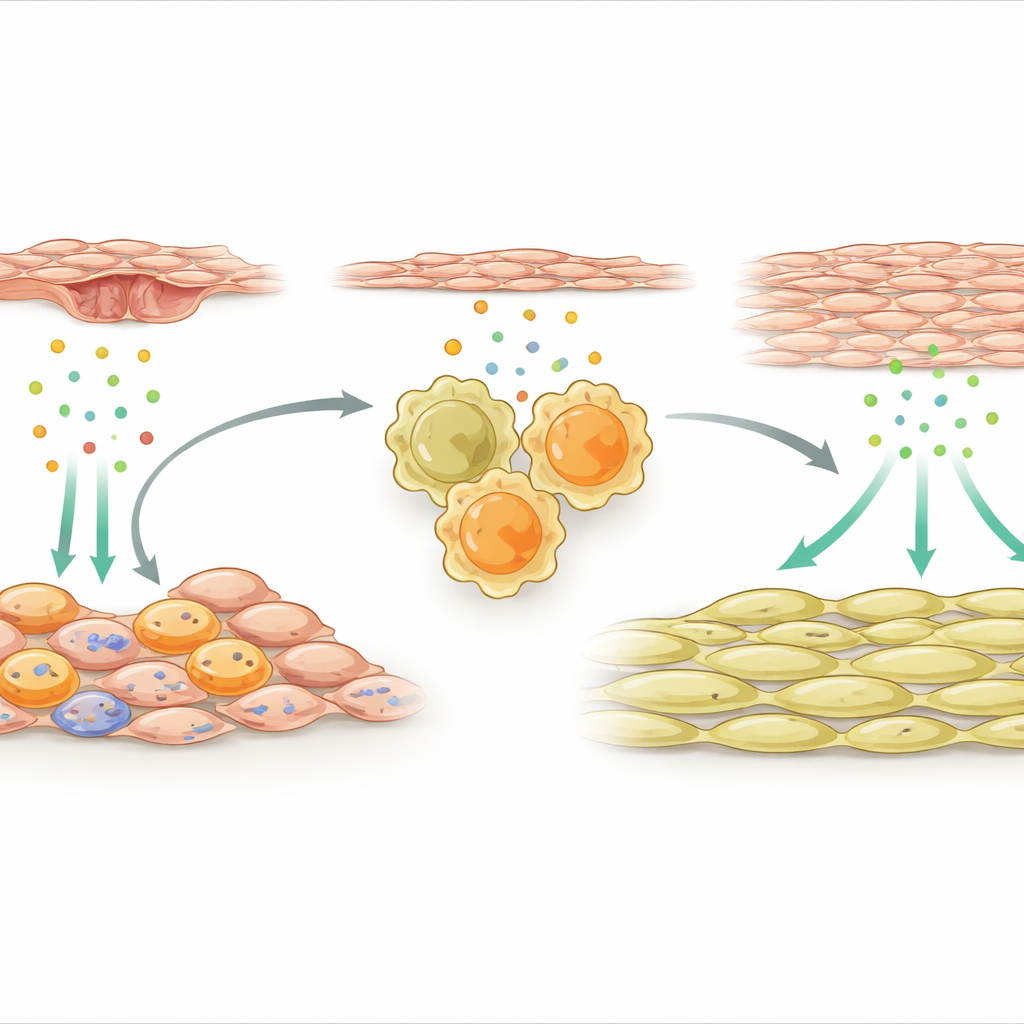
خلايا الدعم التي تشغّل بالماكروفاجات الإصلاح
ثم توجه الفريق إلى خلايا الدعم الخارجية التي تحيط بالشريان. بعد الإصابة، أصبحت مجموعة متخصصة من هذه الخلايا المتوسطة شديدة النشاط وبدأت تعبر عن العديد من الجينات المرتبطة بالمناعة. برزت إشارة واحدة: IL-33، جزيء إنذار يُفرز من الأنسجة المتضررة أو المتوترة. كانت خلايا الدعم المنتجة لـ IL-33 متجمعة قرب البالماكروفاجات في جدار الوعاء. أظهر الباحثون أن عوامل مطلقة من الخلايا البطانية المصابة، بطانة الشريان الداخلية، نشّطت مفتاحًا جزيئيًا يسمى NFκB في الخلايا المتوسطة، والذي بدوره عزز إنتاج IL-33. في كل من الفئران والمرضى البشر المصابين بإعادة تضيق مرتبطة بالدعامات، كانت مستويات IL-33 مرتفعة، مما يشير إلى أن هذا المسار ذو صلة بالسرير الإكلينيكي.
تتابع كيميائي يؤدي إلى سماكة الوعاء
يعمل IL-33 بالارتباط بمستقبل معروف باسم ST2 على الخلايا المناعية. وجدت الدراسة أنه بعد إصابة الشريان، تحمل العديد من البالماكروفاجات الإصلاحية في الجدار هذا المستقبل. عندما حفز IL-33 من خلايا الدعم الخارجية البالماكروفاجات الحاملة ST2، دفعها ذلك إلى حالة إصلاحية شديدة وأدى إلى إفراز بروتين آخر، الأوستيوبونتين. عمل الأوستيوبونتين بعد ذلك مباشرة على خلايا العضلات الملساء، محرضًا إياها على التكاثر والتكدس على داخل الشريان، مكونًا طبقة سميكة تضيق ممر تدفق الدم. إذا أزاله الباحثون IL-33 تحديدًا من الخلايا المتوسطة، أو أزالوا ST2 من البالماكروفاجات، أو حجبوا الأوستيوبونتين بواسطة جزيئات كاتمة للجينات محشورة في هلام موضعي، تقلص نمو العضلات الملساء وبقي الشريان أكثر انفتاحًا.
أفكار جديدة للحفاظ على بقاء الدعامات مفتوحة
للغير متخصصين، الرسالة المركزية هي أن إعادة التضيق الضارة للشرايين بعد تركيب الدعامات ليست مجرد مشكلة خلايا العضلات الملساء التي تتصرف بشكل خاطئ بمفردها. بل إنها مُنسقة بواسطة حوار بين خلايا الدعم الخارجية للوعاء وفئة معينة من البالماكروفاجات «الإصلاحية». تؤدي الإصابة إلى إفراز خلايا الدعم لـ IL-33، الذي ينشط البالماكروفاجات الحاملة ST2، والتي تفرز بدورها الأوستيوبونتين لتحفيز نمو العضلات الملساء بشكل مفرط. إن مقاطعة سلسلة IL-33–ST2–الأوستيوبونتين موضعيًا في موقع الإصابة منعت السماكة المفرطة في الفئران. وهذا يقترح مستقبلًا قد تُدمَج فيه الدعامات مع هلامات أو طبقات ذكية تضبط الشفاء بدقة بدلاً من قمعه قسرًا، مما يساعد الشرايين على إصلاح نفسها دون الانغلاق مرة أخرى.
الاستشهاد: Ping, Y., Qin, Z., Huang, X. et al. Perivascular mesenchymal cells instruct ST2+ reparative macrophages to promote endovascular injury-induced neointimal hyperplasia in mice. Nat Commun 17, 3635 (2026). https://doi.org/10.1038/s41467-026-68587-x
الكلمات المفتاحية: إصلاح الأوعية الدموية, البالماكروفاجات, إشارة IL-33, إعادة التضيق, خلايا العضلات الملساء