Clear Sky Science · ru
Периневральные мезенхимальные клетки направляют ST2+ репаративные макрофаги для продвижения неоинтимальной гиперплазии, вызванной эндоваскулярным повреждением у мышей
Почему восстановление поврежённых артерий может давать обратный эффект
Когда врачи расширяют забитые коронарные артерии с помощью крошечных металлических стентов, они спасают жизни, восстанавливая кровоток. Но у многих пациентов лечёный сосуд постепенно снова сужается: клетки стенки сосуда начинают избыточно разрастаться. В этом исследовании на мышах ставится ключевой вопрос, стоящий за этой проблемой: какие именно клетки внутри артерии решают, останется ли заживление плавным или перерастёт в вредную гиперплазию, способную вновь перекрыть сосуд?
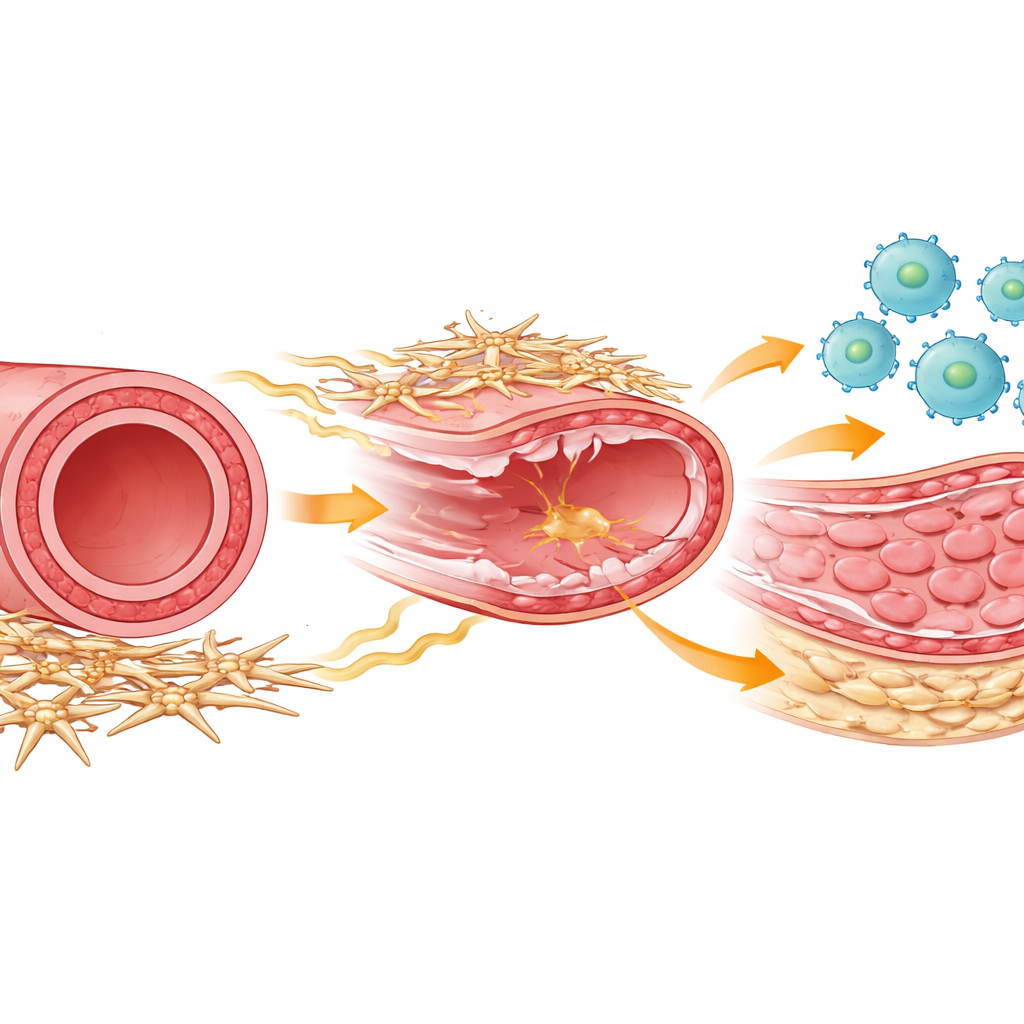
Участники процесса заживления артерии
Внутри каждой артерии несколько типов клеток вместе обеспечивают восстановление повреждений. Иммунные клетки — макрофаги — устремляются к месту травмы, чтобы убрать мусор и координировать ремонт. Гладкомышечные клетки образуют мышечный средний слой, который может утолщаться и сужать сосуд при избыточном делении. Снаружи артерии располагается менее известная группа поддерживающих клеток, часто называемых мезенхимальными или стромальными, которые поддерживают структуру сосуда и обмениваются химическими сигналами с соседями. Авторы использовали модель у мышей, имитирующую соскабливание при установке стента, и затем отслеживали поведение всех этих типов клеток во времени с помощью мощных методов одиночноклеточного чтения генов и детального профильного анализа клеток.
От первичных реагентов к ремонтной бригаде
Непосредственно после повреждения артериальной стенки иммунные клетки заполнили ткань, достигнув пика в течение нескольких дней. На ранней стадии большинство макрофагов имели классический «воспалительный» профиль, подходящий для борьбы с сигналами опасности. Но примерно через неделю доминировал другой тип макрофагов: репаративный, ориентированный на восстановление тканей и стимулирование роста гладкомышечных клеток. Исследователи смогли разделить эти группы по поверхностным маркерам и по времени появления, и показали, что и воспалительные, и репаративные макрофаги в основном происходят из циркулирующих моноцитов, привлечённых из крови. Когда макрофаги экспериментально удаляли в более поздней, репаративной фазе, деление гладкомышечных клеток резко падало и аномальный внутренний слой — неоинтима — не формировался, что доказывает: прибывающие поздно макрофаги, ориентированные на ремонт, необходимы для утолщения, которое может заново закупорить артерии.
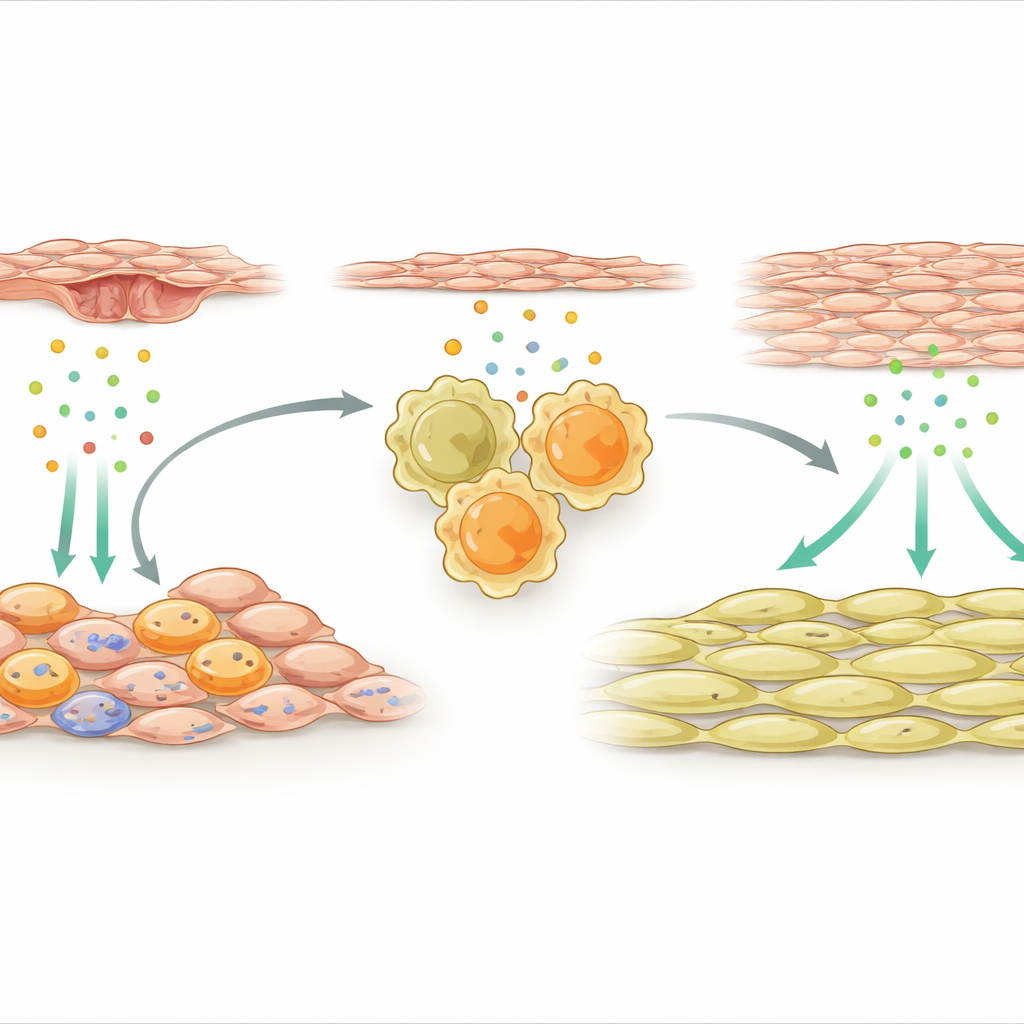
Клетки-поддержки, которые активируют ремонтные макрофаги
Далее команда обратилась к наружным поддерживающим клеткам, окружающим артерию. После травмы специализированный подтип этих мезенхимальных клеток становился сильно активным и начинал экспрессировать множество иммунных генов. Выделялся один сигнал: IL-33, молекула бедствия, выделяемая повреждёнными или под стрессом тканями. Эти IL-33-продуцирующие клетки поддержки группировались рядом с макрофагами в стенке сосуда. Исследователи показали, что факторы, высвобождаемые повреждёнными эндотелиальными клетками — внутренней выстилкой артерии, — активируют молекулярный переключатель NFκB в мезенхимальных клетках, что, в свою очередь, усиливает производство IL-33. Уровни IL-33 были повышены как у мышей, так и у пациентов с рестенозом после установки стента, что свидетельствует о клинической значимости этого пути.
Химическая цепная реакция, приводящая к утолщению сосуда
IL-33 действует через связывание с рецептором, известным как ST2, на иммунных клетках. В исследовании было показано, что после повреждения артерии многие репаративные макрофаги в стенке несут этот рецептор. Когда IL-33 от наружных клеток поддержки стимулировал ST2-положительные макрофаги, это переводило их в выраженно про-репаративный режим и вызывало выделение ими ещё одного белка — остеопонтина. Остеопонтин затем действовал непосредственно на гладкомышечные клетки, побуждая их пролиферировать и накапливаться на внутренней поверхности артерии, образуя утолщённый слой, который сужает канал кровотока. Если удаляли IL-33 специально из мезенхимальных клеток, либо устраняли ST2 в макрофагах, либо блокировали остеопонтин с помощью генно-ингибирующих молекул, упакованных в локальное гидрогелевое средство, рост гладкомышечных клеток подавлялся и артерия оставалась более проходимой.
Новые идеи для поддержания проходимости стентов
Для неспециалистов основной вывод таков: вредное повторное сужение артерий после стентирования — это не только проблема неконтролируемого поведения гладкомышечных клеток. Это скоординированный процесс, в котором участвует диалог между наружными поддерживающими клетками сосуда и определённым подтипом «репаративных» макрофагов. Повреждение заставляет клетки поддержки выделять IL-33, который активирует ST2-положительные макрофаги; те в свою очередь секретируют остеопонтин, чрезмерно стимулирующий рост гладкомышечных клеток. Локальное нарушение этой цепочки IL-33–ST2–остеопонтин на уровне места травмы предотвращало избыточное утолщение у мышей. Это наводит на идею, что в будущем стенты можно будет сочетать с «умными» гелями или покрытиями, которые тонко направляют заживление вместо грубого его подавления, помогая артериям восстановиться, не закрываясь снова.
Цитирование: Ping, Y., Qin, Z., Huang, X. et al. Perivascular mesenchymal cells instruct ST2+ reparative macrophages to promote endovascular injury-induced neointimal hyperplasia in mice. Nat Commun 17, 3635 (2026). https://doi.org/10.1038/s41467-026-68587-x
Ключевые слова: ремонт сосудов, макрофаги, сигнализация IL-33, рестеноз, гладкомышечные клетки