Clear Sky Science · zh
瞬态蛋白结构引导膜上超复合体中电子传输的表面扩散路径
细胞如何保护它们的“电力线”
你的细胞每秒钟转移数十亿个电子以合成能量分子 ATP。即便只有极小一部分电子泄漏,也可能生成危险的活性化学物质,损伤 DNA、蛋白质和脂类。该研究深入探讨了位于线粒体内膜上的微小“电力线”蛋白如何将这些电子安全、高效地从一站传到另一站,揭示了柔性、看似无序的蛋白片段和特定膜脂肪的意外作用。
线粒体内繁忙的电网
在线粒体内部,能量产生通过嵌入膜中的大型蛋白机器链运行。两个关键站点,称为复合体 III 和复合体 IV,通过一种叫细胞色素 c 的小型载体蛋白传递电子。传统上,科学家认为细胞色素 c 在水相中三维漫游,直到碰到每个复合体为止。但许多生物也将这些复合体排列成称为超复合体的簇,这提出了一个问题:形成这样的簇是否真正提高了电子穿梭的效率,还是仅仅让机械装置更有序并减少意外泄漏。
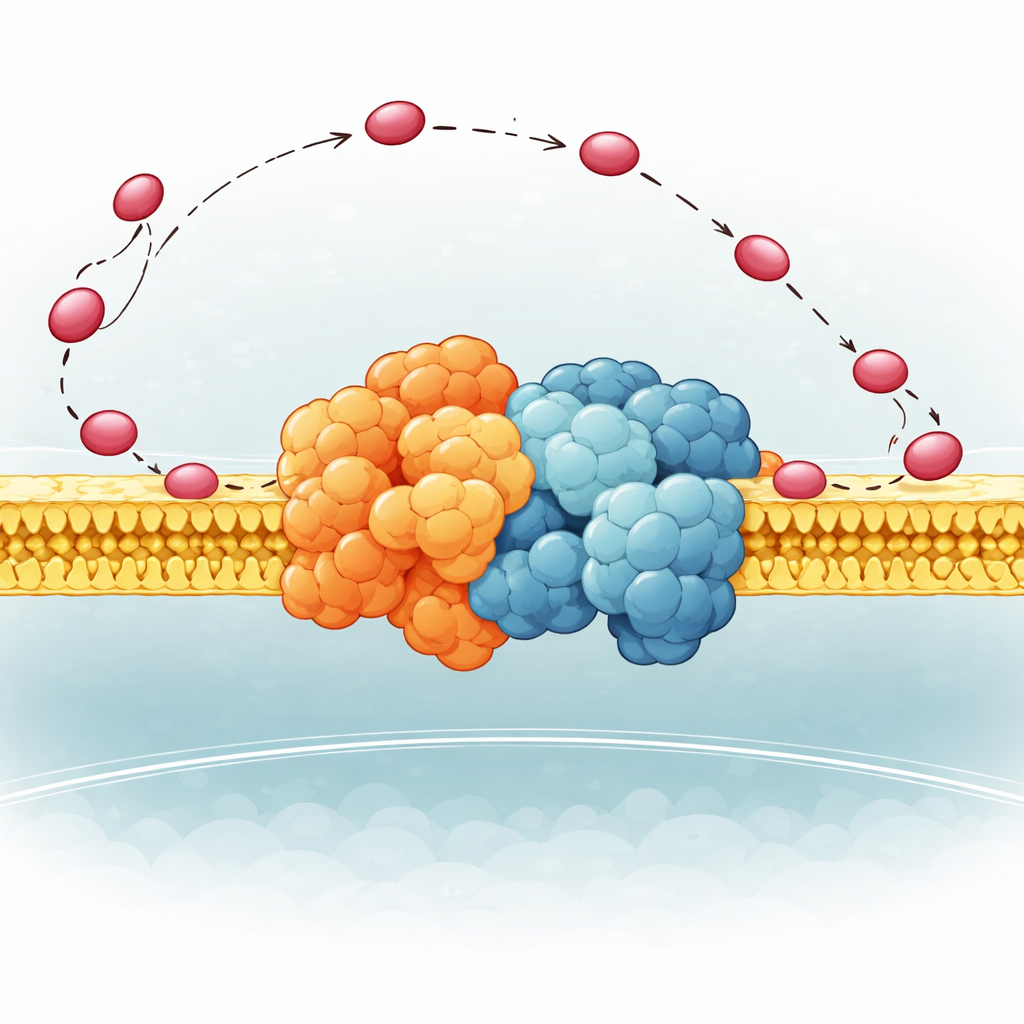
引导载体的柔性铰链
作者把注意力集中在酵母中复合体 III 的一小部分 QCR6 上,该部分含有一段又长又带负电的“铰链”片段,其结构此前过于松散难以清晰捕捉。通过结合先进的计算方法——蛋白折叠算法、分子动力学和冷冻电子显微镜,他们生成了该铰链在附着于完整的复合体 III–复合体 IV 膜上超复合体时可能呈现的一系列现实形态。他们发现 QCR6 并非静止不动:当细胞色素 c 靠近时,铰链的部分区域会折叠成暂时的螺旋并抓住载体;当细胞色素 c 从复合体 III 移向复合体 IV 时,铰链可以伸展并部分展开,沿膜表面跟随并引导它,而不是让它在周围液相中随意漂走。
作为无形引导的膜脂
膜本身也发挥着积极作用。研究团队在模型中用心磷脂取代了普通脂质,心磷脂是一种带负电的脂类,已知对健康的线粒体很重要,且在心脏病和神经退行性疾病中常被改变。模拟显示 QCR6 上的正电位点抓住心磷脂的头部,使铰链有效地系在膜上,同时护送细胞色素 c。这样的耦合使载体沿表面从复合体 III 滑向复合体 IV 的能量成本更低,而不是随机三维跳跃。当移除心磷脂时,这段旅程的能量代价急剧上升,更多的细胞色素 c 漂入体相,其位置也不再明显偏向受电子的位点。
从随机漫游到有引导的“冲浪”
通过运行大规模布朗动力学模拟,研究者追踪了细胞色素 c 在超复合体周围倾向停留的位置。在完整的 QCR6 铰链和存在阴离子脂质时,大多数细胞色素 c 分子保持靠近膜,并在复合体 III 与复合体 IV 的有效接触位点附近停留更长时间。随着铰链伸展,细胞色素 c 的优选位置云从供体侧向受体侧移动,有效地沿着复合体表面“冲浪”。这种有引导的表面扩散提高了电子传递的速度,同时不将细胞色素 c 变成机械装置的永久附着部分;载体仍能与周围池自由交换。
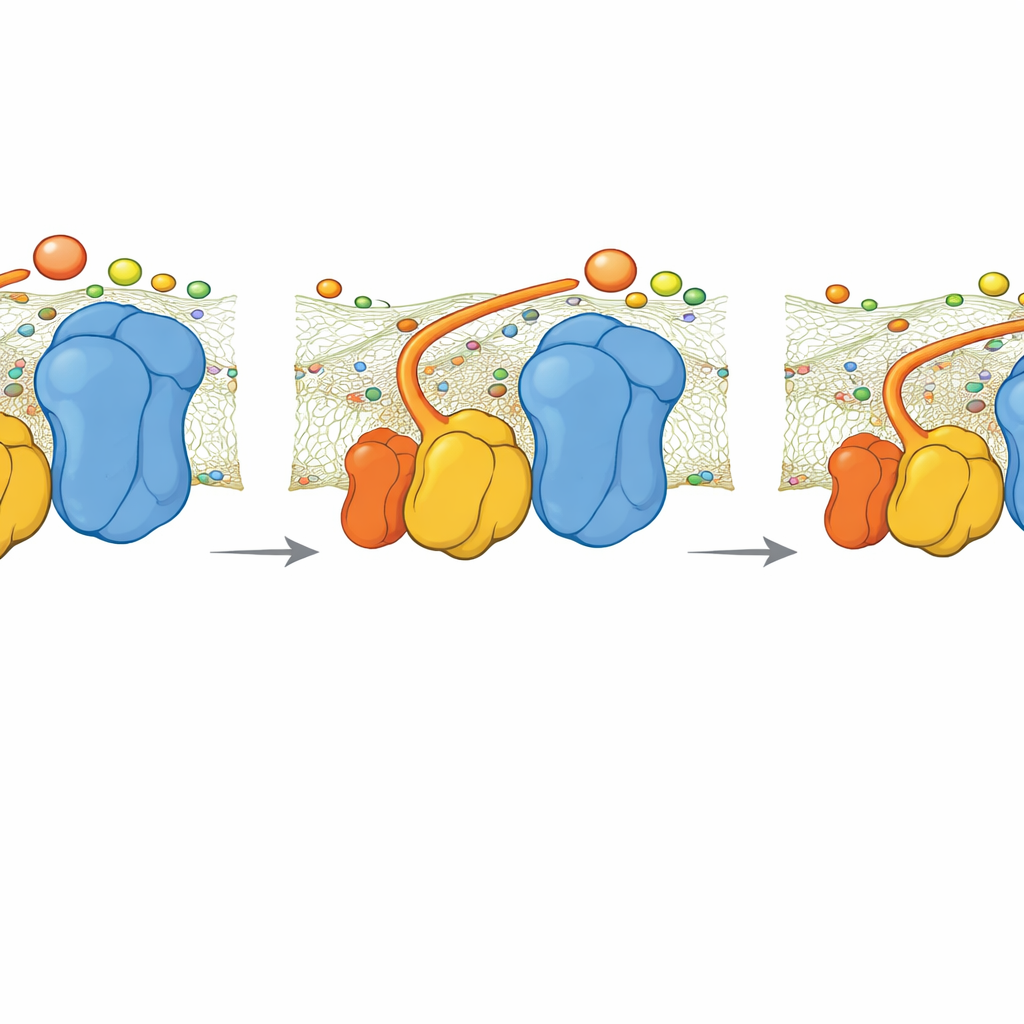
铰链缺失时会发生什么
研究团队还研究了一种缺失 QCR6 的突变酵母株。冷冻电镜成像显示,超复合体重排成更紧凑、略有不同的构型,部分恢复了表面上的连续负电荷。尽管如此,模拟表明没有 QCR6 铰链时,细胞色素 c 将电子从复合体 III 带到复合体 IV 的速率下降。一个将电子流与 ATP 产量联系起来的简单动力学模型表明,在高能量需求下,这种引导的缺失可能使 ATP 生成减少约 30%。在较低需求时,差异较小,因为较慢且不那么有序的扩散仍能满足需求。
这对健康与进化意味着什么
总体而言,这项工作支持了一个新的图景:柔性蛋白片段与带电脂质协同工作,不是作为静态支架,而是将电子载体限制在膜表面并偏向其沿着安全、有效路径移动。在酵母中,异常较长的 QCR6 铰链和丰富的心磷脂产生了这种“重折叠引导扩散”,限制电子泄漏并提高能量产出。在其他生物中,较短的铰链、不同的超复合体设计,甚至共价系缚似乎也达到相似目标——让载体靠近它们需要去的地方。理解这些微妙的引导机制或有助于解释为何心磷脂或超复合体组织的缺陷会出现在衰老、心力衰竭和神经退行性疾病中,并最终可能为微调细胞能量代谢的策略提供启示。
引用: Chan, C.K., Nguyen, J., Hryc, C.F. et al. Transient protein structure guides surface diffusion pathways for electron transport in membrane supercomplexes. Nat Commun 17, 2892 (2026). https://doi.org/10.1038/s41467-025-67110-y
关键词: 线粒体超复合体, 细胞色素c 扩散, 心磷脂, 电子传递链, QCR6 铰链