Clear Sky Science · de
Transiente Proteinstruktur lenkt Oberflächendiffusionswege für den Elektronentransport in Membran-Superkomplexen
Wie Zellen ihre Stromleitungen schützen
Sekündlich bewegen die Zellen Ihres Körpers Milliarden von Elektronen, um das Energiemolekül ATP zu erzeugen. Wenn auch nur ein kleiner Bruchteil dieser Elektronen entweicht, können daraus reaktive und schädliche Verbindungen entstehen, die DNA, Proteine und Fette angreifen. Diese Studie untersucht, wie winzige „Stromleitungs“-Proteine in der inneren Mitochondrienmembran Elektronen sicher und effizient von einer Station zur nächsten lenken und zeigt eine überraschende Rolle flexibler, scheinbar ungeordneter Proteinabschnitte sowie spezieller Membranlipide.
Das geschäftige Stromnetz in Mitochondrien
In Mitochondrien läuft die Energieproduktion über eine Kette großer Proteinkomplexe, die in einer Membran verankert sind. Zwei zentrale Stationen, bekannt als Komplex III und Komplex IV, geben Elektronen mithilfe eines kleinen Transportproteins weiter: Cytochrom c. Klassisch dachte man, Cytochrom c bewege sich dreidimensional durch das wässrige Innere, bis es auf einen Komplex trifft. Viele Organismen ordnen diese Komplexe jedoch auch zu Verbünden, sogenannten Superkomplexen, was die Frage aufwirft, ob solche Cluster tatsächlich die Effizienz des Elektronentransports verbessern oder lediglich die Maschinerie organisieren und zufällige Verluste reduzieren.
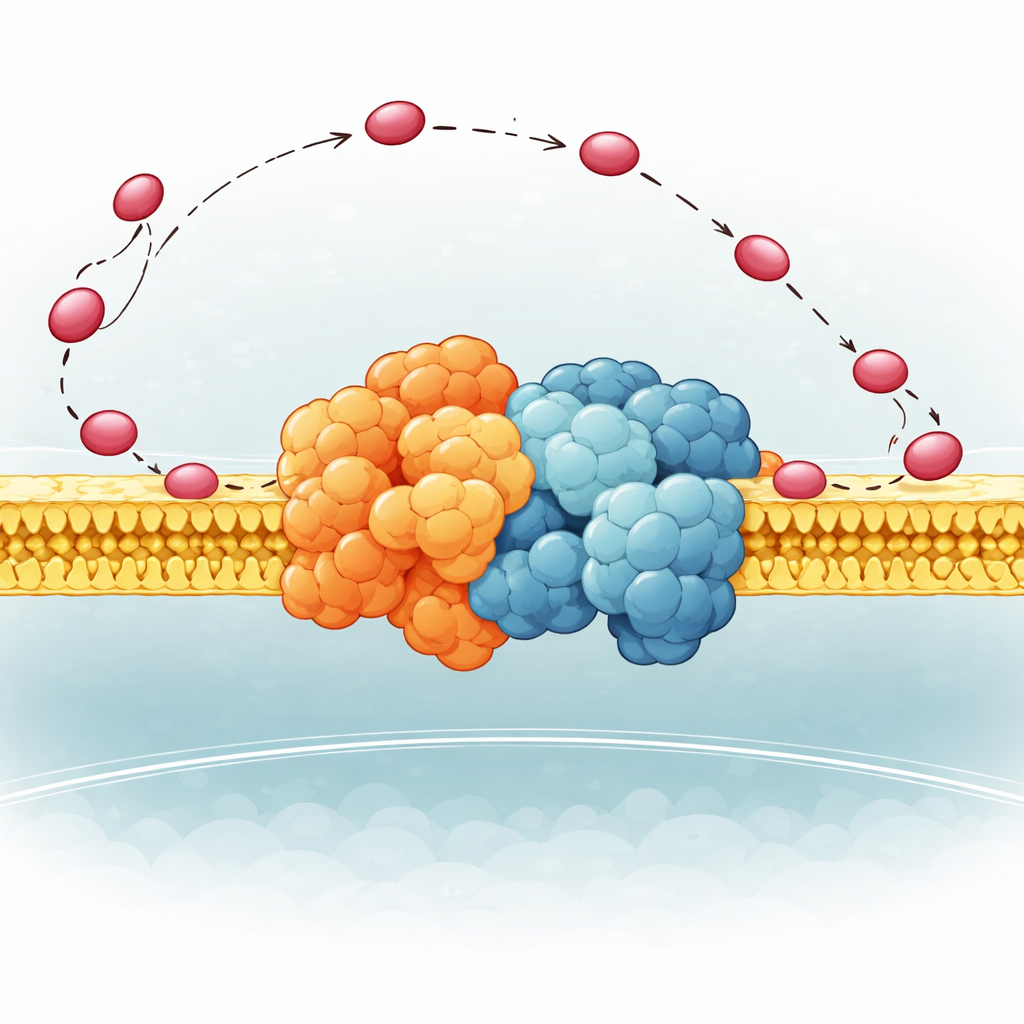
Ein flexibles Scharnier, das den Träger lenkt
Die Autoren konzentrierten sich auf einen kleinen Abschnitt von Komplex III in der Hefe, QCR6 genannt, der ein langes, negativ geladenes „Scharnier“ besitzt, dessen Struktur zuvor zu beweglich war, um klar erfasst zu werden. Mit einer Kombination moderner Rechenmethoden — Proteinfaltungsalgorithmen, Molekulardynamik und Kryo-Elektronenmikroskopie — erzeugten sie ein Ensemble realistischer Konformationen, die dieses Scharnier einnehmen kann, während es an einem vollständigen Komplex-III–Komplex-IV-Superkomplex in einer Membran befestigt ist. Sie fanden heraus, dass QCR6 nicht stillsteht: Wenn Cytochrom c nahekommt, falten sich Teile des Scharniers zu temporären Helices und greifen den Träger; während Cytochrom c sich von Komplex III zu Komplex IV bewegt, kann das Scharnier sich dehnen und teilweise entfalten, es folgen und entlang der Membranoberfläche führen, anstatt es ins umgebende Flüssigkeitsvolumen entweichen zu lassen.
Membranlipide als unsichtbare Leitlinien
Auch die Membran selbst spielt eine aktive Rolle. Das Team ersetzte generische Lipide in seinen Modellen durch Cardiolipin, ein negativ geladenes Fett, das für gesunde Mitochondrien wichtig ist und bei Herzkrankheiten sowie Neurodegeneration oft verändert vorkommt. Simulationen zeigten, dass positiv geladene Stellen auf QCR6 an die Kopfgruppen von Cardiolipin andocken und so das Scharnier effektiv an der Membran befestigen, während es Cytochrom c eskortiert. Diese Kopplung macht es energetisch günstiger für den Träger, von Komplex III zu Komplex IV entlang der Oberfläche zu gleiten, statt zufällig dreidimensional zu hüpfen. Wird Cardiolipin entfernt, steigt die energetische Hürde für diese Reise deutlich, mehr Cytochrom c treibt in die Lösung ab und seine Position wird weniger klar zugunsten der Elektronenakzeptorstelle verschoben.
Vom zufälligen Umherwandern zum gelenkten Surfen
Mit groß angelegten Brown’schen Dynamiksimulationen verfolgten die Forschenden, wo Cytochrom c sich um den Superkomplex herum aufzuhalten pflegt. Mit intaktem QCR6-Scharnier und anionischen Lipiden verbleiben die meisten Cytochrom-c-Moleküle nahe der Membran und verweilen länger an produktiven Kontaktstellen von Komplex III und Komplex IV. Wenn sich das Scharnier ausstreckt, verschiebt sich die bevorzugte Wolke von Cytochrom-c-Positionen von der Donor- zur Akzeptorseite und „surft“ dadurch effektiv entlang der Komplexoberfläche. Diese gelenkte Oberflächendiffusion verbessert die Geschwindigkeit der Elektronenübergabe, ohne Cytochrom c zu einem dauerhaft gebundenen Teil der Maschinerie zu machen; die Träger können weiterhin frei mit dem umgebenden Pool ausgetauscht werden.
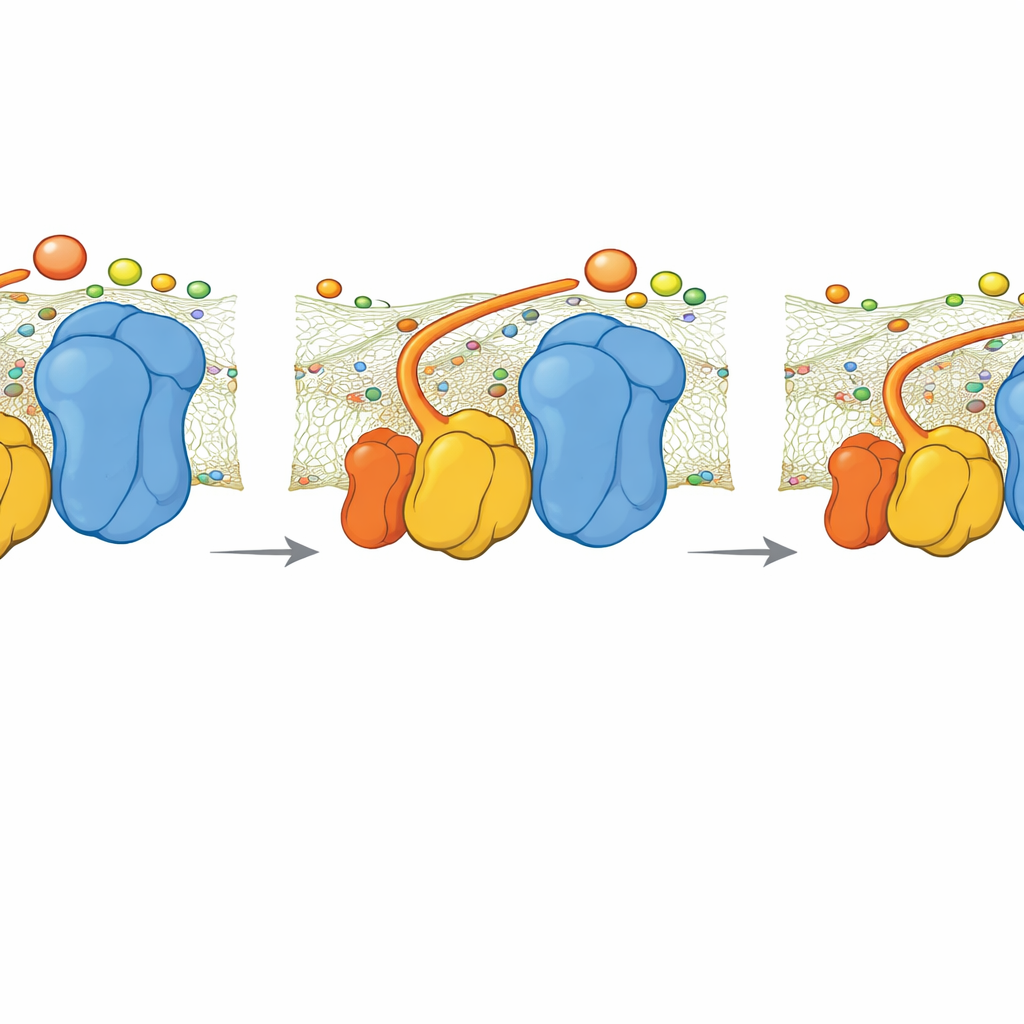
Was passiert, wenn das Scharnier fehlt
Das Team untersuchte außerdem einen mutanten Hefestamm ohne QCR6. Kryo-EM-Aufnahmen zeigten, dass sich der Superkomplex in eine kompaktere, leicht veränderte Form umordnet, die teilweise eine durchgehende negative Ladung über die Oberfläche wiederherstellt. Dennoch zeigten Simulationen, dass ohne das QCR6-Scharnier die Rate, mit der Cytochrom c Elektronen von Komplex III zu Komplex IV überträgt, sinkt. Ein einfaches kinetisches Modell, das den Elektronenfluss mit der ATP-Produktion verknüpft, legt nahe, dass unter hoher Energieanforderung dieser Verlust an Lenkung die ATP-Produktion um etwa 30 Prozent reduzieren könnte. Bei niedrigerer Nachfrage ist der Unterschied geringer, weil langsamere, weniger organisierte Diffusion noch ausreicht.
Warum das für Gesundheit und Evolution wichtig ist
In der Summe stützt die Arbeit ein neues Bild: Statt als statische Gerüste zu wirken, kooperieren flexible Proteinsegmente und geladene Lipide, um Elektronenträger an der Membranoberfläche zu halten und ihre Bewegung entlang sicherer, produktiver Routen zu lenken. In Hefe erzeugen ein ungewöhnlich langes QCR6-Scharnier und reichlich Cardiolipin diese „refolding-guided diffusion“, die Elektronenverluste begrenzt und die Energieausbeute steigert. In anderen Organismen scheinen kürzere Scharniere, andere Superkomplex-Designs oder sogar kovalente Verbindungen ein ähnliches Ziel zu verfolgen — die Träger dort zu halten, wo sie gebraucht werden. Das Verständnis dieser feinen Lenkmechanismen kann helfen zu erklären, warum Defekte in Cardiolipin oder in der Organisation von Superkomplexen bei Alterung, Herzversagen und neurodegenerativen Erkrankungen auftreten und könnte langfristig Ansätze zur Feinabstimmung des zellulären Energiestoffwechsels informieren.
Zitation: Chan, C.K., Nguyen, J., Hryc, C.F. et al. Transient protein structure guides surface diffusion pathways for electron transport in membrane supercomplexes. Nat Commun 17, 2892 (2026). https://doi.org/10.1038/s41467-025-67110-y
Schlüsselwörter: mitochondriale Superkomplexe, Diffusion von Cytochrom c, Cardiolipin, Elektronentransportkette, QCR6-Scharnier