Clear Sky Science · it
La struttura proteica transitoria guida le vie di diffusione superficiale per il trasporto di elettroni nei supercomplessi di membrana
Come le cellule proteggono le loro linee elettriche
Ogni secondo, le cellule del tuo corpo spostano miliardi di elettroni per produrre la molecola energetica ATP. Se anche una piccola frazione di quegli elettroni sfugge, può generare reagenti reattivi pericolosi che danneggiano DNA, proteine e lipidi. Questo studio indaga come piccole proteine “linee elettriche” sulla membrana interna dei mitocondri guidino questi elettroni in modo sicuro ed efficiente da una stazione all’altra, rivelando un ruolo sorprendente per porzioni proteiche flessibili e apparentemente disordinate e per particolari grassi di membrana.
La fitta rete elettrica dentro i mitocondri
All’interno dei mitocondri, la produzione di energia avviene attraverso una catena di grandi macchine proteiche incastonate in una membrana. Due stazioni chiave, note come Complesso III e Complesso IV, si passano gli elettroni usando una piccola proteina trasportatrice chiamata citocromo c. Tradizionalmente, i ricercatori immaginavano il citocromo c che diffonde in tre dimensioni nel fluido interno finché non urta ciascun complesso. Molti organismi tuttavia dispongono questi complessi in aggregati detti supercomplessi, sollevando il dubbio se la formazione di tali raggruppamenti migliori realmente l’efficienza del trasferimento degli elettroni, o limiti semplicemente l’organizzazione della macchina riducendo le fughe accidentali.
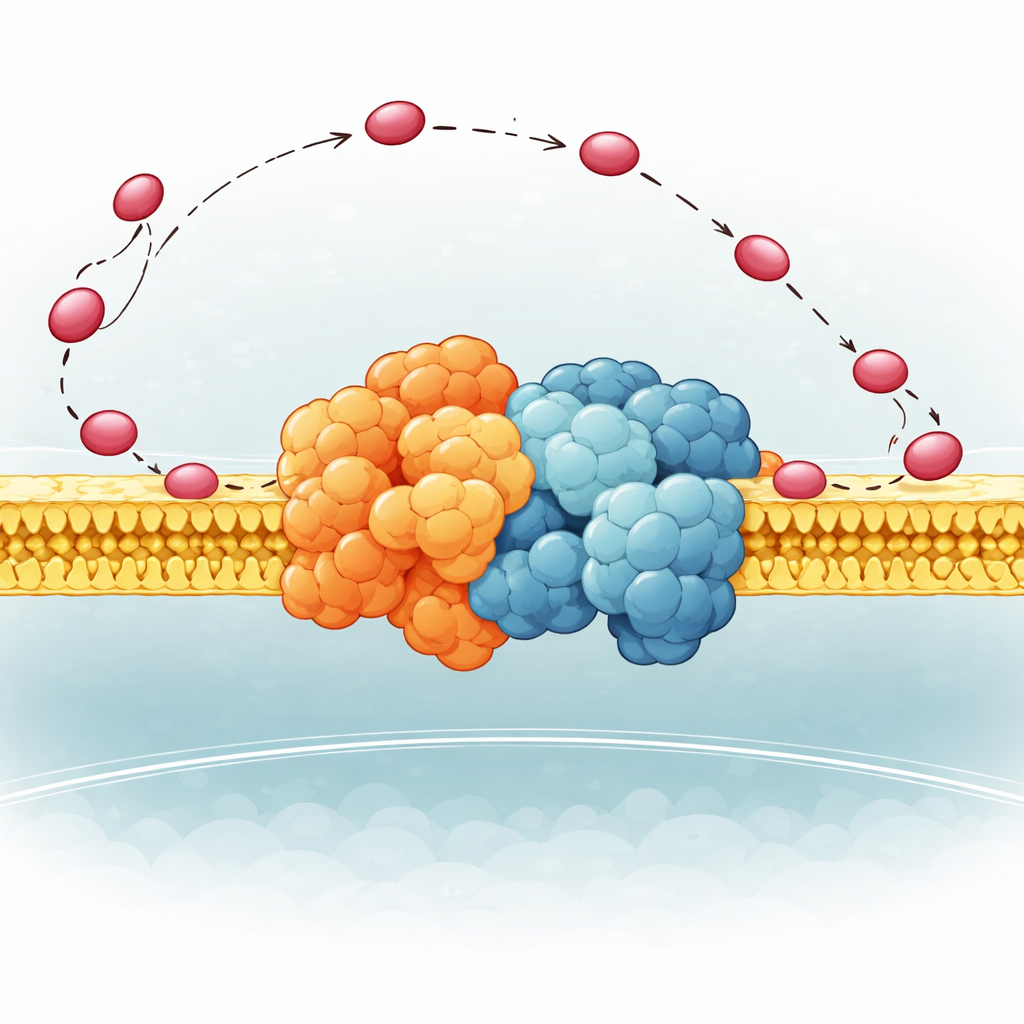
Una cerniera flessibile che indirizza il trasportatore
Gli autori si sono concentrati su una piccola parte del Complesso III nella lievito chiamata QCR6, che possiede un lungo segmento “cerniera” carico negativamente la cui struttura era stata troppo mobile per essere catturata chiaramente in precedenza. Usando una combinazione di metodi avanzati—algoritmi di folding proteico, dinamica molecolare e criomicroscopia elettronica—hanno generato un insieme di conformazioni realistiche che questa cerniera può assumere mentre è attaccata a un supercomplesso Comple- so III–Complesso IV integrato in una membrana. Hanno scoperto che QCR6 non è immobile: quando il citocromo c si avvicina, parti della cerniera si ripiegano in eliche temporanee e afferrano il trasportatore; mentre il citocromo c passa dal Complesso III verso il Complesso IV, la cerniera può allungarsi e parzialmente disfarsi, seguendolo e guidandolo lungo la superficie della membrana invece di lasciarlo vagare nel fluido circostante.
I grassi di membrana come guide invisibili
Anche la membrana gioca un ruolo attivo. Il gruppo ha sostituito i lipidi generici nei loro modelli con cardiolipina, un grasso carico negativamente noto per essere importante per i mitocondri sani e spesso alterato nelle malattie cardiache e neurodegenerative. Le simulazioni hanno mostrato che siti carichi positivamente su QCR6 si legano ai gruppi testa della cardiolipina, ancorando di fatto la cerniera alla membrana mentre accompagna il citocromo c. Questo accoppiamento rende energeticamente più favorevole per il trasportatore scorrere dalla superficie del Complesso III a quella del Complesso IV, anziché compiere salti casuali in tre dimensioni. In assenza di cardiolipina, il costo energetico di questo percorso aumentava bruscamente, più citocromo c migrate nel fluido di fondo e la sua posizione risultava meno chiaramente orientata verso il sito accettore di elettroni.
Da vagabondaggio casuale a surf guidato
Eseguendo ampie simulazioni di dinamica browniana, i ricercatori hanno tracciato dove il citocromo c tende a soffermarsi intorno al supercomplesso. Con una cerniera QCR6 intatta e lipidi anionici presenti, la maggior parte delle molecole di citocromo c rimane vicina alla membrana e trascorre più tempo vicino ai siti di contatto produttivi sul Complesso III e sul Complesso IV. Man mano che la cerniera si estende, la nuvola preferenziale di posizioni del citocromo c si sposta dal lato donatore al lato accettore, effettivamente “surfando” lungo la superficie del complesso. Questa diffusione superficiale guidata migliora la rapidità del trasferimento degli elettroni senza trasformare il citocromo c in una parte permanentemente attaccata della macchina; i trasportatori possono ancora scambiarsi liberamente con la riserva cellulare circostante.
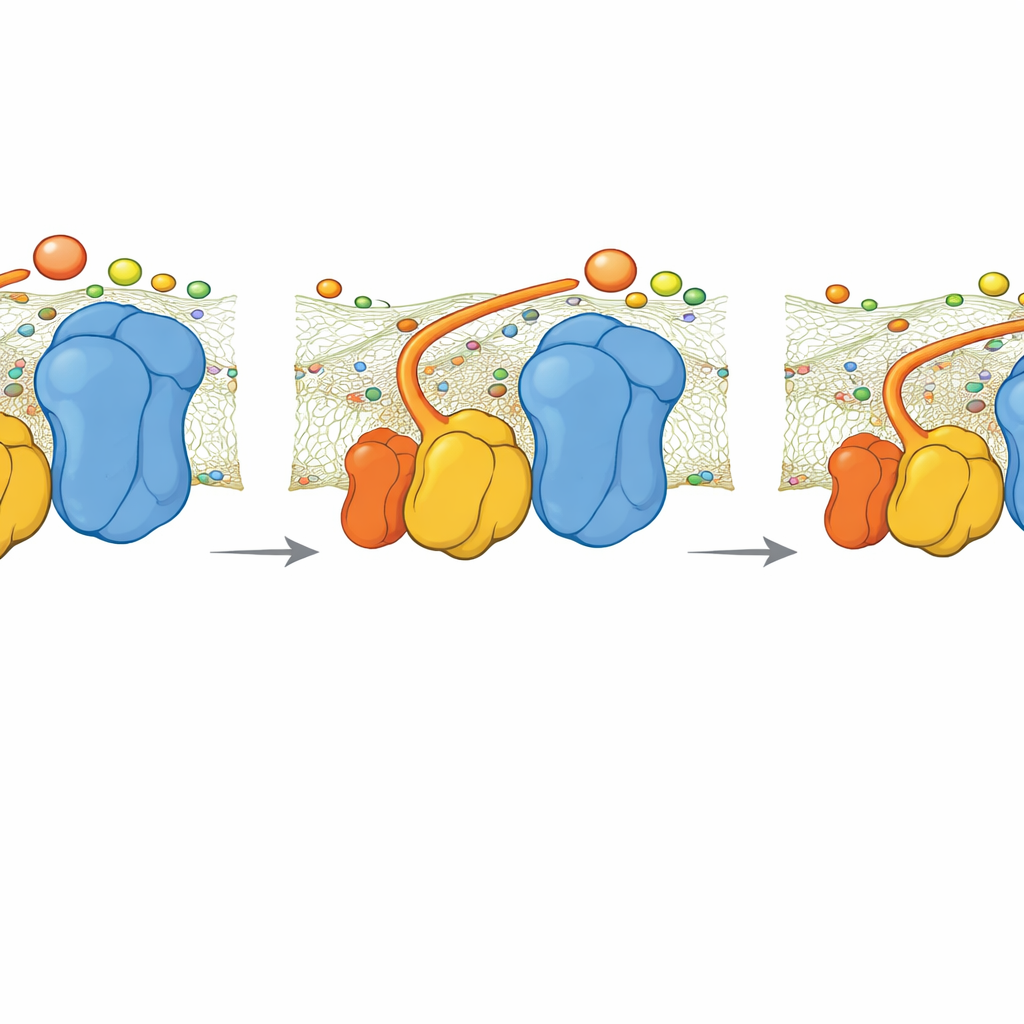
Cosa succede quando manca la cerniera
Il gruppo ha studiato anche un ceppo di lievito mutante privo di QCR6. Le immagini cryo-EM hanno mostrato che il supercomplesso si riorganizza in una forma più compatta e lievemente diversa che in parte ripristina una carica negativa continua sulla superficie. Tuttavia, le simulazioni hanno rivelato che senza la cerniera QCR6 la velocità con cui il citocromo c trasferisce elettroni dal Complesso III al Complesso IV diminuisce. Un semplice modello cinetico, che collega il flusso di elettroni alla produzione di ATP, suggerisce che sotto alta domanda energetica questa perdita di guida potrebbe ridurre la produzione di ATP di circa il 30 percento. A domanda inferiore, la differenza è più piccola, perché una diffusione più lenta e meno organizzata rimane comunque sufficiente.
Perché questo è importante per salute ed evoluzione
Messo insieme, il lavoro sostiene un nuovo quadro: invece di agire come impalcature statiche, segmenti proteici flessibili e lipidi carichi cooperano per confinare i trasportatori di elettroni alla superficie della membrana e orientarne il moto lungo percorsi sicuri e produttivi. Nel lievito, una cerniera QCR6 insolitamente lunga e l’abbondanza di cardiolipina generano questa “diffusione guidata dal ripiegamento” che limita le fughe di elettroni e aumenta la resa energetica. In altri organismi, cerniere più corte, diversi disegni di supercomplessi o persino legami covalenti sembrano perseguire lo stesso obiettivo—mantenere i trasportatori vicini al luogo in cui servono. Comprendere questi sottili meccanismi di guida può contribuire a spiegare perché difetti nella cardiolipina o nell’organizzazione dei supercomplessi si manifestano nell’invecchiamento, nell’insufficienza cardiaca e nelle malattie neurodegenerative, e potrebbe infine informare strategie per modulare il metabolismo energetico cellulare.
Citazione: Chan, C.K., Nguyen, J., Hryc, C.F. et al. Transient protein structure guides surface diffusion pathways for electron transport in membrane supercomplexes. Nat Commun 17, 2892 (2026). https://doi.org/10.1038/s41467-025-67110-y
Parole chiave: supercomplessi mitocondriali, diffusione del citocromo c, cardiolipina, catena di trasporto degli elettroni, cerniera QCR6