Clear Sky Science · ar
البنية البروتينية العابرة توجه مسارات الانتشار السطحي لنقل الإلكترونات في فوق-المجمعات الغشائية
كيف تحافظ الخلايا على سلامة خطوط طاقتها
كل ثانية، تحرّك خلايا جسمك مليارات الإلكترونات لتصنيع جزيء الطاقة ATP. إذا تسربت نسبة صغيرة من تلك الإلكترونات، قد تتكوّن مركبات تفاعلية خطرة تضرّ الحمض النووي والبروتينات والدهون. تتعمّق هذه الدراسة في كيفية توجيه بروتينات "الخط الكهربائي" الصغيرة على الغشاء الداخلي للميتوكوندريا لهذه الإلكترونات بأمان وكفاءة من محطة إلى أخرى، كاشفة دوراً مفاجئاً لقطع بروتينية مرنة تبدو غير منظمة ودهون غشائية خاصة.
شبكة الطاقة المزدحمة داخل الميتوكوندريا
داخل الميتوكوندريا، يجري إنتاج الطاقة عبر سلسلة من الآلات البروتينية الكبيرة المضمنة في الغشاء. محطتان رئيسيتان، تعرفان بالمجمع III والمجمع IV، تنقلان الإلكترونات باستخدام ناقل بروتيني صغير يُدعى سيتوكروم c. تقليدياً، تصوّر العلماء سيتوكروم c ينجرف في ثلاثة أبعاد عبر الوسط المائي حتى يصطدم بكل مجمع. لكن العديد من الكائنات تصطف أيضاً تلك المجمعات في تجمعات تُسمى فوق-المجمعات، مما يطرح اللغز: هل يؤدي تجميعها فعلاً إلى تحسين كفاءة نقل الإلكترونات، أم أنه يقتصر على تنظيم الآلة وتقليل التسرب العرضي؟
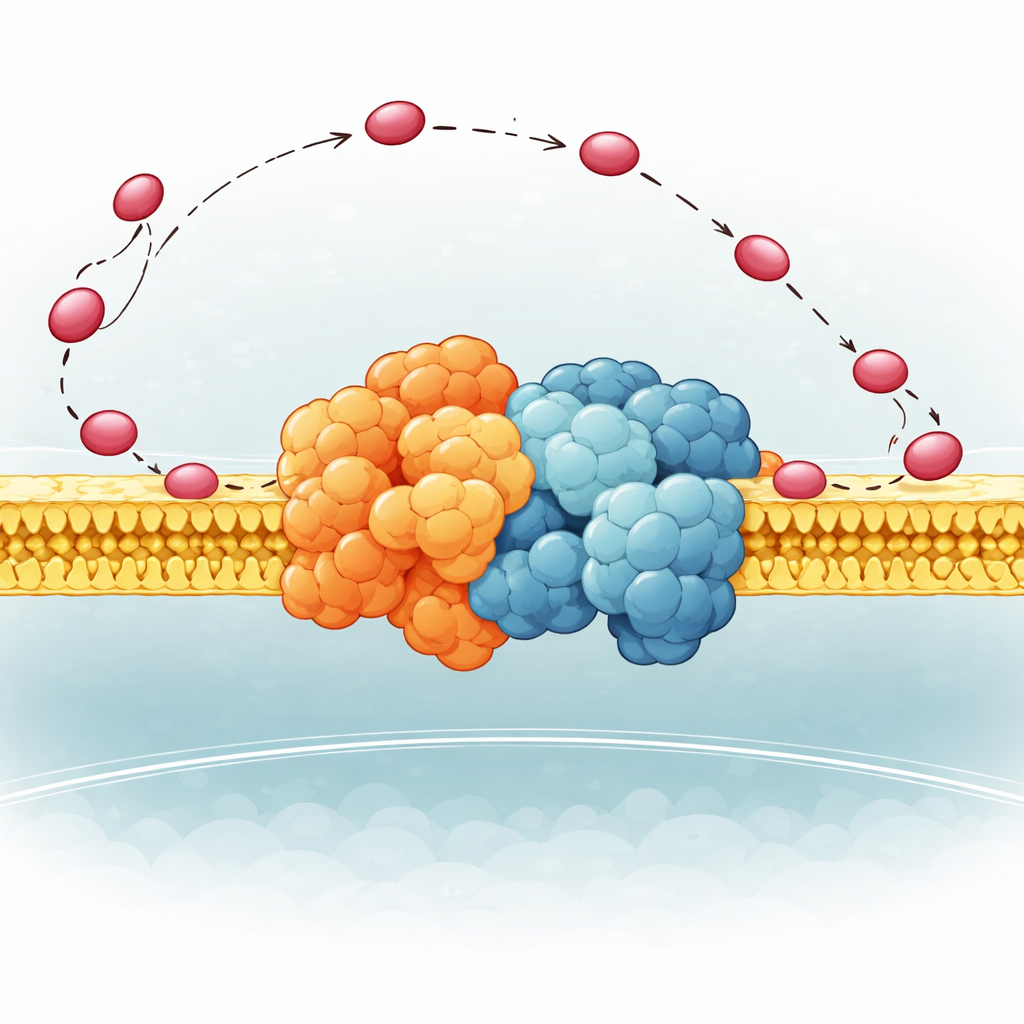
مفصل مرن يوجّه الناقل
تركّز المؤلفون على جزء صغير من المجمع III في الخميرة يُدعى QCR6، الذي يحتوي على مقطع "مفصلي" طويل مشحون سلبياً كانت بنيته مرنة جداً لدرجة أنه لم تُلتقط بوضوح سابقاً. باستخدام مزيج من طرق حاسوبية متقدمة—خوارزميات طي البروتين، الديناميكا الجزيئية، والمجهر الإلكتروني بالتبريد—أنشأوا مجموعة أشكال واقعية يمكن أن يتخذها هذا المفصل وهو متصل بفوق-المجمع الكامل للمجمع III–المجمع IV في غشاء. وجدوا أن QCR6 لا يظل ثابتاً: عندما يقترب سيتوكروم c، تطوي أجزاء من المفصل إلى محاور لولبية مؤقتة وتمسُك بالناقل؛ ومع انتقال سيتوكروم c من المجمع III نحو المجمع IV، يمكن أن يمتد المفصل وينفك جزئياً، متتبّعاً وموّجهاً إياه على سطح الغشاء بدلاً من السماح له بالانجراف إلى السائل المحيط.
الدهون الغشائية كأدلة غير مرئية
يلعب الغشاء ذاته دوراً فعالاً أيضاً. استبدل الفريق الدهون العامة في نماذجهم بالكارديوليبن، دهن مشحون سلبياً معروف بأهميته لصحة الميتوكوندريا وغالباً ما يتغير في أمراض القلب والتنكس العصبي. أظهرت المحاكيات أن بقعاً موجبة الشحنة على QCR6 ترتبط برؤوس جزيئات الكارديوليبن، مما يقيّد المفصل إلى الغشاء أثناء مرافقته لسيتوكروم c. هذا الاقتران يجعل الأمر أرخص طاقياً للناقل أن ينزلق من المجمع III إلى المجمع IV على السطح، بدلاً من القفز عشوائياً في ثلاثة أبعاد. عندما أُزيل الكارديوليبن، ارتفع التكلفة الطاقية لهذه الرحلة بشكل حاد، واندفع المزيد من سيتوكروم c إلى المحلول العام، وأصبحت مواضعه أقل انحيازاً نحو موقع قبول الإلكترون.
من التجوال العشوائي إلى الركوب الموجي الموجه
من خلال تشغيل محاكيات ديناميكا براونية واسعة النطاق، تتبّع الباحثون أين يميل سيتوكروم c إلى التوقف حول الفوق-المجمع. مع وجود مفصل QCR6 سليم ودهون سالبة الشحنة، تبقى معظم جزيئات سيتوكروم c قريبة من الغشاء وتقضي وقتاً أطول بالقرب من مواقع التماس المنتجة على المجمع III والمجمع IV. مع امتداد المفصل، يتحول سحابة المواضع المفضلة لسيتوكروم c من جهة المانح إلى جهة المستقبل، لتقوم فعلياً بـ"الركوب الموجي" على طول سطح المجمع. يحسّن هذا الانتشار السطحي الموجه سرعة تبادل الإلكترونات دون تحويل سيتوكروم c إلى جزء ملتصق دائماً بالآلة؛ إذ لا يزال بإمكان الناقلين تبادل الاتصال بحرية مع المجموعة المحيطة.
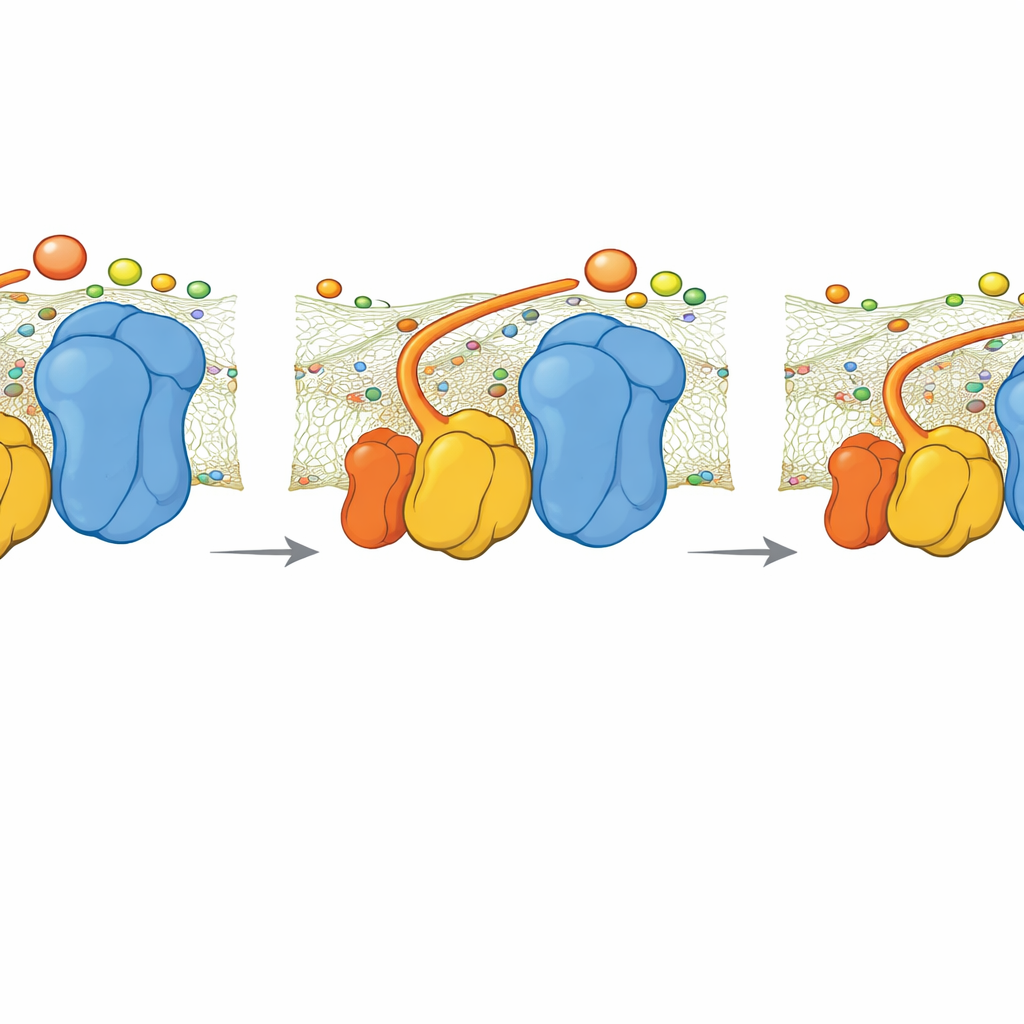
ماذا يحدث عند غياب المفصل
درس الفريق أيضاً سلالة خميرة طفيلية تفتقر إلى QCR6. أظهرت صور المجهر الإلكتروني بالتبريد أن الفوق-المجمع يعاد ترتيبه إلى شكل أكثر تماسُكاً ومختلفاً قليلاً يعيد جزئياً شحنة سالبة متواصلة عبر السطح. مع ذلك، كشفت المحاكيات أنه بدون مفصل QCR6 ينخفض معدل انتقال سيتوكروم c للإلكترونات من المجمع III إلى المجمع IV. نموذج حركي بسيط يربط تدفق الإلكترونات بإنتاج ATP يشير إلى أن هذا الفقد في التوجيه قد يقلص إنتاج ATP بحوالي 30٪ تحت طلب طاقة عالٍ. عند طلب أقل، يكون الفرق أصغر، لأن الانتشار الأبطأ والأقل تنظيماً يظل كافياً.
لماذا يهم هذا للصحة والتطور
عموماً، تدعم النتائج صورة جديدة: بدلاً من أن تعمل كحوامل ثابتة، تتعاون مقاطع بروتينية مرنة ودهون مشحونة لاحتجاز ناقلات الإلكترون على سطح الغشاء وتحفيز حركتها على مسارات آمنة ومنتجة. في الخميرة، يولّد مفصل QCR6 الطويل بشكل غير عادي وكميات كبيرة من الكارديوليبن هذا "الانتشار الموجه بإعادة الطي" الذي يحدّ من تسرب الإلكترونات ويعزز إنتاج الطاقة. في كائنات أخرى، قد تخدم المفاصل الأقصر أو تصاميم فوق-المجمع المختلفة أو حتى الروابط التساهمية هدفاً مشابهاً—إبقاء الناقلين قريبين من مواقع حاجتهم. قد يساعد فهم هذه الآليات الدقيقة للتوجيه في تفسير سبب ظهور عيوب في الكارديوليبن أو تنظيم الفوق-المجمعات في الشيخوخة وفشل القلب والأمراض التنكسية العصبية، وقد يوجه مستقبلاً استراتيجيات لضبط استقلاب الطاقة الخلوية.
الاستشهاد: Chan, C.K., Nguyen, J., Hryc, C.F. et al. Transient protein structure guides surface diffusion pathways for electron transport in membrane supercomplexes. Nat Commun 17, 2892 (2026). https://doi.org/10.1038/s41467-025-67110-y
الكلمات المفتاحية: فوق-المجمعات الميتوكوندرية, انتشار السيتوكروم c, الكارديوлипين, سلسلة نقل الإلكترونات, مفصل QCR6