Clear Sky Science · sv
Övergående proteinstruktur styr ytdiffusionsvägar för elektrontransport i membransuperkomplex
Hur celler håller sina kraftledningar säkra
Varje sekund förflyttar cellerna i din kropp miljarder elektroner för att bilda energimolekylen ATP. Om även en liten andel av de elektronerna läcker bort kan de skapa reaktiva kemikalier som skadar DNA, proteiner och fetter. Denna studie undersöker hur små ”kraftlednings”proteiner på mitokondriens inre membran styr dessa elektroner säkert och effektivt från en station till nästa och avslöjar en överraskande roll för flexibla, till synes oordnade proteindelar och speciella membranfetter.
Det livliga elnätet inne i mitokondrierna
Inne i mitokondrierna sker energiproduktionen genom en kedja av stora proteinkomplex inbäddade i ett membran. Två centrala stationer, kända som komplex III och komplex IV, överför elektroner med hjälp av ett litet bärarprotein kallat cytochrom c. Traditionellt föreställde sig forskare att cytochrom c rör sig fritt i tre dimensioner genom den vattenfyllda inre ytan tills det stöter på varje komplex. Men många organismer organiserar också dessa komplex i kluster som kallas superkomplex, vilket väcker frågan om sådana kluster verkligen förbättrar hur effektivt elektroner förflyttas, eller bara håller maskineriet organiserat och minskar oavsiktliga läckor.
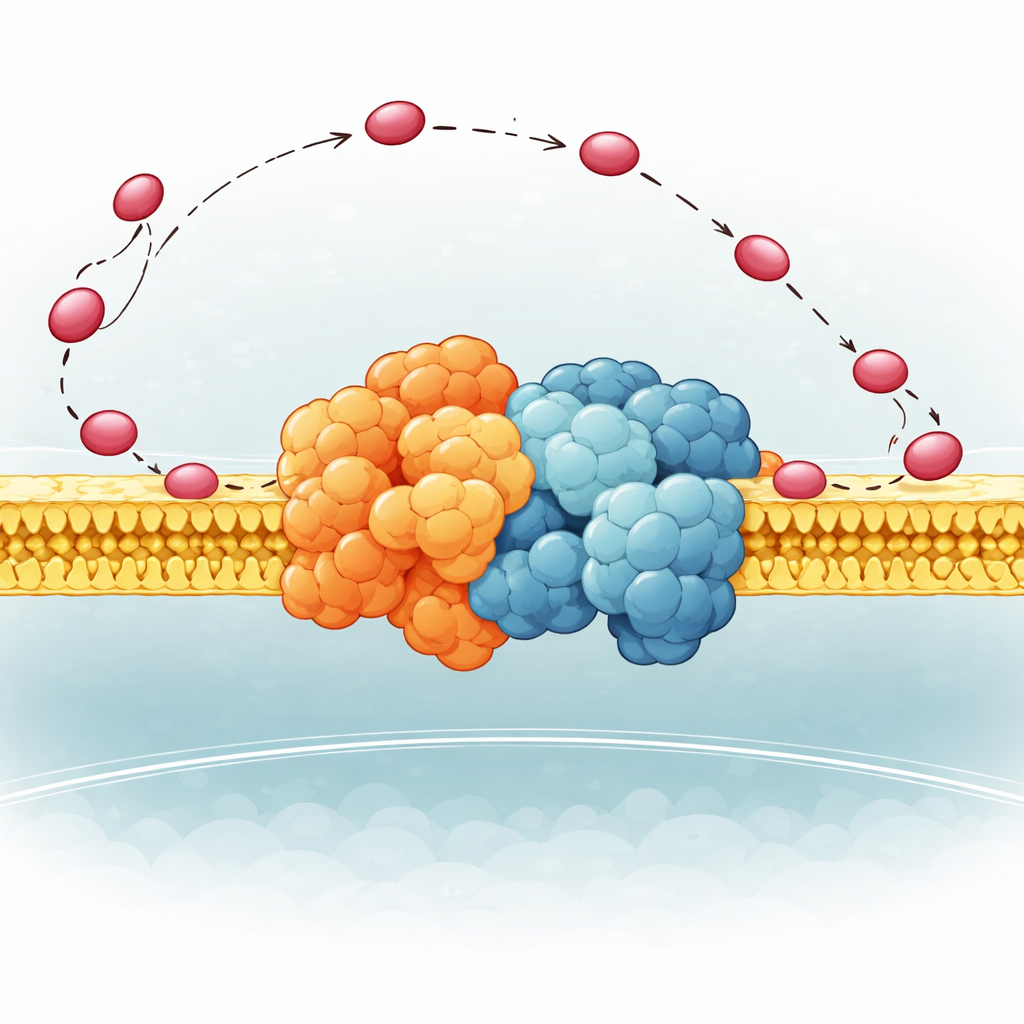
Ett flexibelt gångjärn som styr bäraren
Författarna fokuserade på en liten del av komplex III i jäst som kallas QCR6, som har ett långt, negativt laddat ”gångjärn” vars struktur tidigare varit för lös för att tydligt bestämmas. Genom att kombinera avancerade datormetoder—proteinvikningsalgoritmer, molekylär dynamik och kryoelektronmikroskopi—genererade de en samling realistiska former som detta gångjärn kan anta när det är kopplat till ett komplett komplex III–komplex IV-superkomplex i ett membran. De fann att QCR6 inte ligger still: när cytochrom c närmar sig veckas delar av gångjärnet till tillfälliga helixar och fångar bäraren; när cytochrom c rör sig från komplex III mot komplex IV kan gångjärnet sträckas ut och delvis veckas upp, följa och styra det längs membranytan i stället för att låta det irra iväg ut i omgivande vätska.
Membranfetter som osynliga vägvisare
Membranet spelar också en aktiv roll. Teamet bytte ut generiska lipider i sina modeller mot kardiolipin, en negativt laddad fettmolekyl som är viktig för friska mitokondrier och ofta förändras vid hjärtsjukdom och neurodegeneration. Simuleringarna visade att positivt laddade områden på QCR6 hakar fast i kardiolipins huvudgrupper och effektivt förankrar gångjärnet till membranet medan det eskorterar cytochrom c. Denna koppling gör det energimässigt billigare för bäraren att glida från komplex III till komplex IV längs ytan, snarare än att hoppa slumpmässigt i tre dimensioner. När kardiolipin togs bort ökade den energimässiga kostnaden för denna förflyttning kraftigt, fler cytochrom c drev ut i bulklösningen och deras position blev mindre tydligt förskjuten mot det elektronacceptanta sätet.
Från slumpvandring till vägledd surfing
Genom att köra storskaliga Brownsk dynamik-simuleringar följde forskarna var cytochrom c tenderar att dröja runt superkomplexet. Med ett intakt QCR6-gångjärn och anjoniska lipider närvarande förblir de flesta cytochrom c-molekyler nära membranet och tillbringar mer tid nära produktiva kontaktpunkter på komplex III och komplex IV. När gångjärnet förlängs skiftar den föredragna molnen av cytochrom c-positioner från donatorsidan till acceptorsidan, vilket effektivt ”surfar” längs komplexets yta. Denna vägledda ytdiffusion förbättrar hur snabbt elektroner kan överföras utan att göra cytochrom c till en permanent bunden del av maskineriet; bärarna kan fortfarande utbytas fritt med den omgivande poolen.
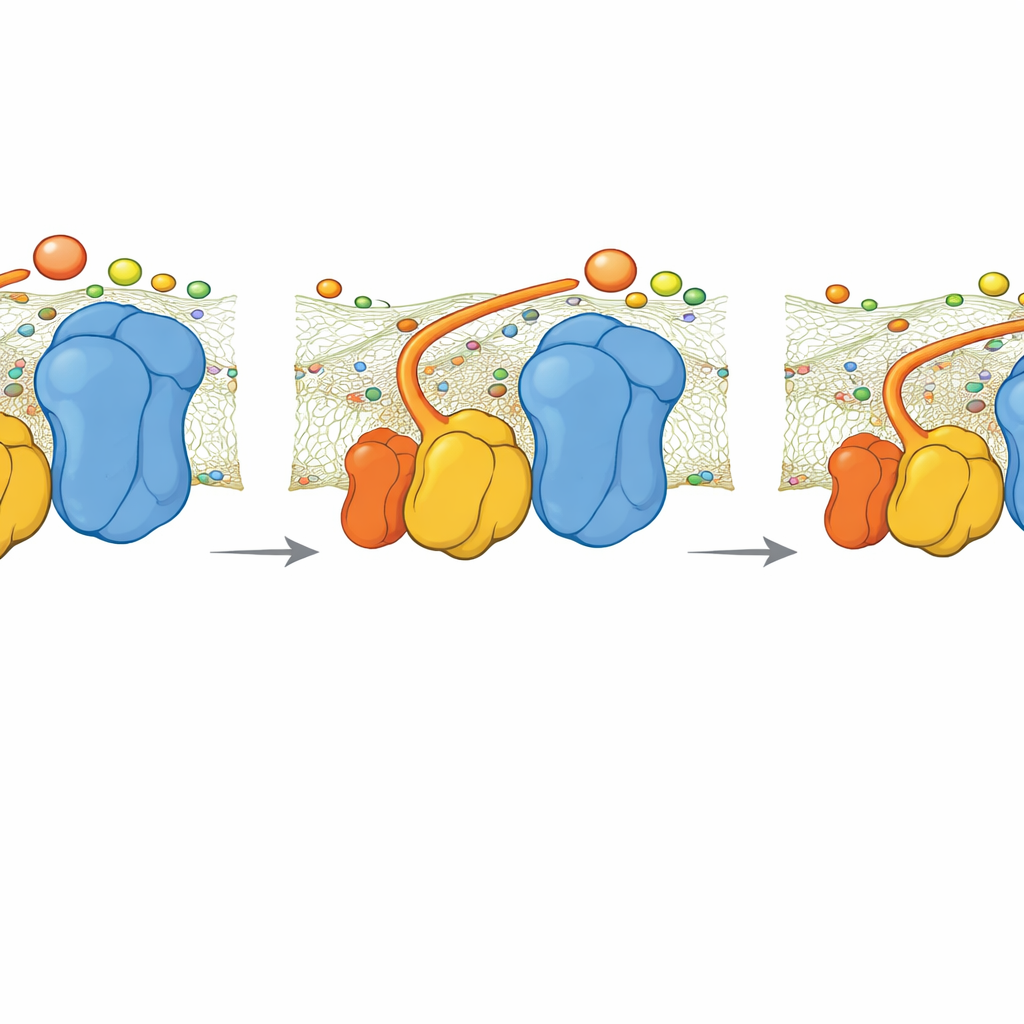
Vad händer när gångjärnet saknas
Forskarna studerade också en mutant jäststam som saknar QCR6. Kryo-EM-bilder visade att superkomplexet omarrangerar till en mer kompakt, något annorlunda form som delvis återställer en kontinuerlig negativ laddning över ytan. Trots detta visade simuleringarna att utan QCR6-gångjärnet sjunker takten med vilken cytochrom c överför elektroner från komplex III till komplex IV. En enkel kinetisk modell som kopplar elektronflöde till ATP-produktion antyder att under hög energiefterfrågan kan denna förlorade styrning minska ATP-produktionen med ungefär 30 procent. Vid lägre efterfrågan är skillnaden mindre, eftersom långsammare, mindre organiserad diffusion ändå kan räcka.
Varför detta spelar roll för hälsa och evolution
Tillsammans stöder arbetet en ny bild: i stället för att fungera som statiska ställningar samarbetar flexibla proteinsegment och laddade lipider för att begränsa elektronbärare till membranytan och förskjuta deras rörelse längs säkra, produktiva rutter. I jäst genererar ett ovanligt långt QCR6-gångjärn och rikligt med kardiolipin denna ”omvikningsstyrda diffusion” som begränsar elektronläckage och ökar energiutbytet. I andra organismer verkar kortare gångjärn, olika superkomplexdesign eller till och med kovalenta förankringar tjäna ett liknande syfte—att hålla bärare nära där de behövs. Att förstå dessa subtila styrmekanismer kan hjälpa till att förklara varför defekter i kardiolipin eller superkomplexorganisation visar sig vid åldrande, hjärtsvikt och neurodegenerativa sjukdomar, och kan så småningom informera strategier för att finjustera cellernas energimetabolism.
Citering: Chan, C.K., Nguyen, J., Hryc, C.F. et al. Transient protein structure guides surface diffusion pathways for electron transport in membrane supercomplexes. Nat Commun 17, 2892 (2026). https://doi.org/10.1038/s41467-025-67110-y
Nyckelord: mitokondriella superkomplex, cytochrom c-diffusion, kardiolipin, elektrontransportkedja, QCR6-hinge