Clear Sky Science · pt
A estrutura proteica transitória guia as rotas de difusão na superfície para o transporte de elétrons em supercomplexos de membrana
Como as Células Protegem Suas Linhas de Energia
A cada segundo, as células do seu corpo movimentam bilhões de elétrons para produzir a molécula energética ATP. Se mesmo uma pequena fração desses elétrons vazar, podem formar substâncias reativas perigosas que danificam DNA, proteínas e lipídios. Este estudo investiga como pequenas “linhas de energia” proteicas na membrana interna das mitocôndrias guiam esses elétrons de forma segura e eficiente de uma estação para outra, revelando um papel surpreendente para trechos proteicos flexíveis, aparentemente desordenados, e para lipídios de membrana especiais.
A Rede Elétrica Atarefada Dentro das Mitocôndrias
No interior das mitocôndrias, a produção de energia ocorre por meio de uma cadeia de grandes máquinas proteicas embutidas na membrana. Duas estações-chave, conhecidas como Complexo III e Complexo IV, transferem elétrons usando uma pequena proteína transportadora chamada citocromo c. Tradicionalmente, os cientistas imaginavam o citocromo c flutuando em três dimensões pelo fluido interno até colidir com cada complexo. Mas muitos organismos também organizam esses complexos em agrupamentos chamados supercomplexos, o que levanta a questão de se montar esses agrupamentos realmente melhora a eficiência do transporte de elétrons ou apenas mantém a maquinaria organizada e reduz vazamentos acidentais.
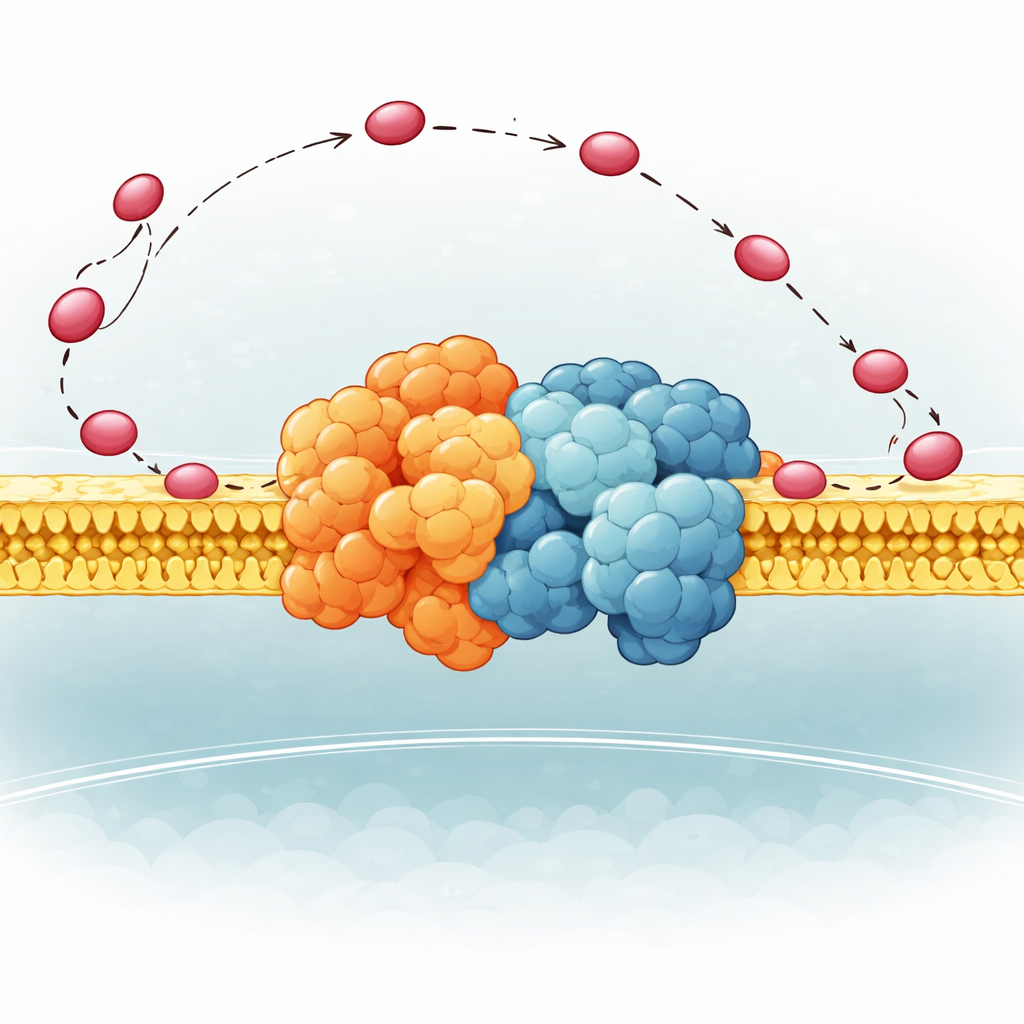
Uma Dobradiça Flexível que Orienta o Transportador
Os autores concentraram-se em uma pequena parte do Complexo III em levedura chamada QCR6, que tem um longo segmento “dobradiça” carregado negativamente cuja estrutura era muito flexível para ser capturada claramente antes. Usando uma combinação de métodos computacionais avançados — algoritmos de dobra proteica, dinâmica molecular e criomicroscopia eletrônica — eles geraram um conjunto de formas realistas que essa dobradiça pode assumir enquanto está ligada a um supercomplexo completo Complexo III–Complexo IV em uma membrana. Eles descobriram que QCR6 não fica imóvel: quando o citocromo c se aproxima, partes da dobradiça se enrolam em hélices temporárias e agarram o transportador; à medida que o citocromo c se move do Complexo III em direção ao Complexo IV, a dobradiça pode estender-se e parcialmente desdobrar-se, seguindo e guiando-o ao longo da superfície da membrana em vez de deixá-lo vagar pelo fluido circundante.
Os Lipídios de Membrana como Guias Invisíveis
A própria membrana também desempenha um papel ativo. A equipe substituiu lipídios genéricos em seus modelos por cardiolipina, um lipídio carregado negativamente conhecido por ser importante para mitocôndrias saudáveis e frequentemente alterado em doenças cardíacas e neurodegenerativas. As simulações mostraram que pontos carregados positivamente em QCR6 prendem-se às cabeças da cardiolipina, ancorando efetivamente a dobradiça à membrana enquanto ela escolta o citocromo c. Esse acoplamento torna energeticamente mais barato para o transportador deslizar do Complexo III para o Complexo IV ao longo da superfície, em vez de saltar aleatoriamente em três dimensões. Quando a cardiolipina foi removida, o custo energético dessa jornada aumentou acentuadamente, mais citocromos c derivaram para a solução bulk e sua posição tornou-se menos claramente direcionada ao sítio aceitador de elétrons.
Do Vaguear Aleatório ao Surf Guiado
Ao executar simulações de dinâmica browniana em grande escala, os pesquisadores rastrearam onde o citocromo c tende a permanecer ao redor do supercomplexo. Com uma dobradiça QCR6 intacta e lipídios aniônicos presentes, a maioria das moléculas de citocromo c permanece próxima à membrana e passa mais tempo perto dos sítios de contato produtivos no Complexo III e no Complexo IV. À medida que a dobradiça se estende, a nuvem preferida de posições do citocromo c desloca-se do lado do doador para o lado do aceitador, efetivamente “surfando” ao longo da superfície do complexo. Essa difusão guiada pela superfície melhora a rapidez com que os elétrons são transferidos sem tornar o citocromo c uma parte permanentemente presa da maquinaria; os transportadores ainda podem trocar livremente com o reservatório circundante.
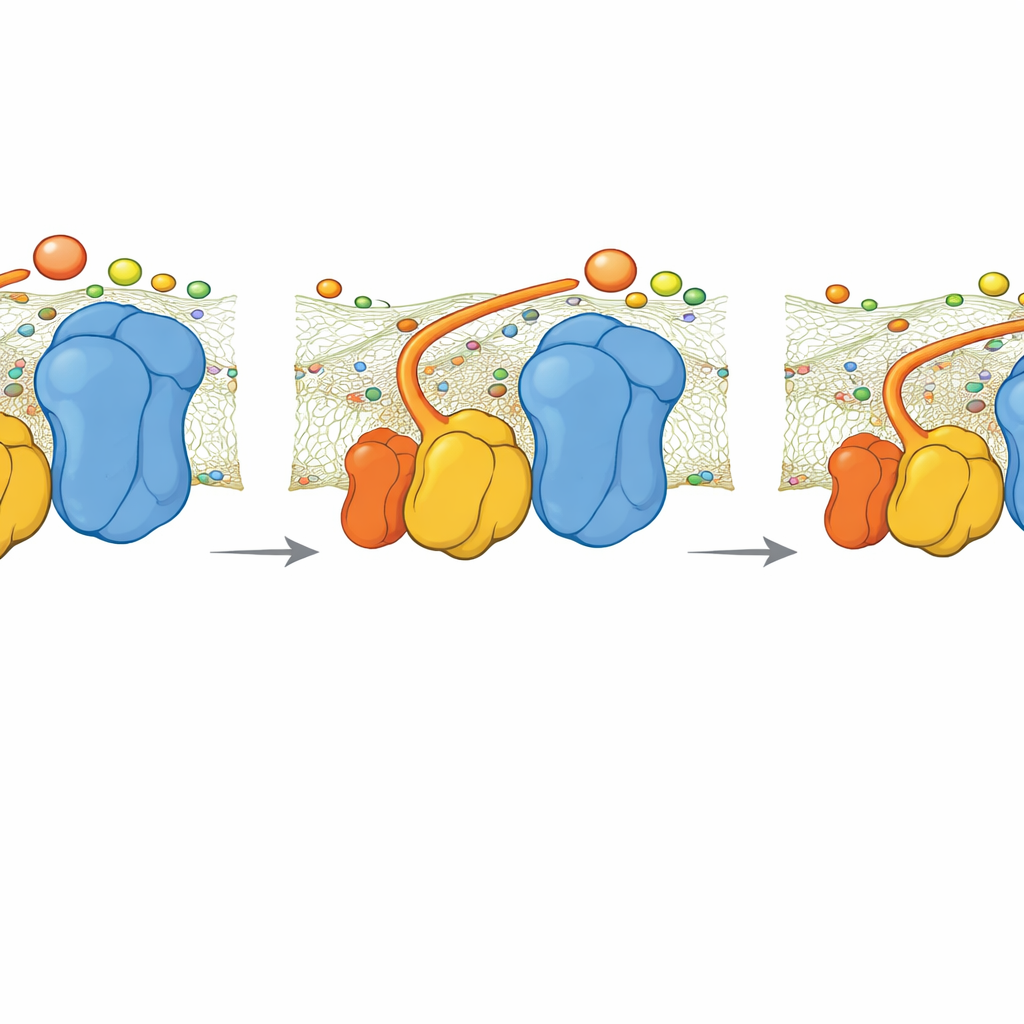
O Que Acontece Quando a Dobradiça Falta
A equipe também estudou uma cepa mutante de levedura sem QCR6. Imagens por criomicroscopia eletrônica mostraram que o supercomplexo se rearranja em uma forma mais compacta e ligeiramente diferente que restaura parcialmente uma carga negativa contínua pela superfície. Ainda assim, as simulações revelaram que, sem a dobradiça QCR6, a taxa com que o citocromo c transfere elétrons do Complexo III para o Complexo IV diminui. Um modelo cinético simples, ligando o fluxo de elétrons à produção de ATP, sugere que, sob alta demanda energética, essa perda de orientação poderia reduzir a produção de ATP em aproximadamente 30%. Em demandas mais baixas, a diferença é menor, porque uma difusão mais lenta e menos organizada ainda é suficiente.
Por Que Isso Importa para Saúde e Evolução
Em conjunto, o trabalho apoia um novo quadro: em vez de atuar como suportes estáticos, segmentos proteicos flexíveis e lipídios carregados cooperam para confinar os transportadores de elétrons à superfície da membrana e direcionar seu movimento ao longo de rotas seguras e produtivas. Em leveduras, uma dobradiça QCR6 incomumente longa e abundância de cardiolipina geram essa “difusão guiada por replegamento” que limita o vazamento de elétrons e aumenta a produção de energia. Em outros organismos, dobradiças mais curtas, projetos diferentes de supercomplexos ou mesmo amarras covalentes parecem servir ao mesmo objetivo — manter os transportadores próximos de onde são necessários. Compreender esses mecanismos sutis de orientação pode ajudar a explicar por que defeitos na cardiolipina ou na organização de supercomplexos aparecem no envelhecimento, na insuficiência cardíaca e em doenças neurodegenerativas, e pode, eventualmente, informar estratégias para ajustar o metabolismo energético celular.
Citação: Chan, C.K., Nguyen, J., Hryc, C.F. et al. Transient protein structure guides surface diffusion pathways for electron transport in membrane supercomplexes. Nat Commun 17, 2892 (2026). https://doi.org/10.1038/s41467-025-67110-y
Palavras-chave: supercomplexos mitocondriais, difusão de citocromo c, cardiolipina, cadeia de transporte de elétrons, dobradiça QCR6