Clear Sky Science · pl
Przejściowa struktura białka kieruje ścieżkami dyfuzji po powierzchni dla transportu elektronów w nadkompleksach błonowych
Jak komórki chronią swoje linie energetyczne
Co sekundę komórki twojego ciała przesuwają miliardy elektronów, by wytworzyć cząsteczkę energii ATP. Nawet niewielka część tych elektronów, która ucieknie, może tworzyć niebezpieczne reaktywne związki uszkadzające DNA, białka i lipidy. Badanie to analizuje, jak niewielkie „linie energetyczne” — białka na wewnętrznej błonie mitochondrium — prowadzą te elektrony bezpiecznie i wydajnie między kolejnymi stacjami, ujawniając zaskakującą rolę elastycznych, pozornie nieuporządkowanych fragmentów białkowych oraz specyficznych tłuszczów błonowych.
Gęsta sieć energetyczna wewnątrz mitochondriów
W mitochondriach produkcja energii przebiega przez łańcuch dużych maszyn białkowych osadzonych w błonie. Dwie kluczowe stacje, znane jako Kompleks III i Kompleks IV, przekazują elektrony z użyciem małego białkowego nośnika nazwanego cytochromem c. Tradycyjnie wyobrażano sobie cytochrom c dryfujący trójwymiarowo w wodnym wnętrzu, aż zderzy się z każdym kompleksem. Jednak wiele organizmów układa te kompleksy w skupiska zwane nadkompleksami, co rodzi pytanie, czy takie grupowanie faktycznie poprawia efektywność transferu elektronów, czy jedynie porządkuje mechanizmy i zmniejsza przypadkowe wycieki.
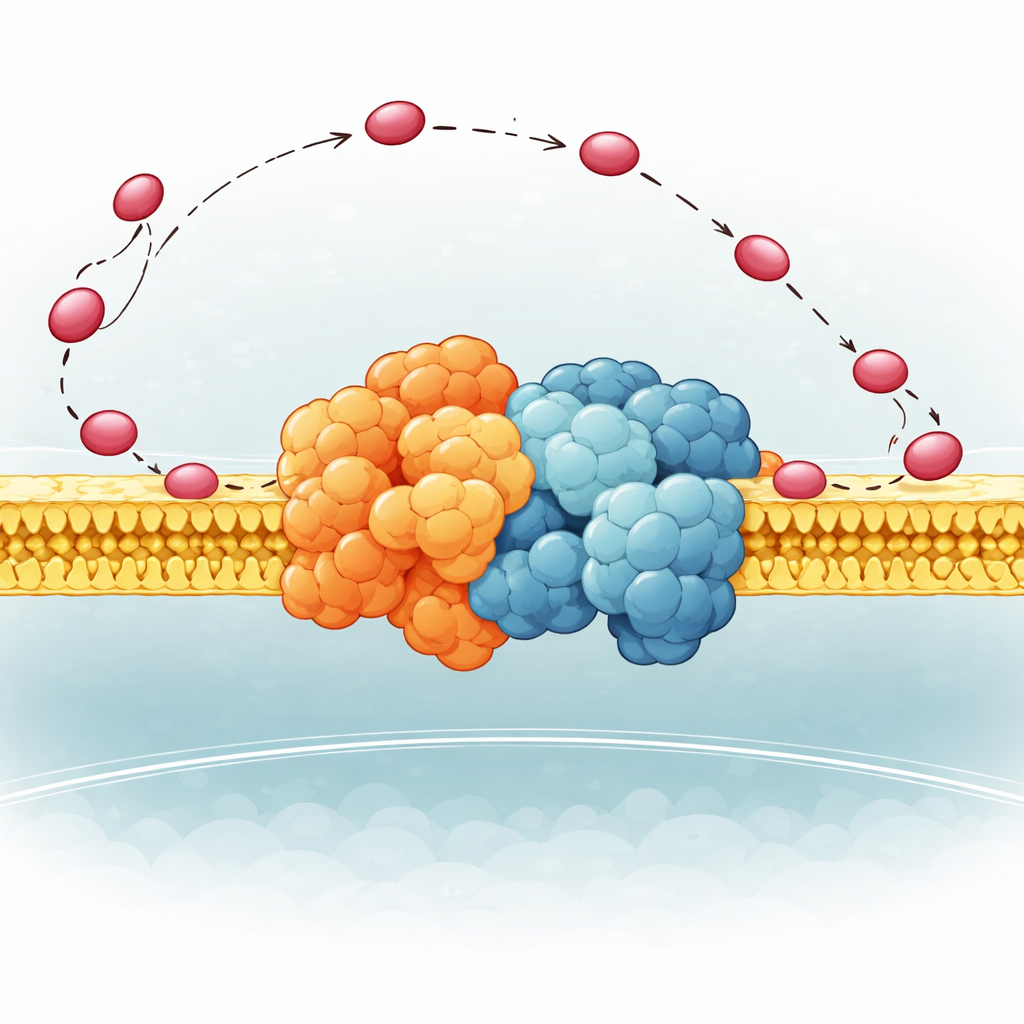
Elastyczny zawias, który kieruje nośnikiem
Autorzy skupili się na małym fragmencie Kompleksu III u drożdży nazwanym QCR6, który ma długi, ujemnie naładowany segment „zawiasu”, którego struktura była wcześniej zbyt ruchoma, aby ją precyzyjnie uchwycić. Wykorzystując kombinację zaawansowanych metod komputerowych — algorytmów fałdowania białek, dynamiki molekularnej i kriomikroskopii elektronowej — wygenerowali zespół realistycznych kształtów, które ten zawias może przyjmować będąc przyłączonym do pełnego nadkompleksu Kompleks III–Kompleks IV w błonie. Odkryli, że QCR6 nie jest nieruchomy: gdy cytochrom c zbliża się, fragmenty zawiasu tworzą tymczasowe helisy i chwytają nośnik; gdy cytochrom c przesuwa się od Kompleksu III w stronę Kompleksu IV, zawias może się wydłużać i częściowo rozwijać, podążając i kierując nim wzdłuż powierzchni błony, zamiast pozwolić mu błąkać się w otaczającym płynie.
Tłuszcze błonowe jako niewidzialni przewodnicy
Sama błona również odgrywa aktywną rolę. Zespół zastąpił w modelach uniwersalne lipidy kardiolipiną, ujemnie naładowanym tłuszczem znanym z istotnej roli w zdrowych mitochondriach, często zmienianym w chorobach serca i neurodegeneracji. Symulacje pokazały, że dodatnio naładowane miejsca na QCR6 zaczepiają się o grupy głowowe kardiolipiny, skutecznie przytwierdzając zawias do błony, gdy eskortuje cytochrom c. To sprzężenie obniża koszt energetyczny przesunięcia nośnika z Kompleksu III do Kompleksu IV wzdłuż powierzchni, zamiast losowego przeskakiwania w trzech wymiarach. Gdy usunięto kardiolipinę, koszt energetyczny tej podróży znacząco wzrósł, więcej cytochromu c odpłynęło do roztworu i jego pozycja stała się mniej wyraźnie ukierunkowana na miejsce przyjmujące elektrony.
Od przypadkowego błądzenia do prowadzonego surfowania
Dzięki przeprowadzeniu szeroko zakrojonych symulacji dynamiki Browna badacze śledzili, gdzie cytochrom c ma tendencję do pozostawania w pobliżu nadkompleksu. Przy nienaruszonym zawiasie QCR6 i obecności anionowych lipidów większość cząsteczek cytochromu c pozostaje blisko błony i spędza więcej czasu w pobliżu produktywnych miejsc kontaktu na Kompleksie III i Kompleksie IV. W miarę wydłużania się zawiasu preferowana chmura pozycji cytochromu c przesuwa się ze strony dawcy na stronę akceptora, efektywnie „surfując” po powierzchni kompleksu. Ta ukierunkowana dyfuzja powierzchniowa poprawia szybkość przekazywania elektronów, nie czyniąc z cytochromu c trwale przyłączonego elementu maszyny; nośniki nadal mogą swobodnie wymieniać się z otaczającą pulą.
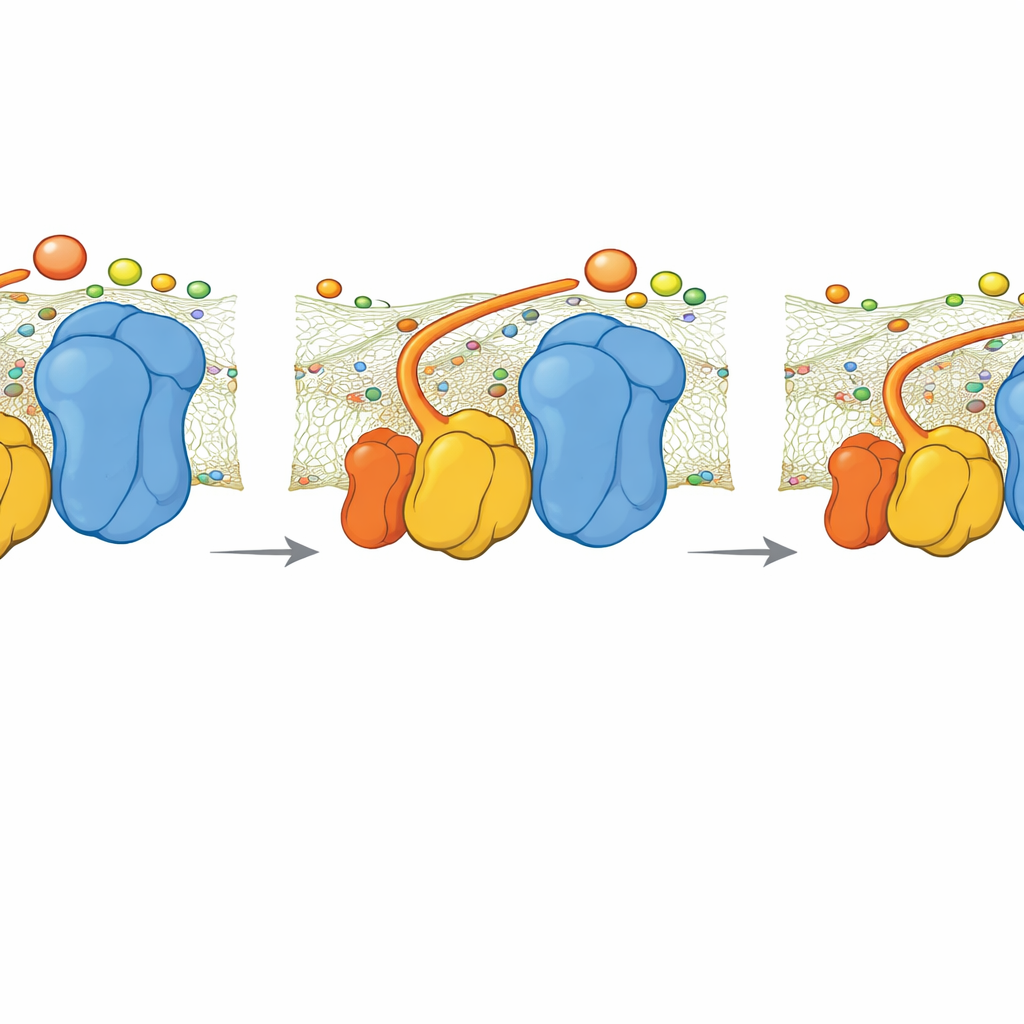
Co się dzieje, gdy zawias brakuje
Zespół przebadał też mutanty drożdży pozbawione QCR6. Obrazowanie kriomikroskopowe wykazało, że nadkompleks przebudowuje się do bardziej zwartego, nieco innego kształtu, który częściowo przywraca ciągły ładunek ujemny na powierzchni. Niemniej jednak symulacje ujawniły, że bez zawiasu QCR6 tempo, w jakim cytochrom c przekazuje elektrony z Kompleksu III do Kompleksu IV, spada. Prosty model kinetyczny łączący przepływ elektronów z produkcją ATP sugeruje, że przy dużym zapotrzebowaniu na energię utrata tego prowadzenia mogłaby obniżyć produkcję ATP o około 30 procent. Przy niższym zapotrzebowaniu różnica jest mniejsza, ponieważ wolniejsza, mniej zorganizowana dyfuzja nadal wystarcza.
Dlaczego to ma znaczenie dla zdrowia i ewolucji
W całości praca wspiera nowy obraz: zamiast działać jak statyczne rusztowania, elastyczne fragmenty białkowe i naładowane lipidy współpracują, by ograniczyć ruch nośników elektronów do powierzchni błony i uprzedzić ich ruch wzdłuż bezpiecznych, produktywnych tras. U drożdży nietypowo długi zawias QCR6 i obfita kardiolipina generują tę „dyfuzję kierowaną przez przefałdowanie”, która ogranicza wycieki elektronów i zwiększa wydajność energetyczną. U innych organizmów krótsze zawiasy, różne projekty nadkompleksów czy nawet kowalencyjne przytwierdzenia wydają się realizować podobny cel — utrzymywać nośniki blisko miejsc, gdzie są potrzebne. Zrozumienie tych subtelnych mechanizmów kierowania może pomóc wyjaśnić, dlaczego defekty kardiolipiny lub organizacji nadkompleksów pojawiają się w starzeniu, niewydolności serca i chorobach neurodegeneracyjnych, i w przyszłości może inspirować strategie pozwalające dostroić metabolizm energetyczny komórek.
Cytowanie: Chan, C.K., Nguyen, J., Hryc, C.F. et al. Transient protein structure guides surface diffusion pathways for electron transport in membrane supercomplexes. Nat Commun 17, 2892 (2026). https://doi.org/10.1038/s41467-025-67110-y
Słowa kluczowe: nadkompleksy mitochondrialne, dyfuzja cytochromu c, kardiolipina, łańcuch transportu elektronów, zawias QCR6