Clear Sky Science · ru
Переходная структура белка направляет пути поверхностной диффузии для электронного транспорта в мембранных суперкомплексах
Как клетки защищают свои «линии электропередачи»
Каждую секунду клетки вашего тела перемещают миллиарды электронов, чтобы синтезировать молекулу энергии АТФ. Если даже малая часть этих электронов утечет, они могут образовать реакционноспособные соединения, повреждающие ДНК, белки и липиды. В этом исследовании рассматривается, как крошечные «линии электропередачи» — белки на внутренней мембране митохондрий — направляют электроны безопасно и эффективно от одной станции к другой, выявляя неожиданную роль гибких, кажущихся неструктурированными участков белков и особых мембранных жиров.
Занятая энергосеть внутри митохондрий
Внутри митохондрий производство энергии проходит через цепочку крупных белковых машин, встроенных в мембрану. Две ключевые станции, известные как Комплекс III и Комплекс IV, передают электроны с помощью небольшого переносчика — цитохрома c. Традиционно учёные представляли, что цитохром c дрейфует в трёх измерениях в водной прослойке, пока не столкнётся с каждым комплексом. Но во многих организмах эти комплексы также группируются в скопления — суперкомплексы, что ставит вопрос: улучшает ли такая организация фактическую эффективность транспорта электронов или лишь упорядочивает машины и снижает случайные утечки.
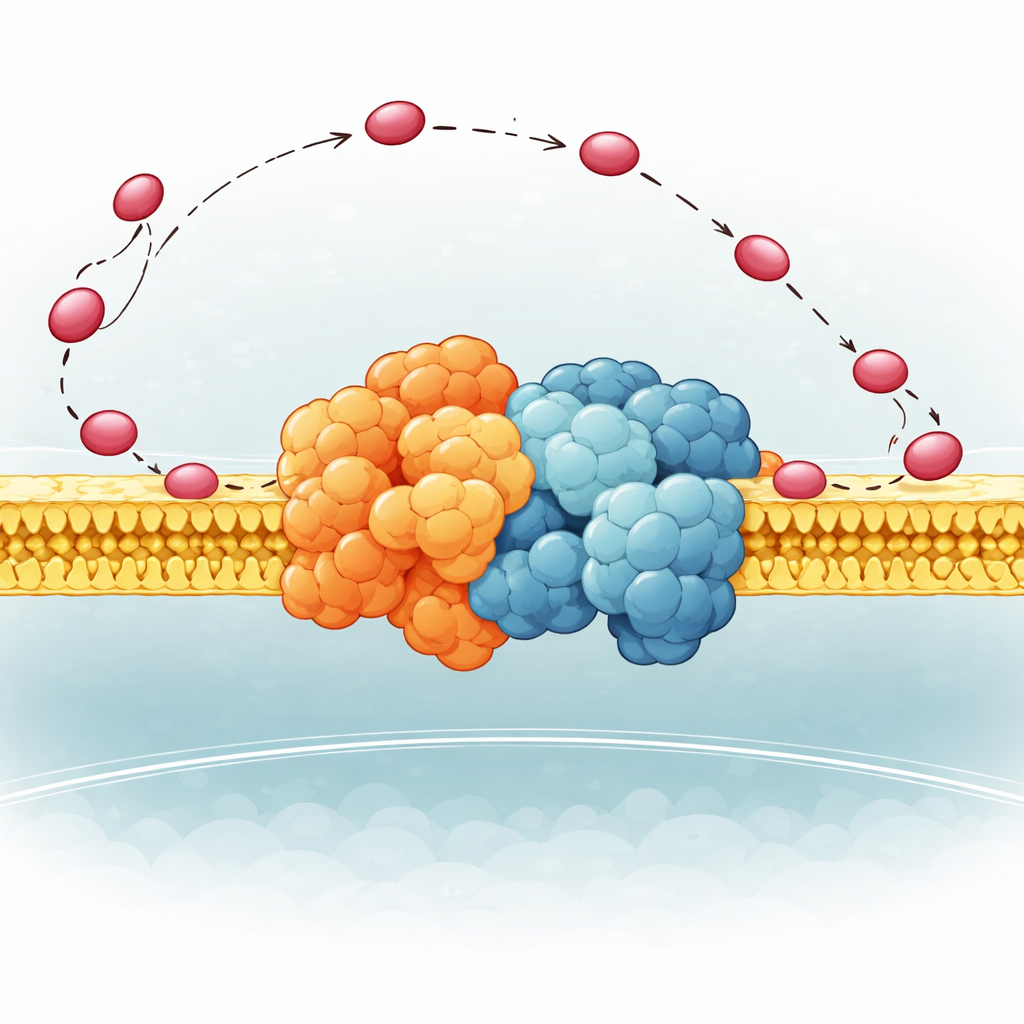
Гибкий шарнир, направляющий переносчик
Авторы сосредоточились на небольшой части Комплекса III у дрожжей, называемой QCR6, у которой есть длинный отрицательно заряженный «шарнир», структура которого ранее была слишком подвижной для чёткой фиксации. Сочетая современные вычислительные методы — алгоритмы предсказания сворачивания белков, молекулярную динамику и крио-электронную микроскопию — они получили ансамбль реалистичных форм, которые этот шарнир может принимать, оставаясь прикреплённым к полному суперкомплексу Комплекс III–Комплекс IV в мембране. Оказалось, что QCR6 не статичен: когда цитохром c приближается, части шарнира сворачиваются во временные спирали и захватывают переносчик; по мере перехода цитохрома c от Комплекса III к Комплексу IV шарнир может растягиваться и частично разворачиваться, следуя за ним и направляя его вдоль поверхности мембраны, вместо того чтобы позволять ему блуждать в окружающей жидкости.
Мембранные липиды как невидимые направляющие
Сама мембрана также играет активную роль. Исследователи заменили общие липиды в моделях кардиолипином — отрицательно заряженным липидом, важным для здоровых митохондрий и часто изменяющимся при сердечных и нейродегенеративных заболеваниях. Моделирование показало, что положительно заряженные участки QCR6 прилипают к головным группам кардиолипина, эффективно прикрепляя шарнир к мембране, пока он сопровождает цитохром c. Такое сопряжение удешевляет по энергии переход переносчика с Комплекса III на Комплекс IV вдоль поверхности, по сравнению с случайными перескоками в трёх измерениях. При удалении кардиолипина энергетические затраты на этот путь резко возрастали, большее число молекул цитохрома c уносилось в объём раствора, и их распределение становилось менее смещённым в сторону сайта, принимающего электроны.
От случайного блуждания к направленному «сёрфингу»
Проводя крупномасштабные симуляции броуновской динамики, исследователи отслеживали, где цитохром c склонен задерживаться вокруг суперкомплекса. При наличии целого шарнира QCR6 и анионных липидов большинство молекул цитохрома c остаётся близко к мембране и проводит больше времени у продуктивных контактных участков на Комплексе III и Комплексе IV. По мере удлинения шарнира предпочтительное облако позиций цитохрома смещается с донорской стороны на акцепторную, фактически «сёрфя» по поверхности комплекса. Эта направленная поверхностная диффузия повышает скорость передачи электронов, не превращая цитохром c в постоянно прикреплённую часть механизма; переносчики по-прежнему могут свободно обмениваться с окружающим пулом.
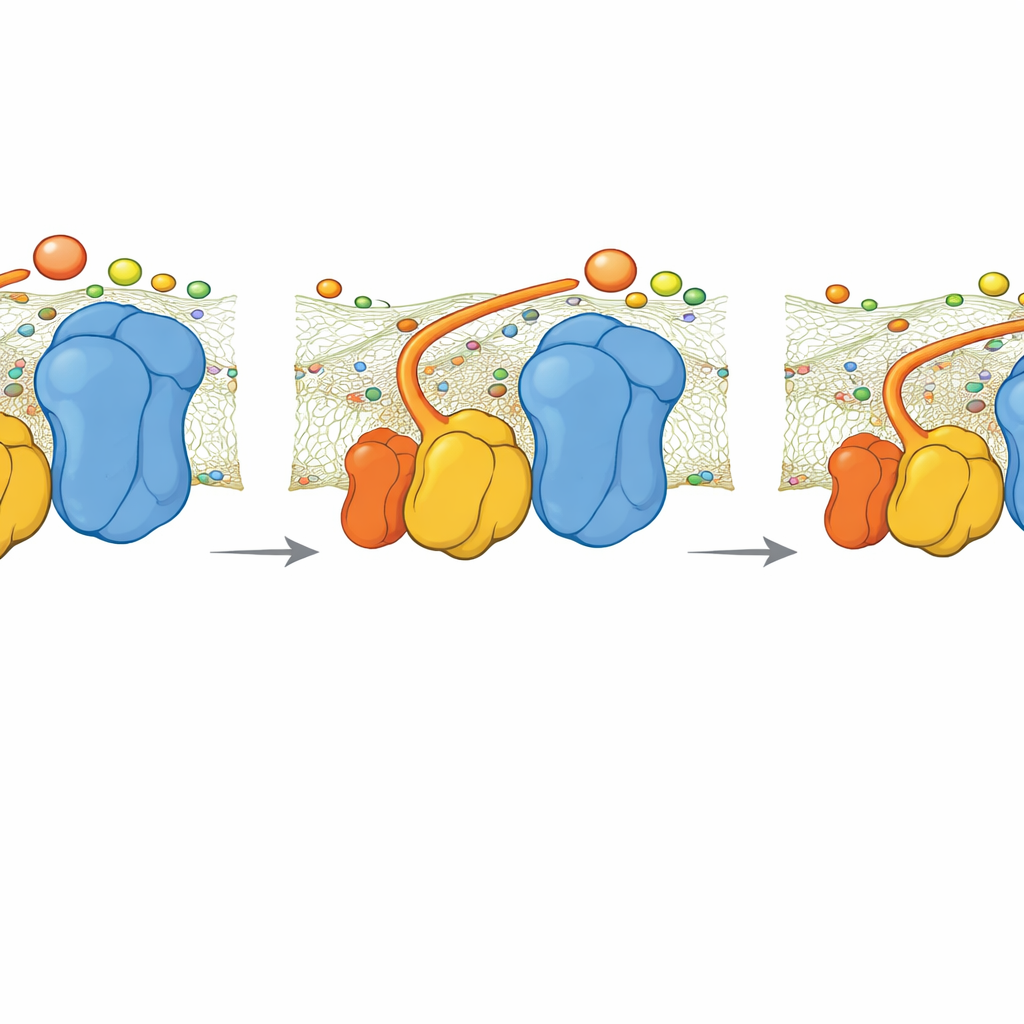
Что происходит, когда шарнира нет
Команда также изучала мутантный штамм дрожжей без QCR6. Крио-ЭМ показала, что суперкомплекс перестраивается в более компактную, слегка отличную форму, которая частично восстанавливает непрерывный отрицательный заряд на поверхности. Тем не менее моделирование выявило, что без шарнира QCR6 скорость, с которой цитохром c переносит электроны от Комплекса III к Комплексу IV, снижается. Простейшая кинетическая модель, связывающая поток электронов с выходом АТФ, показывает, что при высокой потребности в энергии потеря такого «наведения» может сократить производство АТФ примерно на 30 процентов. При более низком спросе разница меньше, потому что более медленная, менее организованная диффузия всё ещё достаточна.
Значение для здоровья и эволюции
В целом работа поддерживает новую картину: вместо того чтобы быть статическими каркасами, гибкие участки белков и заряженные липиды сотрудничают, ограничивая переносчики электронов поверхностью мембраны и смещая их движение по безопасным, продуктивным маршрутам. У дрожжей необычно длинный шарнир QCR6 и обилие кардиолипина создают этот механизм «рефолдинг-направляемой диффузии», который ограничивает утечки электронов и повышает выработку энергии. У других организмов короче шарниры, иные конструкции суперкомплексов или даже ковалентные привязки, по-видимому, служат той же цели — держать переносчики ближе к месту их необходимости. Понимание этих тонких направляющих механизмов может помочь объяснить, почему дефекты кардиолипина или организации суперкомплексов проявляются при старении, сердечной недостаточности и нейродегенеративных заболеваниях, и в перспективе может помочь в разработке стратегий тонкой настройки клеточного энергообмена.
Цитирование: Chan, C.K., Nguyen, J., Hryc, C.F. et al. Transient protein structure guides surface diffusion pathways for electron transport in membrane supercomplexes. Nat Commun 17, 2892 (2026). https://doi.org/10.1038/s41467-025-67110-y
Ключевые слова: митохондриальные суперкомплексы, диффузия цитохрома c, кардиолипин, цепь переноса электронов, шарнир QCR6