Clear Sky Science · nl
Voorbijgaande eiwitstructuur leidt oppervlakte-diffusiepaden voor elektronentransport in membraan-supercomplexen
Hoe cellen hun energienet veilig houden
Elke seconde verplaatsen de cellen in je lichaam miljarden elektronen om het energiemolecuul ATP te vormen. Als zelfs een klein deel van die elektronen weglekt, kunnen ze gevaarlijke reactieve stoffen vormen die DNA, eiwitten en vetten beschadigen. Deze studie onderzoekt hoe kleine “stroomlijn”-eiwitten op het binnenmembraan van mitochondriën deze elektronen veilig en efficiënt van het ene station naar het andere leiden, en onthult een verrassende rol voor flexibele, schijnbaar ongeordende eiwitsegmenten en specifieke membraanfetten.
Het drukke energienet binnen mitochondriën
In mitochondriën loopt energieproductie via een keten van grote eiwitmachines ingebed in een membraan. Twee sleutelstations, Complex III en Complex IV, geven elektronen door met behulp van een klein draagereiwit genaamd cytochroom c. Traditioneel zagen wetenschappers cytochroom c als vrij rondbewegend in drie dimensies door de waterige ruimte totdat het tegen een complex aanbotst. Veel organismen ordenen deze complexen echter ook in clusters die supercomplexen worden genoemd, wat de vraag oproept of zulke clusters daadwerkelijk de efficiëntie van de elektronenoverdracht verbeteren, of alleen de machines georganiseerd houden en accidentele lekkage verminderen.
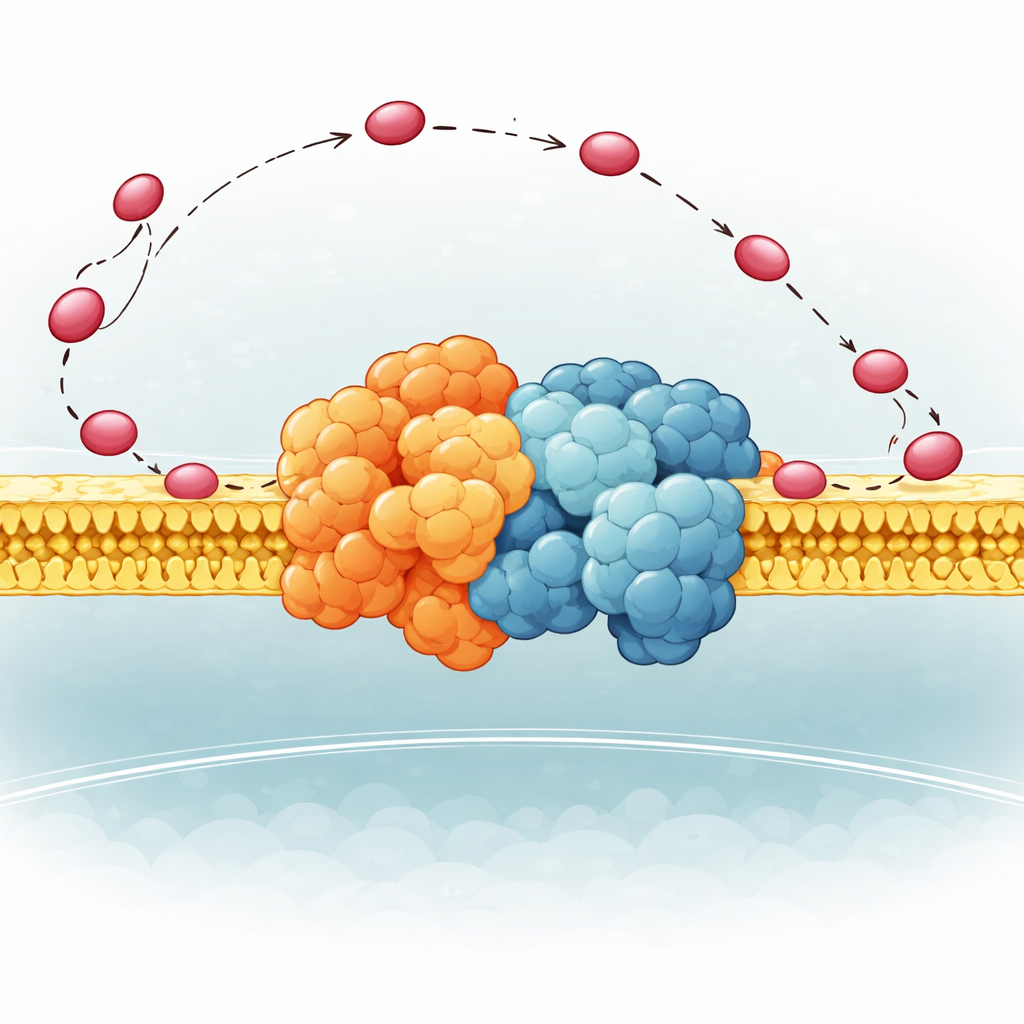
Een flexibel scharnier dat de drager stuurt
De auteurs concentreerden zich op een klein onderdeel van Complex III in gist, genoemd QCR6, dat een lang, negatief geladen “scharnier”segment heeft waarvan de structuur tot nu toe te beweeglijk was om duidelijk vast te leggen. Met een combinatie van geavanceerde rekenmethoden — eiwitvouwingalgoritmen, moleculaire dynamica en cryo-elektronmicroscopie — genereerden ze een ensemble van realistische vormen die dit scharnier kan aannemen terwijl het vastzit aan een volledig Complex III–Complex IV-supercomplex in een membraan. Ze vonden dat QCR6 niet stilstaat: wanneer cytochroom c in de buurt komt, vouwen delen van het scharnier tijdelijk tot helices en grijpen de drager; terwijl cytochroom c zich van Complex III naar Complex IV beweegt, kan het scharnier uitrekken en gedeeltelijk ontvouwen, het volgend en geleidend langs het membraanoppervlak in plaats van het te laten afdwalen in de omliggende vloeistof.
Membraanfetten als onzichtbare gidsen
Het membraan zelf speelt ook een actieve rol. Het team verving generieke lipiden in hun modellen door cardiolipine, een negatief geladen vet dat belangrijk is voor gezonde mitochondriën en vaak verandert bij hartziekte en neurodegeneratie. Simulaties toonden aan dat positief geladen plekken op QCR6 zich vasthechten aan cardiolipinekopgroepen, waardoor het scharnier effectief aan het membraan wordt bevestigd terwijl het cytochroom c begeleidt. Deze koppeling maakt het energetisch voordeliger voor de drager om van Complex III naar Complex IV langs het oppervlak te schuiven in plaats van willekeurig in drie dimensies te hoppen. Wanneer cardiolipine werd verwijderd, steeg de energetische kosten van deze reis sterk, meer cytochroom c dreef in de bulkoplossing en werd de plaatsing minder duidelijk gebiased richting de elektronacceptor.
Van willekeurig dwalen naar geleide surfsessies
Door grootschalige Browniaanse dynamicasimulaties uit te voeren, volgden de onderzoekers waar cytochroom c de neiging heeft te vertoeven rond het supercomplex. Met een intact QCR6-scharnier en aanwezige anionische lipiden blijven de meeste cytochroom c-moleculen dicht bij het membraan en brengen ze meer tijd door in de buurt van productieve contactplaatsen op Complex III en Complex IV. Wanneer het scharnier zich uitstrekt, verschuift de voorkeurswolk van cytochroom c-posities van de donorzijde naar de acceptorzijde en surft het als het ware langs het oppervlak van het complex. Deze geleide oppervlaktediffusie verbetert hoe snel elektronen kunnen worden overgedragen zonder van cytochroom c een permanent gebonden onderdeel van de machinerie te maken; dragers kunnen nog steeds vrij uitwisselen met de omringende pool.
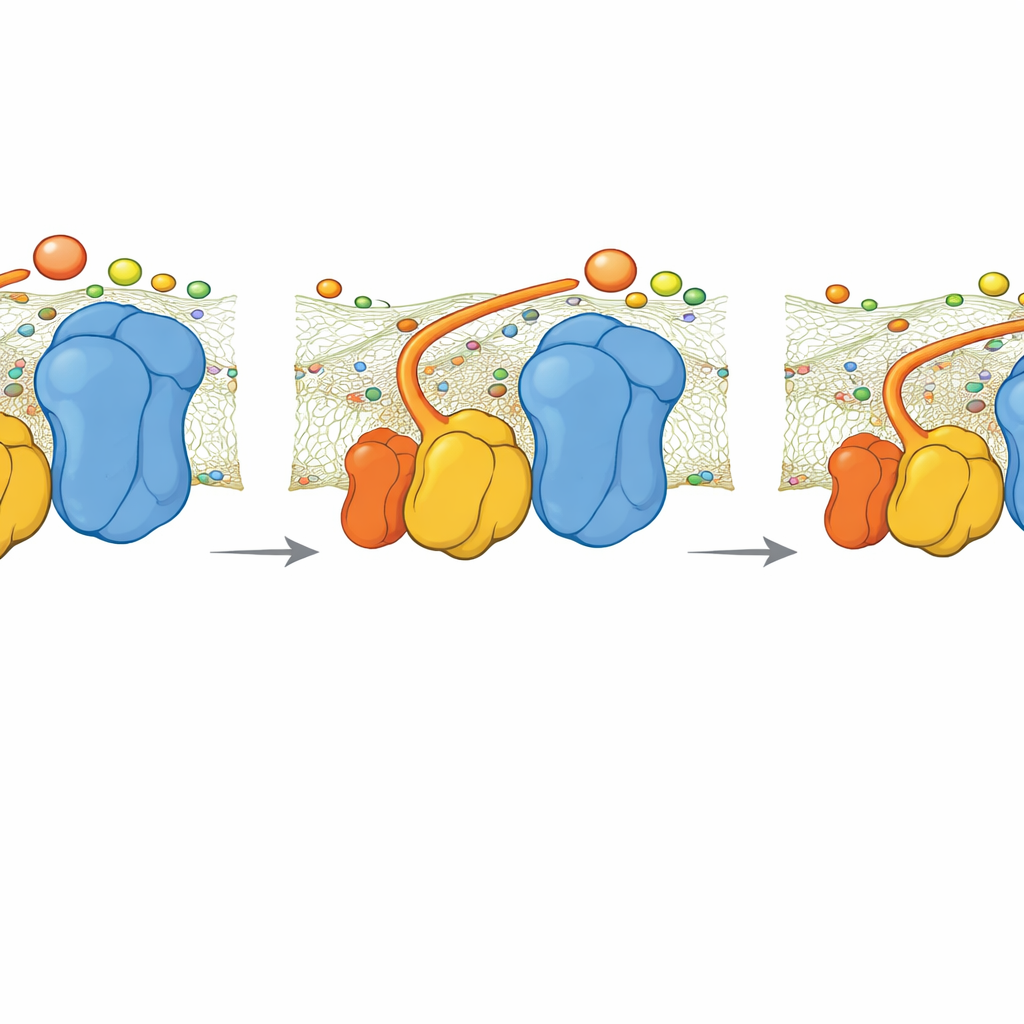
Wat gebeurt er als het scharnier ontbreekt
Het team bestudeerde ook een mutantgiststam zonder QCR6. Cryo-EMbeelden toonden dat het supercomplex zich herschikt tot een compactere, iets andere vorm die gedeeltelijk een doorlopende negatieve lading over het oppervlak herstelt. Desalniettemin lieten simulaties zien dat zonder het QCR6-scharnier de snelheid waarmee cytochroom c elektronen van Complex III naar Complex IV verplaatst daalt. Een eenvoudig kinetisch model dat elektronenstroom koppelt aan ATP-opbrengst suggereert dat bij hoge energievraag dit verlies aan sturing de ATP-productie met ongeveer 30 procent zou kunnen verminderen. Bij lagere vraag is het verschil kleiner, omdat langzamere, minder georganiseerde diffusie nog steeds volstaat.
Waarom dit belangrijk is voor gezondheid en evolutie
Samengenomen ondersteunt het werk een nieuw beeld: in plaats van te fungeren als statische steigers werken flexibele proteïnesegmenten en geladen lipiden samen om draagereiwitten aan het membraanoppervlak te beperken en hun beweging te sturen langs veilige, productieve routes. In gist genereren een uitzonderlijk lang QCR6-scharnier en overvloedige cardiolipine deze “hervouwings-geleide diffusie” die elektronenlekkage beperkt en energieopbrengst verhoogt. In andere organismen lijken kortere scharnieren, verschillende supercomplexontwerpen of zelfs covalente verbindingen hetzelfde doel te dienen — dragers dicht bij de plaats waar ze nodig zijn houden. Inzicht in deze subtiele stuurmechanismen kan helpen verklaren waarom defecten in cardiolipine of supercomplexorganisatie zichtbaar worden bij veroudering, hartfalen en neurodegeneratieve ziekten, en kan uiteindelijk strategieën informeren om de cellulaire energiemetabolisme fijn af te stemmen.
Bronvermelding: Chan, C.K., Nguyen, J., Hryc, C.F. et al. Transient protein structure guides surface diffusion pathways for electron transport in membrane supercomplexes. Nat Commun 17, 2892 (2026). https://doi.org/10.1038/s41467-025-67110-y
Trefwoorden: mitochondriale supercomplexen, diffusie van cytochroom c, cardiolipine, elektronentransportketen, QCR6 scharnier